推荐厂家
暂无
暂无


 400-825-5669
400-825-5669
 留言咨询
留言咨询

 400-860-5168转4978
400-860-5168转4978
 留言咨询
留言咨询

 400-860-5168转4978
400-860-5168转4978
 留言咨询
留言咨询



一、实验目的与原理质粒多为一些双链、环状的DNA分子,是独立于细菌染色体之外进行复制和遗传的辅助性遗传单位。质粒是进行分子生物学实验操作,进行遗传工程改良物种等工作时最主要的DNA载体。提取质粒的基本步骤分为三步:①细菌的培养和质粒的扩增②细菌菌体的裂解③质粒DNA的纯化本实验采取的菌体裂解方法为碱解法,质粒纯化方法为梯度离心法。二、材料与试剂1、材料:大肠杆菌2、仪器:超净工作台,培养箱,摇床,恒温水浴锅,台式离心机,取液器一套,低温冰箱,冷冻真空干燥机,电泳仪,水平电泳槽,紫外观测仪3、试剂:Solution I 25 mM Tris-Hcl(pH7.4) 10 mM EDTA(pH8.0) 50 mM葡萄糖 高压灭菌,4℃保存 Solution II 0.2 M NaOH, 1%SDS 现配现用 Solution III 5 N KAc pH4.8 高压灭菌,4℃保存 3 M NaAc PH5.2, 高压灭菌,4℃保存。异丙醇,溶菌酶(8 mg/ml),酚/氯仿,无水乙醇,70%乙醇,LB培养基,电泳试剂三、操作步骤1、细菌繁殖LB培养基,2 ml/20ml,37℃,200rpm,摇一摇,过夜2、离心10 min,5000 rpm, 4℃;弃上淸液3、沉淀(菌体细胞)预冷的TES缓冲液洗涤,离心10 min,5000 rpm, 4℃加入预冷的1 ml Solution I,冰浴,10 min4、重新悬浮,加入150 ul溶菌酶母液,室温放置5 min5、加入1.2 ml Solution II, 冰浴,5 min6、加入0.9 ml预冷乙酸钾,混匀,离心10 min,12000 rpm, 4℃7、加入1.5 ml异丙醇,-20℃冰箱内放置15 min8、离心10 min,12000 rpm, 4℃9、取沉淀,悬于400 ul TE缓冲液中10、加入40 ul,3 M NaAc11、酚/氯仿,抽提,乙醇沉淀12、离心10 min,12000 rpm, 4℃13、取沉淀,冷冻干燥,再悬浮于50 ul TE缓冲液中。14、电泳检测提取DNA的质量四、结果与分析超螺旋结构DNA
[font=宋体][font=宋体]质粒[/font][font=Calibri]DNA[/font][font=宋体]的质量和纯度对于生命科学实验至关重要。本文将系统地介绍确定质粒[/font][font=Calibri]DNA[/font][font=宋体]质量[/font][font=Calibri]/[/font][font=宋体]纯度的最佳方法,包括实验室检测与生物信息学分析,旨在为研究人员提供专业、准确和可靠的评估手段。[/font][/font][font=宋体] [/font][b][font=宋体][font=Calibri]1. [/font][font=宋体]引言[/font][/font][/b][font=宋体] [/font][font=宋体][font=宋体]质粒[/font][font=Calibri]DNA[/font][font=宋体]在生物科学研究中扮演着关键角色,涉及基因表达、基因治疗、基因组编辑等多个领域。因此,确保质粒[/font][font=Calibri]DNA[/font][font=宋体]的质量和纯度对于实验的成功至关重要。随着技术的不断发展,确定质粒[/font][font=Calibri]DNA[/font][font=宋体]质量[/font][font=Calibri]/[/font][font=宋体]纯度的方法也在不断改进和完善。[/font][/font][font=宋体] [/font][b][font=宋体][font=Calibri]2. [/font][font=宋体]质粒[/font][font=Calibri]DNA[/font][font=宋体]质量的评估[/font][/font][/b][font=宋体] [/font][font=宋体][font=宋体]评估质粒[/font][font=Calibri]DNA[/font][font=宋体]质量的方法主要包括电泳分析、酶切鉴定和生物信息学比对。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]2.1 [/font][font=宋体]电泳分析:琼脂糖凝胶电泳是最常用的方法。通过观察电泳图谱,可以判断[/font][font=Calibri]DNA[/font][font=宋体]是否完整,是否存在降解现象。[/font][/font][font=宋体][font=Calibri]2.2 [/font][font=宋体]酶切鉴定:使用限制性内切酶对质粒[/font][font=Calibri]DNA[/font][font=宋体]进行酶切,再通过电泳分离酶切产物。如果酶切产物的大小与预期一致,说明质粒[/font][font=Calibri]DNA[/font][font=宋体]的结构是正确的。[/font][/font][font=宋体][font=Calibri]2.3 [/font][font=宋体]生物信息学比对:利用基因组学和序列分析工具,对质粒[/font][font=Calibri]DNA[/font][font=宋体]的序列进行比对,检测是否存在突变、插入或缺失等变异。[/font][/font][font=宋体] [/font][b][font=宋体][font=Calibri]3. [/font][font=宋体]质粒[/font][font=Calibri]DNA[/font][font=宋体]纯度的评估[/font][/font][/b][font=宋体] [/font][font=宋体][font=宋体]评估质粒[/font][font=Calibri]DNA[/font][font=宋体]纯度的方法主要包括紫外分光光度计测定、高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法和生物信息学分析。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]3.1 [/font][font=宋体]紫外分光光度计测定:在[/font][font=Calibri]260[/font][font=宋体]纳米处测定吸光度值,可以计算出[/font][font=Calibri]DNA[/font][font=宋体]的浓度。同时观察[/font][font=Calibri]A260/A280[/font][font=宋体]比值,纯度良好的质粒[/font][font=Calibri]DNA[/font][font=宋体]在该波长下的吸光度值应该较高,且[/font][font=Calibri]A260/A280[/font][font=宋体]比值应接近[/font][font=Calibri]1.8[/font][font=宋体]。[/font][/font][font=宋体][font=Calibri]3.2 [/font][font=宋体]高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法([/font][font=Calibri]HPLC[/font][font=宋体]):可以分离和测定质粒[/font][font=Calibri]DNA[/font][font=宋体]的组成和浓度,具有较高的灵敏度和特异性,能够检测到低浓度的杂质。[/font][/font][font=宋体][font=Calibri]3.3 [/font][font=宋体]生物信息学分析:利用软件工具对质粒[/font][font=Calibri]DNA[/font][font=宋体]的序列进行分析,预测可能的杂质成分,如蛋白质、[/font][font=Calibri]RNA[/font][font=宋体]等。[/font][/font][font=宋体] [/font][b][font=宋体][font=Calibri]4. [/font][font=宋体]结论[/font][/font][/b][font=宋体] [/font][font=宋体][font=宋体]确定质粒[/font][font=Calibri]DNA[/font][font=宋体]质量[/font][font=Calibri]/[/font][font=宋体]纯度的最佳方法需要综合运用多种手段。实验室检测方法如电泳分析、紫外分光光度计测定和高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法提供了快速、直观的结果。而生物信息学分析则从序列和组分的角度提供了深入的洞察,使研究人员能够更全面地了解质粒的属性和潜在问题。结合这两类方法,研究人员可以获得关于质粒[/font][font=Calibri]DNA[/font][font=宋体]质量[/font][font=Calibri]/[/font][font=宋体]纯度的准确、可靠的信息,从而确保实验结果的准确性。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州提供快速、高通量、高品质以及个性化的[url=https://cn.sinobiological.com/services/plasmid-dna-preparation-service][b]质粒[/b][/url][/font][font=Calibri][url=https://cn.sinobiological.com/services/plasmid-dna-preparation-service][b]DNA[/b][/url][/font][font=宋体][url=https://cn.sinobiological.com/services/plasmid-dna-preparation-service][b]制备服务[/b][/url]。不仅满足实验室研究人员的小量质粒[/font][font=Calibri]DNA[/font][font=宋体]制备需求,也可为生物工业用户和医药公司等提供大规模的质粒[/font][font=Calibri]DNA[/font][font=宋体]制备服务。义翘神州升级改造后的质粒[/font][font=Calibri]DNA[/font][font=宋体]制备平台,采用[/font][font=Calibri]GMP[/font][font=宋体]级别的生产线,对过程和最终产品的严格管控,确保了最终产品质量符合客户需求。义翘神州可以提供从μ[/font][font=Calibri]g[/font][font=宋体]级别,[/font][font=Calibri]mg[/font][font=宋体]级别至[/font][font=Calibri]g[/font][font=宋体]级别不同规模的科研级和工业级别的质粒生产服务,满足不同的需求。详情关注:[/font][font=Calibri]https://cn.sinobiological.com/services/plasmid-dna-preparation-service[/font][/font][font=宋体] [/font][b][font=宋体][font=宋体]义翘神州:蛋白与抗体的专业引领者,欢迎通过百度搜索[/font][font=宋体]“义翘神州”与我们取得联系。[/font][/font][/b]
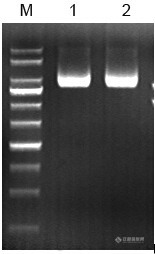
利用硅胶膜法提取纯化质粒DNA摘要:系统的阐述了质粒核酸提取过程中针对裂解和核酸纯化两大关键步骤的研究,重点介绍了利用硅胶膜法提取纯化核酸,以及在实验过程中的一些经验。关键词:硅胶膜法;纯化;质粒DNA一、前言随着分子生物学技术的发展,核酸的分子生物学技术成为了药物研发、遗传病和感染性疾病的诊断、基因研究及物种鉴定等的常用研究手段之一。然而,核酸提取质量是进行下游一系列研究的关键,因此提取的方法会直接影响后续实验。细菌质粒是一类双链闭合环状的DNA,大小范围从1kb至200kb以上不等。各种质粒都是存在于细胞质中、独立于细胞染色体之外的自主复制的遗传成份。质粒已成为目前最常用的基因克隆的载体分子,重要的条件是可获得大量纯化的质粒DNA分子。硅胶膜法是一种应用最为广泛的提取纯化质粒DNA的方法,因硅基质材料可特异吸附核酸DNA,使用方便、快捷,不需要使用有毒溶剂如酚、氯仿等,使得提取质粒核酸像过滤一样简单。二、实验部分2.1 原理硅基质材料吸附核酸的原理主要利用DNA在高盐低pH值环境下与硅基质材料相结合,在低盐高pH值环境下与硅基质材料脱离的特征。其机理是带负电荷的DNA和带正电的二氧化硅粒子之间有很强的亲和力。在高浓度盐离子的作用下,盐离子打破水中的氢和二氧化硅上带负电荷的氧离子间的氢键,DNA与硅基质紧密结合,洗涤除去其他杂质;再用低离子强度的TE缓冲液或蒸馏水洗脱结合的DNA分子,机理是当盐被清除后,再水化的硅基质破坏了基质和DNA之间的吸引力,因而DNA从硅基质上被洗脱下来。2.2 主要试剂溶液Ⅰ:50mM葡萄糖,25mM Tris-HCl(pH 8.0),10mM EDTA(pH 8.0)。溶液Ⅱ:0.2NNaOH,1% SDS。溶液Ⅲ:醋酸钾(KAc)缓冲液,pH 4.8。漂洗液:60mM 乙酸钾、10mM Tris-HCl (pH 7.5) 、60% 乙醇TE:10mMTris-HCl(pH 8.0),1mM EDTA(pH 8.0)。2.3 主要步骤该步骤采用CommaPrePTM的质粒小提纯化柱。http://ng1.17img.cn/bbsfiles/images/2015/07/201507171513_556042_3310_3.jpgCommaPrep™核酸小提柱可用在核酸提取过程中过柱结合、洗涤、洗脱步骤中http://ng1.17img.cn/bbsfiles/images/2015/07/201507171516_556043_3310_3.jpg1. 取1.5ml过夜培养的菌液,加入离心管中,使用常规台式离心机,12,000 rpm 离心1 min, 尽量吸除上清。 (注意:应根据所培养菌体的浓度与质粒的拷贝数,确定收集的菌液量。菌量过大可能导致溶菌不充分,纯化时会影响质粒纯度菌液较多时可以通过多次离心将菌体沉淀收集到一个离心管中)。2. 将细菌沉淀重悬于100uL溶液Ⅰ中,移液器或涡旋振荡器彻底悬浮细菌沉淀,使菌体分 散混匀。 (注意:如果有未彻底混匀的菌块,会影响裂解,导致提取量和纯度偏低。并且溶液Ⅰ中 要加入适量的RNA酶)3. 向离心管中加入200uL溶液Ⅱ,温和地上下翻转数次,并将离心管放置于冰上2-3min,使细胞膜裂解。(注意:温和地混合,不要剧烈震荡,以免污染基因组DNA。此时菌液应变得清亮,如果未变得清亮,可能由于菌体过多,裂解不彻底,应减少菌体量。)4. 加入150uL溶液Ⅲ,立即将管温和颠倒数次混匀,见白色絮状沉淀。12000rpm, 离心2分钟。 (注意:加入溶液Ⅲ后,要立即将管温和颠倒,避免产生局部沉淀。如果上清液中存在沉淀,可再一次离心。溶液Ⅲ为中和溶液,此时质粒DNA复性,染色体和蛋白质不可逆变性,形成不可溶复合物。)5. 吸取上清至吸附柱(内管)中(吸附柱在离心管中),尽量不要吸出沉淀,12000rpm,离心30秒。弃去废液,将吸附柱重新放入一个新的离心管中。6. 加入750uL的漂洗液(漂洗液要在实验前加入无水乙醇)12000rpm离心,1min。取出 DNA结合柱,弃废液,重新插入DNA结合柱到离心管中。7. 用500uL漂洗液重复冲洗过程。12000rpm离心,1min。(注意:重复一次可以增加质粒的回收效率。)8. 转移DNA结合柱到1个新的1.5mL离心管中,加入60uL的无核酸酶的水到DNA结合柱中,洗脱质粒DNA,室温条件下,12000rpm离心,1min。 (注意:不要转入DNA结合柱中的漂洗液,如果混有,就需要12000rpm离心,1min。洗脱缓冲液体积不少于50uL,体积小会影响回收效率。 洗脱液的pH值对于洗脱效率有很大的影响,若用水洗脱应保证pH值在7.0-8.5范围内, pH小于7会降低洗脱效率。如果长期保存DNA,洗脱液建议使用TE。)9. 加入100uL的无核酸酶水到结合柱中,洗脱质粒DNA,离心12000rpm,1min。(注意:重复一次,增加洗脱效率。)10.洗脱DNA后,从1.5mL离心管中取出DNA结合柱并废弃。11.取2uLDNA进行电泳,检测DNA质量。12.将纯化的DNA溶液于-20℃中。三、实验结果图为质粒DNA(10kb)的凝胶电泳图,说明提取效果较好。http://ng1.17img.cn/bbsfiles/images/2015/07/201507171525_556044_3310_3.jpg


