推荐厂家
暂无
暂无
 银牌9年
银牌9年
 400-860-5168转3750
400-860-5168转3750
 留言咨询
留言咨询
 留言咨询
留言咨询
 留言咨询
留言咨询

 400-628-5299
400-628-5299
 留言咨询
留言咨询
 400-803-1678
400-803-1678
 留言咨询
留言咨询

 400-877-0075
400-877-0075
 留言咨询
留言咨询





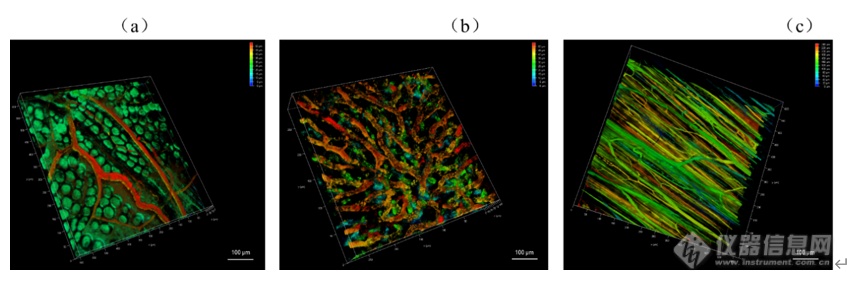
[align=center][b]双光子激光扫描显微镜的检测模式及其在生物医学领域的应用[/b][/align][align=center][font=宋体]刘皎[/font][sup]1[/sup],吴晶[sup]1[/sup][/align][align=center]1. [font=宋体]北京大学医药卫生分析中心,北京,[/font]100191[/align][b][font=黑体][[/font]摘要] [/b]双光子激光扫描显微镜(two-photon laser scan microscope, TPLSM[font=宋体])具有低光毒性、高时空分辨率、高信噪比等优点,结合了激光扫描共聚焦显微镜和双光子激发技术,广泛应用于脑科学、免疫学、肿瘤、胚胎发育等生物医学相关研究领域。本文结合作者所在的北京大学医药卫生分析中心共聚焦平台的工作经验,概述了[/font]TPLSM适用的样本、检测模式以及在生物医学领域的应用,以期为相关科研技术人员提供参考。[b][font=&][Abstract][/font] [/b]Two-photon laser scan microscopy (TPLSM) has the advantages of low phototoxicity, high spatial and temporal resolution, and high signal-to-noise ratio.TPLSM combines laser scanning confocal microscopy with two-photon excitationtechnology and it is widely used in brain science, immunology, tumor, embryodevelopment and other biomedical related research fields. Based on the author'swork experience in the confocal center of Peking University Medical and HealthAnalysis Center, this paper summarizes the applicable samples, detection modesand applications of TPLSM in the biomedical field, in order to provide referencefor related scientific researchers and technicians.[b][font=黑体][[/font]关键词] [/b]显微镜双光子,检测模式,应用[b]1 引言[/b]双光子激发技术的基本原理是在高光子密度情况下,荧光分子可同时吸收2个长波长光子,产生一个一半波长光子去激发荧光分子的相同效果。双光子激光扫描显微镜(two-photon laser scan microscope, TPLSM[font=宋体])在激光扫描共聚焦显微镜的基础上,以红外飞秒激光作为光源,长波长的近红外激光受散射影响小,易穿透标本,可深入组织内部非线性激发荧光,对细胞毒性小且具有高空间分辨率,适合生物样品的深层成像及活体样品的长时间观察成像[/font][1]。使用高能量锁模脉冲激光器,物镜焦点处的光子密度最高,在焦点平面上才有光漂白及光毒性,焦点外不损伤细胞。双光子效应只发生在焦点处,所以双光子显微镜无需共聚焦针孔,也能做到点激发点探测,提高了荧光检测效率[2]。[b][/b]双光子激光扫描显微镜显微镜可以通过XYZ,XYT,XYλ,XYZT,XYλT等多种模式实现多维成像,亦可进行更复杂实验的拍摄,比如二次谐波成像(Second Harmonic Generation Imaging,SHG[font=宋体])、双光子荧光寿命成像([/font]Two-photon Fluorescence Lifetime Imaging Microscopy, TP-FLIM[font=宋体])、荧光寿命[/font]-[font=宋体]荧光共振能量转移成像([/font]FluorescenceLifetime - Fluorescence Resonance Energy Transfer Imaging, FLIM-FRET[font=宋体])等实验以满足对样品的定性、定量、定位、共定位等多维度多功能的研究。[/font]TPLSM已成为生命科学各领域重要的研究工具,可在细胞及亚细胞水平对活体动物的神经细胞形态结构、离子浓度、细胞运动、分子相互作用等生理现象进行直接的长时间成像监测,还能进行光激活染及光损伤等光学操纵,广泛应用于脑科学、免疫学、肿瘤、胚胎发育等生物医学相关研究[3-5]。本文拟通过按TPLSM常见的检测模式分别阐述其在生物医学领域的应用,以其为相关科研技术人员提供参考。[b]2. TPLSM适用的样本[/b]TPLSM适用的样本非常广泛,从液体、固体等形式的材料或制剂、细菌、细胞、细胞团、类器官、组织切片、到各种模式动物(如线虫、果蝇、斑马鱼、小鼠、大鼠、兔、猴等)及其[font=宋体]脑、脊髓、肝脏、肺、皮肤等器官[/font],都可以通过搭载不同载物台进行测试。相对于传统激光扫描共聚焦显微镜200μm的成像深度极限,双光子显微镜成像深度可达800μm,如果是透明化样品可更厚。TPLSM尤其适合活体动物成像,且比小动物荧光成像有更高的分辨率和信噪比,一般TPLSM的XY轴分辨率为200 nm左右,Z轴分辨率为300 nm左右。[b]3. TPLSM的检测模式[/b]3.1 二维成像模式TPLSM可以实现点扫描、点探测,得到生物样品高反差、高分辨率、高灵敏度的二维图像,从而获得细胞/组织等光学切片的物理、生物化学特性及变化。也可以对所感兴趣的区域进行准确的定性、定量及定位分析。激光扫描显微镜的zoom功能,可以用来调节扫描区域的放大倍数。但受物镜分辨率的限制,一味的增大zoom值,不能得到相应的高清图像,需根据实际情况参考piexl size进行设定。TPLSM可以实现XY、XZ或XT的二维成像模式,XT线扫会在后文与XYT时间序列成像一起进行举例说明(图2b)。3.2 三维成像模式3.2.1 Z轴序列三维成像(XYZ)[align=left]TPLSM可沿Z轴方向通过电动载物台的连续扫描对样品进行无损伤的光学切片(XYZ),获得三维立体图像。同理,通过沿Y轴方向连续扫描,可获得连续的XZY图像。如图1所示TPLSM[font=宋体]可以顺利观察到可以观察到血管清晰形态结构:单个胚胎的胎盘微血管(图[/font]1a)、肝脏血窦微血管(图1b)和后肢微血管(图1c)[6]。[/align][align=center][img=,690,230]https://ng1.17img.cn/bbsfiles/images/2022/12/202212151626576232_4807_3237657_3.png!w690x230.jpg[/img][/align][align=center]图1(a)胚胎胎盘微(b)肝脏血窦和(c)后肢的微血管三维成像[/align]3.2.2 时间序列扫描模式(XYT)[align=left]按照一定的时间间隔重复采集,则可实现对该样品的实时监测(XYT)。此类实验可观察组织区域内特异荧光探针标记的单个细胞或细胞内不同部位接受刺激后的整个变化过程。[font=宋体]如图[/font]2[font=宋体]([/font]a[font=宋体]),可以根据微血管[/font]XYT[font=宋体]序列扫描的成像结果中某一血细胞在前后两张图的位置移动和这两帧图的扫描时间间隔计算血流速度。若血流速度很快,[/font]XYT扫描不足以捕捉实际流速,可以使用XT线扫计算。如图2(b),微血管XT扫描图像中绿色荧光背景里的黑色线条代表单个血细胞的流动轨迹,每条线条的横坐标代表血细胞移动的距离(distance / μm[font=宋体]),纵坐标代表此段时间([/font]time/ ms[font=宋体]),根据这两个数据可以计算出单位时间内血细胞的流动速度([/font]μm / ms)[6]。[/align][align=center][img=,690,262]https://ng1.17img.cn/bbsfiles/images/2022/12/202212151627102569_8367_3237657_3.png!w690x262.jpg[/img] [/align][align=center]图2 微血管(a)XYT扫描结果和(b)XT一维扫描结果图像计算血流说明示意图[/align]3.2.3 光谱扫描模式(XYλ/XYΛ)通常配置有可调节接受范围的检测器的TPLSM,可以实现从400nm-800nm的发射波谱扫描。通过配置具有连续可调波长的双光子激光器,还可以实现750nm-1300nm激发波谱扫描。这对于开发研制特殊染料探针的课题来说是很方便、全面的检测功能。3.3四维成像模式(XYZT/XYλT/XYΛT)基于上述三维成像模式,结合时间序列扫描,可以实现TPLSM的四维成像。3.4二次谐波成像(SHG)SHG是一个二阶非线性过程,且一般为非共振过程,适合富含胶原纤维的样本成像,如角膜、鼠尾肌腱、皮肤等。生物组织产生的二次谐波最主要的转换源自胶原,不同生物组织中的二次谐波信号强弱与组织中的胶原含量密切相关,含胶原丰富的组织包括结缔组织和肌肉组织等二次谐波信号也比较强,另外还有一些能产生强二次谐波的生物结构是微管,如细胞分裂中纺锤体。对于具有中心对称性的生物结构,如果局部中心对称性的破坏也会产生二次谐波:在两中心对称介质的界面,不同物态分子的相互作用使局部微观场特性在交界面(如细胞膜)发生突变,从而产生界面二次谐波[7]。除了动物组织外,一些含有特殊分子结构的植物组织也能产生二次谐波。二次谐波显微成像具有高空间分辨率、深成像深度、低损伤、以及对结构对称性的高度敏感性的特点,如果能与其他成像技术结合,将成为生物样品研究的有力工具[8]。3.5双光子荧光寿命成像(TP-FLIM)[9]FLIM技术是研究细胞内生命活动状态的一种非常可靠的方法。荧光寿命是荧光团在返回基态之前处于激发态的平均时间,是荧光团的固有性质,因此其不受探针浓度、激发光强度和光漂白效应等因素影响,且能区分荧光光谱非常接近的不同荧光团,故具有非常好的特异性和很高的灵敏度。此外,由于荧光分子的荧光寿命能十分灵敏地反映激发态分子与周围微环境的相互作用及能量转移,因此FLIM技术常被用来实现对微环境中许多生化参数的定量测量,如细胞中折射率、黏度、温度、pH值的分布和动力学变化等,这在生物医学研究中具有非常重要的意义。目前FLIM技术在细胞生物学中一些重要科学问题的研究、临床医学上一些重大疾病的诊断与治疗研究以及纳米材料的生物医学应用研究等方面均有广泛应用,并取得了许多利用传统的研究手段无法获取的数据。FLIM检测需要脉冲激光,TPLSM带有的高能量锁模脉冲激光器可以满足激发要求。3.6荧光寿命-荧光共振能量转移成像(FLIM-FRET)[10]传统的FRET过程分析通常是基于荧光强度成像来实现,分析的结果容易受光谱串扰的影响。而将FLIM技术应用于FRET过程分析,利用FLIM技术可定量测量这一优势,可非常灵敏地反映供体荧光分子与受体荧光分子之间的能量转移过程。当受体分子与供体之间的距离10nm时,供体的能量转移到受体,受体从基态发生能量跃迁,从而影响供体的荧光寿命。与没有受体分子的时候相比,发生FRET的供体分子的荧光寿命降低。因此,FRET-FLIM联合能够实时监测生物细胞中蛋白质的动态变化,如蛋白质折叠、分子间(蛋白-蛋白,蛋白-核酸)相互作用和细胞间信号分子传递、分子运输以及病理学研究等。[b]4 结论和展望[/b]综上,TPLSM应用灵活,具备多种检测模式,适用于多种样本,亦可实现多种实验目的,如荧光的定量、定性、定位、共定位,动态荧光的测定等。一些特殊的实验模式,将TPLSM在生物医学领域的应用进一步扩大。通过结合其他技术(多手段联合拓展,如膜片钳、原子力显微镜、光电联用等),TPLSM必将成为助力生物医学领域研究的有力工具。双光子荧光成像由于具有天生的三维层析能力以及深穿透能力,在活体生物组织成像上广受欢迎。双光子显微镜镜下空间增大后,可广泛应用于猴、大小鼠、兔等较大的模式动物的活体成像。且可结合电生理技术、光遗传技术,广泛应用于麻醉、清醒或运行行为等生理状态下的动物脑科学神经相关研究,在单细胞、单树突精度上对神经元群体活动进行监控。如结合膜片钳技术,对活体脑组组急性切片神经元进行双光子深层成像[11];结合光遗传技术,实现视觉皮层同一神经元和神经元群体的稳定操控和长期多次重复记录[12];对在健身球上移动的头部固定小鼠小脑进行成像,探讨觉醒状态和运动行为对胶质网络中钙离子的激发的影响[13];结合多种疾病模型,探讨大脑皮层神经元及胶质细胞活性的改变及作用等[14]。随着多种双光子显微镜系统的出现,双光子显微镜成像技术将以其实时、无损地探测、诊断及检测能力,在生物医药及临床医学应用中发挥更大作用。[b]参考文献[/b][1] [font=宋体]李娟[/font],[font=宋体]张岚岚[/font],[font=宋体]吴珏珩[/font].[font=宋体]双光子显微镜的应用优势与维护要素[/font][J].[font=宋体]中国医学装备[/font],2021,18(12):158-163.[2] HendelT,Mank M, Schnell B,et al.Fluorescence changes of genetic calcium indicatorsand OGB1correlated with neural ac tivity and calcium in vivo and in vitro[J].JNeurosci, 2008,28(29):7399-7411.[3] DolginE.What leva lamps and vinaigrette can teach us about cellbiology[J].Nature,2018,555(7696):300-302.[4] Noguchi J,Nagaoka A, Watanabe S,et al.in vivo two-photon uncaging of glutamate revealingthe structure-function relatio nships of dendritic spines in the neocortex ofadult mice[J]. J Physiol,2011,589(Pt 10):2447-2457.[5] BishopD,Nikiél, Brinkoetter M,et al.Nearinfrared branding efficiently correlateslight and electron microscopy[J]. Nat Methods,2011,8(7):568-570.[6] [font=宋体]刘皎[/font],[font=宋体]丛馨[/font],[font=宋体]何其华[/font].[font=宋体]活体小鼠微血管血流倒置双光子激光扫描显微镜检测方法的建立[/font][J].解剖学报,2022,53(02):261-265.[7] [font=宋体]屈军乐[/font],[font=宋体]陈丹妮[/font],[font=宋体]杨建军[/font],[font=宋体]许改霞[/font],[font=宋体]林子扬[/font],[font=宋体]刘立新[/font],[font=宋体]牛憨笨[/font].[font=宋体]二次谐波成像及其在生物医学中的应用[/font][J].[font=宋体]深圳大学学报[/font],2006,(01):1-9.[8] [font=宋体]孙娅楠[/font],[font=宋体]赵静[/font],[font=宋体]李超华[/font],[font=宋体]等[/font].[font=宋体]二次谐波结合双光子荧光成像方法观察人源胶原蛋白透皮吸收情况[/font][J].激光生物学报,2017,26(1):24-29.[9] [font=宋体]刘雄波,林丹樱,吴茜茜,严伟,罗腾,杨志刚,屈军乐,荧光寿命显微成像技术及应用的最新研究进展。物理学报,[/font]2018,67(17):178701-1-178701-14[10] [font=宋体]罗淋淋,牛敬敬,莫蓓莘,林丹樱,刘琳,荧光共振能量转移[/font]-荧光寿命显微成像(FRET-FLIM[font=宋体])技术在生命科学研究中的应用进展。光谱学与光谱分析,[/font]2021,41(4):1023-1031[11] Isom-BatzG,Zimmem PE.Collagen injection for female urinary incontinence after urethralor periurethral surgery[J].J Unol,2009,181(2):701-704.[12] JuN,Jiang R,Mrcknik SL,et al.Long-term all-optical interrogation of corticalneurons in awake-behaving nonhuman prim ates[J].LOSBiology,2018,16(8):e2005839.[13]Nimmerjahn A,Mukamel EA, Schnitzer MJ.Motor behavior activates Bergmann glialnetworks[J].Neuron,2009,62(3):400-412.[23] Huang L, Lafaille JJ, YangG.LearningDependent dendritic spine plasticity is impaired in spontaneousautoimmune encep halomyelitis[J].Dev Neurobiol,2021,81(5):736-745.[14] Huang L,Lafaille JJ,Yang G.LearningDependent dendritic spine plasticity is impaired inspontaneous autoimmune encep halomyelitis[J].Dev Neurobiol, 2021,81(5):736-745.
[align=center][font='times new roman'][size=16px][b]超高分辨[/b][/size][/font][font='times new roman'][size=16px][b]显微镜及其在生物医学领域的应用[/b][/size][/font][/align][align=center][font='times new roman'][size=14px]刘皎[/size][/font][font='times new roman'][sup][size=14px]1[/size][/sup][/font][font='times new roman'][size=14px],[/size][/font][font='times new roman'][sup][size=14px] [/size][/sup][/font][font='times new roman'][size=14px]吴晶[/size][/font][font='times new roman'][sup][size=14px]1[/size][/sup][/font][/align][align=center]1. [font='times new roman']北京大学医药卫生分析中心,北京,[/font][font='times new roman']100191[/font][/align][font='times new roman'][b]摘要[/b][/font][font='times new roman'][b] [/b][/font][font='times new roman']超高分辨显微镜([/font][font='times new roman']Super-Resolution Microscopy[/font][font='times new roman'])作为一类强大的科学工具,可以突破传统光学显微镜的分辨极限,实现对微小结构的高分辨率成像,已经在生物医学领域引起了广泛的关注和应用。本文将探讨超高分辨显微镜的不同类型和原理,介绍[/font][font='times new roman']其[/font][font='times new roman']在生物医学领域的应用[/font][font='times new roman']及展望其未来发展[/font][font='times new roman']。[/font][font='times new roman'][b]Abstract[/b][/font][font='times new roman']Super Resolution Microscopy[/font][font='times new roman'], as a powerful scientific tool, can break through the resolution limit of traditional optical microscopes and achieve high-resolution imaging of small structures. It has attracted widespread attention and application in the biomedical field. This article will explore the different types and principles of Super Resolution Microscopy, introduce their applications in the biomedical field, and look forward to their future development[/font][font='times new roman'].[/font][font='times new roman'][b]关键词[/b][/font][font='times new roman']超高分辨[/font][font='times new roman']显微镜,[/font][font='times new roman']成像技术[/font][font='times new roman'],应用[/font][font='times new roman'][b]1 [/b][/font][font='times new roman'][b]引言[/b][/font][font='times new roman']显微镜的产生和发展对于生命科学研究的进步有至关重要的作用[/font][font='times new roman'],它将微观世界呈现在大家面前,包括微生物的存在、组织细胞结构及生理病理活动等。显微镜技术的不断革新将成像分辨率不断提高,但相当长一段时间内光学成像无法突破一个极限值,即[/font][font='times new roman']xy[/font][font='times new roman']轴横向分辨率约[/font][font='times new roman']200nm[/font][font='times new roman'],[/font][font='times new roman']z[/font][font='times new roman']轴纵向分辨率约[/font][font='times new roman']500nm[/font][font='times new roman'],因此小于这个尺寸的生命活动和结构[/font][font='times new roman'],如病毒、亚细胞结构等,[/font][font='times new roman']是无法清楚地观察到的[/font][font='times new roman']。[/font][font='times new roman']聚焦点的光强会根据点扩散函数([/font][font='times new roman']point spread functio[/font][font='times new roman']n[/font][font='times new roman'],[/font][font='times new roman']PSF[/font][font='times new roman'])而展开[/font][font='times new roman'],[/font][font='times new roman']对于圆形孔径,[/font][font='times new roman']PSF[/font][font='times new roman']呈现为艾里斑([/font][font='times new roman']Airy disk[/font][font='times new roman'])的模式[/font][font='times new roman']。[/font][font='times new roman']激光扫描共聚焦显微镜([/font][font='times new roman']Confocal Laser Scanning Microscopy, CLSM[/font][font='times new roman'])的分辨率取决于[/font][font='times new roman']PSF[/font][font='times new roman']的大小,如果焦点很小,则每个像素[/font][font='times new roman']点[/font][font='times new roman']获取到的信息也很小,从而得到清晰锐利的图像;反之,则结果图像变得模糊。因此,[/font][font='times new roman']CLSM[/font][font='times new roman']成像的[/font][font='times new roman']主要挑战在于实现越来越小的[/font][font='times new roman']PSF[/font][font='times new roman']以获得更好的分辨率。德国物理学家恩斯特[/font][font='times new roman'][/font][font='times new roman']阿贝([/font][font='times new roman']Ernst Abbe[/font][font='times new roman'],[/font][font='times new roman']1840-1905[/font][font='times new roman']年)在[/font][font='times new roman']19[/font][font='times new roman']世纪[/font][font='times new roman']70[/font][font='times new roman']年代首次[/font][font='times new roman']提出阿贝衍射极限,即[/font][font='times new roman']由于衍射效应,[/font][font='times new roman']PSF[/font][font='times new roman']大[/font][font='times new roman']小与[/font][font='times new roman']λ/NA[/font][font='times new roman']成正比([/font][font='times new roman']d=0.61λ/NA[/font][font='times new roman']),其中[/font][font='times new roman']λ[/font][font='times new roman']是光的波长,[/font][font='times new roman']NA[/font][font='times new roman']是物镜最重要的参数[/font][font='times new roman']——[/font][font='times new roman']数值孔径[/font][font='times new roman']。由于可见光波长范围在[/font][font='times new roman']400-760nm[/font][font='times new roman']之间,[/font][font='times new roman']NA[/font][font='times new roman']值最大在[/font][font='times new roman']1.7[/font][font='times new roman']左右,所以分辨率极限在[/font][font='times new roman']200nm[/font][font='times new roman']左右。随着物理学和测量技术的进步,突破衍射极限的显微镜不断涌现,目前公认的超高分辨显微镜主要有三类,包括[/font][font='times new roman']结构照明显微镜([/font][font='times new roman']Structured Illumination Microscopy[/font][font='times new roman'],[/font][font='times new roman']SIM[/font][font='times new roman'])[/font][font='times new roman'],受激发射减耗显微镜([/font][font='times new roman']Stimulated Emission Depletion Microscopy[/font][font='times new roman'],[/font][font='times new roman']STED[/font][font='times new roman']),和[/font][font='times new roman']单分子定位显微镜。单分子定位显微镜包括光敏定位显微镜([/font][font='times new roman']Photoactivation Localization Microscopy[/font][font='times new roman'],[/font][font='times new roman']PALM[/font][font='times new roman'])和随机光学重建显微镜([/font][font='times new roman']Stochastic Optical Reconstruction Microscopy[/font][font='times new roman'],[/font][font='times new roman']STORM[/font][font='times new roman'])[/font][font='times new roman']。[/font][font='times new roman']2014[/font][font='times new roman']年三位科学家[/font][font='times new roman']史蒂芬[/font][font='times new roman'][/font][font='times new roman']霍尔([/font][font='times new roman']Stefan W. Hell[/font][font='times new roman'])[/font][font='times new roman']、埃里克[/font][font='times new roman'][/font][font='times new roman']贝兹([/font][font='times new roman']Eric Betzig[/font][font='times new roman'])和威廉[/font][font='times new roman'][/font][font='times new roman']莫纳([/font][font='times new roman']William E. Moerner[/font][font='times new roman'])因他们在超[/font][font='times new roman']高[/font][font='times new roman']分辨显微镜技术领域的贡献而获得了诺贝尔化学奖。[/font][font='times new roman'][b]2 [/b][/font][font='times new roman'][b]不同类型的超高分辨显微镜[/b][/font][font='times new roman'][b]2.1[/b][/font][font='times new roman'][b] [/b][/font][font='times new roman'][b]结构照明显微镜([/b][/font][font='times new roman'][b]Structured Illumination Microscopy[/b][/font][font='times new roman'][b],[/b][/font][font='times new roman'][b]SIM[/b][/font][font='times new roman'][b])[/b][/font][font='times new roman']SIM[/font][font='times new roman']本质是利用两束激发光在样品上进行干涉,产生明暗交替的莫尔条纹,高空间频率的莫尔条纹会放大激发条纹与样品空间频率不一致的结构,从而将样品中的高频信息整合入收集到的图像中。[/font][font='times new roman']通过投射特殊的光照明模式如格点或条纹光栅,以一定的模式照射样品,引入空间频率信息,采集多个图像并经过复杂的数据处理之后,重建高分辨率图像。由于每个图像都采用不同的结构照明模式,包含了不同的信息,合并后的图像能够展示出比传统显微镜更多的细节[/font][font='times new roman']。[/font][font='times new roman']相比于其他超高分辨成像技术,[/font][font='times new roman']SIM[/font][font='times new roman']最大的优势就是宽场[/font][font='times new roman']成像,速度快,基本可以达到实时观察。[/font][font='times new roman']SIM[/font][font='times new roman']技术的前身可以追溯到[/font][font='times new roman']20[/font][font='times new roman']世纪[/font][font='times new roman']70[/font][font='times new roman']年代初。当时,光学学家特奥多尔[/font][font='times new roman'][/font][font='times new roman']赫普恩([/font][font='times new roman']Theodor [/font][font='times new roman']H?upl[/font][font='times new roman'])首次提出了使用周期性光栅照明来提高显微镜分辨率的想法。这奠定了[/font][font='times new roman']SIM[/font][font='times new roman']技术的基础,尽管当时还没有实际的[/font][font='times new roman']SIM[/font][font='times new roman']显微镜。[/font][font='times new roman']21[/font][font='times new roman']世纪初期,史蒂芬[/font][font='times new roman'][/font][font='times new roman']霍尔([/font][font='times new roman']Stefan W. Hell[/font][font='times new roman'])和埃里克[/font][font='times new roman'][/font][font='times new roman']贝兹([/font][font='times new roman']Eric Betzig[/font][font='times new roman'])等科学家分别独立开发了[/font][font='times new roman']SIM[/font][font='times new roman']的现代版本。[/font][font='times new roman']SIM[/font][font='times new roman']技术开始广泛传播,吸引了生物学家和显微镜专家的关注。它被认为是一种相对低成本的[/font][font='times new roman']超高分辨[/font][font='times new roman']率成像方法,因为它不需要昂贵的激光设备或复杂的样品准备。[/font][font='times new roman'][b]2.2 [/b][/font][font='times new roman'][b]受激发射减耗[/b][/font][font='times new roman'][b]显微镜([/b][/font][font='times new roman'][b]Stimulated Emission Depletion Microscopy[/b][/font][font='times new roman'][b],[/b][/font][font='times new roman'][b]STED[/b][/font][font='times new roman'][b])[/b][/font][font='times new roman']STED[/font][font='times new roman']技术的概念最早由斯德哥尔摩大学的斯蒂芬[/font][font='times new roman'][/font][font='times new roman']霍尔([/font][font='times new roman']Stefan W. Hell[/font][font='times new roman'])提出。他的想法是通过将激发光束与一个特殊的抑制光束结合,从而实现对荧光标记物的光抑制,[/font][font='times new roman']通过受激辐射淬灭光斑外围的荧光分子,[/font][font='times new roman']使其在空间上变得更加紧凑,[/font][font='times new roman']减少[/font][font='times new roman']PSF[/font][font='times new roman']从而提高分辨率。[/font][font='times new roman']我们也叫“甜甜圈”技术。[/font][font='times new roman']STED[/font][font='times new roman']显微镜背后基本思想就是利用非线性光学设计一个低于阿贝衍射极限的更小[/font][font='times new roman']PSF[/font][font='times new roman']。[/font][font='times new roman']分辨率与[/font][font='times new roman']STED[/font][font='times new roman']光强有关,提高[/font][font='times new roman']STED[/font][font='times new roman']光的强度可以使荧光光斑焦[/font][font='times new roman']点中心直径趋于[/font][font='times new roman']0[/font][font='times new roman'],但是实际应用中,光损伤较大,[/font][font='times new roman']STED[/font][font='times new roman']光强不可能无限增加,顾[/font][font='times new roman']其分辨率[/font][font='times new roman']最高[/font][font='times new roman']可达到[/font][font='times new roman']3[/font][font='times new roman']0[/font][font='times new roman']nm[/font][font='times new roman']左右[/font][font='times new roman']。[/font][font='times new roman']目前的[/font][font='times new roman']STED[/font][font='times new roman']只能应用于较薄的组织器官或细胞,光毒性较强,成像厚度有限不太适合活体或活细胞长时间成像。[/font][font='times new roman']STED[/font][font='times new roman']光路较为复杂,对系统稳定性要求较高。[/font][font='times new roman'][b]2.3 [/b][/font][font='times new roman'][b]单分子定位显微镜[/b][/font][font='times new roman']单分子定位显微镜[/font][font='times new roman']中荧光标记的单个分子被分别激发和检测。单分子的中心可以以极高的精度确定从而实现高分辨率,包括光敏定位显微镜([/font][font='times new roman']Photoactivation Localization Microscopy[/font][font='times new roman'],[/font][font='times new roman']PALM[/font][font='times new roman'])和随机光学重建显微镜([/font][font='times new roman']Stochastic Optical Reconstruction Microscopy[/font][font='times new roman'],[/font][font='times new roman']STORM[/font][font='times new roman'])。[/font][font='times new roman']PALM[/font][font='times new roman']的历史可以追溯到[/font][font='times new roman']2006[/font][font='times new roman']年,由埃里克[/font][font='times new roman'][/font][font='times new roman']贝兹([/font][font='times new roman']Eric Betzig[/font][font='times new roman'])和哈拉尔德[/font][font='times new roman'][/font][font='times new roman']赫斯([/font][font='times new roman']Harald Hess[/font][font='times new roman'])提出了单分子定位这一概念。在[/font][font='times new roman']PALM[/font][font='times new roman']中,样品中的分子被标记上特定的荧光染料。这些染料可以通过光激活从一个基态转变到一个激发态,此过程可通过使用激活光(通常是紫外光)来实现。同期[/font][font='times new roman']STORM[/font][font='times new roman']的成像技术也发展起来,代表科学家是华人庄小威。[/font][font='times new roman']STORM[/font][font='times new roman']的工作原理与[/font][font='times new roman']PALM[/font][font='times new roman']类似,是通过特殊的分子标记和随机活性化,实现单分子定位进而实现超高分辨率成像。具有光激活能力的标记物通常在某种光照条件下会发光,但也会在某一时刻被随机地熄灭。这种随机光熄灭是[/font][font='times new roman']PALM[/font][font='times new roman']技术的关键,因为它允许在不同时间点捕获标记物的位置。通过记录标记物的位置,可以得到它们的坐标。这一过程需要在短时间内多次拍摄样品,以获得足够多的数据点。最后,通过将多个标记物的坐标叠加在一起,可以生成高分辨率的图像。这种以成像时间换取空间分辨率的形式,使得[/font][font='times new roman']PALM[/font][font='times new roman']或[/font][font='times new roman']STORM[/font][font='times new roman']的分辨率通常能够达到数十纳米。[/font][font='times new roman'][b]3 [/b][/font][font='times new roman'][b]应用领域和未来发展[/b][/font][font='times new roman']超高分辨显微镜可以探索微观世界的无限可能性,已经彻底改变了科学研究的方式。在细胞生物学领域,它被用于研究[/font][font='times new roman']亚细胞结构,如微丝、微管、肌动蛋白等,[/font][font='times new roman']细胞器[/font][font='times new roman']如线粒体、溶酶体等,[/font][font='times new roman']分子分布和细胞膜动态、观察蛋白质的相互作用;在神经科学领域,它可用于观察神经元的亚细胞结构和突触的细节,有助于解剖和理解神经系统的结构和功能,以及神经系统相关疾病的机制;在癌症研究领域,被用于研究癌细胞的特征、蛋白质分布以及肿瘤微环境,这对于癌症的早期诊断和治疗规划非常重要;在材料科学领域,它被用于研究纳米材料的结构和性质、帮助科学家精确控制和制备纳米结构;在药物研发领域,它可用于研究药物靶标蛋白的定位和与其他分子的相互作用,这对于药物设计和筛选非常重要[/font][font='times new roman'];在微生物领域,对于研究细菌[/font][font='times new roman']结构变化至关重要,规避了电子显微镜无法进行活体成像等弊端,可以更加推进微生物学发展。[/font][font='times new roman']当然,[/font][font='times new roman']超[/font][font='times new roman']高[/font][font='times new roman']分辨成像技术[/font][font='times new roman']也有一定的挑战。超高分辨成像技术[/font][font='times new roman']通常需要高度复杂的设备和精密的校准,这使得其设备成本相对较高,[/font][font='times new roman']再加上样本制备的困难,[/font][font='times new roman']限制了其广泛应用。[/font][font='times new roman']样品准备在超高分辨成像中具有重要作用,新的标记技术和荧光探针的发展将提高成像的灵敏度和特异性[/font][font='times new roman'],[/font][font='times new roman']开发更友好、无损伤的样品准备方法,以减少对样品的干扰[/font][font='times new roman'],[/font][font='times new roman']甚至[/font][font='times new roman']包括无标记成像技术以减少样品标记的需求。开源软件和自动化工作流程将使超高分辨成像技术更易于使用和共享,促进科学研究的进展。[/font][font='times new roman']超高分辨技术通常对于三维成像和大样本的深度成像有限制,需要克服分辨率和深度之间的权衡。[/font][font='times new roman']同时超高分辨[/font][font='times new roman']成像的时间分辨率还可以继续提升[/font][font='times new roman']。[/font][font='times new roman']虽然[/font][font='times new roman']目前[/font][font='times new roman']SIM[/font][font='times new roman']和[/font][font='times new roman']minflux[/font][font='times new roman']更适合[/font][font='times new roman']观察[/font][font='times new roman']活细胞[/font][font='times new roman']动态过程,但时间分辨率的提高仍然是一个挑战,特别是对于极短时间尺度的现象[/font][font='times new roman'],[/font][font='times new roman']这将使科学家能够更深入地探索微观世界,并获得更多信息。[/font][font='times new roman']随着技术的不断进步,[/font][font='times new roman']超高分辨[/font][font='times new roman']成像有望在[/font][font='times new roman']包括临床医学[/font][font='times new roman']等[/font][font='times new roman']更多领域得到广泛应用[/font][font='times new roman'],未[/font][font='times new roman']来如果能实现超高分辨的动物甚至人的[/font][font='times new roman']活体成像,减少样品固定和处理的需求,允许观察生物过程的实时发生[/font][font='times new roman']将会更有现实意义[/font][font='times new roman']。[/font][font='times new roman']并且在科学研究的需求下,[/font][font='times new roman']多模态[/font][font='times new roman']或多尺度[/font][font='times new roman']成像将[/font][font='times new roman']与[/font][font='times new roman']不同[/font][font='times new roman']的[/font][font='times new roman']超高分辨[/font][font='times new roman']技术相结合,[/font][font='times new roman']例如,结合光学成像和质谱成像[/font][font='times new roman'],[/font][font='times new roman']从分子水平到组织水平[/font][font='times new roman']提供[/font][font='times new roman']生命活动[/font][font='times new roman']更全面的信息。[/font][font='times new roman']也可以[/font][font='times new roman']发展高通量的样品处理和成像技术,以便更快速地获得大规模的数据。[/font][font='times new roman']超高分辨[/font][font='times new roman']成像生成的数据量巨大,处理和分析这些大数据需要强大的计算资源和高效的算法。数据存储和传输也是挑战。[/font][font='times new roman']超高分辨[/font][font='times new roman']成像数据可能受到噪声和伪迹的影响,这需要高级的图像处理技术来减少其影响,以获得准确的图像。数据分析通常需要复杂的算法和数学模型,需要专业知识和技能。对于某些应用,如神经科学中的活体成像,需要实时数据分析,这增加了挑战。深度学习和人工智能技术[/font][font='times new roman']有望[/font][font='times new roman']在数据分析中发挥越来越重要的作用,[/font][font='times new roman']实现[/font][font='times new roman']自动处理和解释图像数据。发展实时数据分析技术,使科学家能够在数据采集过程中获得及时反馈。开发更易用的高级图像处理工具,使非专业用户也能够进行数据分析。结合不同成像技术和数据源的信息,以提供更全面的信息。开发自动化和高通量的数据分析工作流程,以应对大规模数据的挑战。促进数据共享和开放科学,以促进合作和加速科学研究的进展。未来,随着计算能力的提高和新技术的引入,[/font][font='times new roman']超高分辨[/font][font='times new roman']成像数据分析将变得更加强大和高效。这将有助于更深入地理解微观世界,并在生物学、医学、材料科学等领域推动创新和发展。[/font][font='times new roman']总的来说,尽管[/font][font='times new roman']超高分辨[/font][font='times new roman']成像面临一些挑战,但其前景充满希望。未来的发展将使这一领域更加强大,有望在科学研究和实际应用中提供更多的机会和洞察力。[/font][font='times new roman'][b]4 [/b][/font][font='times new roman'][b]结论和展望[/b][/font][font='times new roman']超高分辨显微镜的成像原理基于破解传统显微镜的分辨极限,通过结构照明、图像重建[/font][font='times new roman']和单分子成像等策略,实现对微小结构的高分辨率成像。这一技术的应用领域包括生物学、材料科学、纳米技术和医学等,有望推动科学研究的进一步发展。超高分辨显微镜已经在生物医学领域取得了显著的突破,使研究人员更深入地理解细胞和分子结构。然而,仍然存在挑战,包括样品准备和数据分析的复杂性。未来,我们可以期待更多技术的发展,以进一步提高分辨率和扩大应用领域。[/font][font='times new roman']随着技术的不断发展,我们可以期待更多超分辨显微镜技术的突破,如更高分辨率、更高灵敏度和更快成像速度。超分辨显微镜的应用也将继续扩展到新的领域,如药物研发、个性化医学和环境科学。它将为我们提供更多工具来解决生物学的重要问题,如疾病机制、药物研发和生态系统健康。总之,超分辨显微镜技术的未来展望是光明的,它将继续推动科学研究向前迈进,揭示微观世界的微小奥秘,为改善生活质量和解决全球挑战做出贡献。这个领域的不断创新将激发更多科学家的热情,共同追求更深入的科学知识和更广泛的应用。[/font][font='times new roman'][b]参考文献[/b][/font][font='times new roman']Hell[/font][font='times new roman'] [/font][font='times new roman']S [/font][font='times new roman']W[/font][font='times new roman'].[/font][font='times new roman']Far-field[/font][font='times new roman'] [/font][font='times new roman']optical[/font][font='times new roman'] [/font][font='times new roman']nanoscopy[/font][font='times new roman'][J][/font][font='times new roman'].[/font][font='times new roman']Science[/font][font='times new roman'],[/font][font='times new roman']2007[/font][font='times new roman'],[/font][font='times new roman']316(5828)[/font][font='times new roman']:[/font][font='times new roman']1153-1158[/font][font='times new roman']Hell[/font][font='times new roman'] [/font][font='times new roman']S W[/font][font='times new roman'],[/font][font='times new roman']Wichmann J[/font][font='times new roman'].[/font][font='times new roman']Breaking[/font][font='times new roman'] [/font][font='times new roman']the diffraction[/font][font='times new roman'] [/font][font='times new roman']resolution[/font][font='times new roman'] [/font][font='times new roman']limit[/font][font='times new roman'] [/font][font='times new roman']by stimulated[/font][font='times new roman']-[/font][font='times new roman']emission[/font][font='times new roman']-[/font][font='times new roman']depletion fluorescence[/font][font='times new roman'] [/font][font='times new roman']microscopy[J][/font][font='times new roman'].[/font][font='times new roman']Optics[/font][font='times new roman'] [/font][font='times new roman']Letters[/font][font='times new roman'],[/font][font='times new roman']1994[/font][font='times new roman'],[/font][font='times new roman']19(11)[/font][font='times new roman']:[/font][font='times new roman']780-782[/font][font='times new roman']Dani A[/font][font='times new roman'],[/font][font='times new roman']Huang B[/font][font='times new roman'],[/font][font='times new roman']Bergan J[/font][font='times new roman'],[/font][font='times new roman']et[/font][font='times new roman'] [/font][font='times new roman']a1[/font][font='times new roman'].[/font][font='times new roman'] Super-resolution[/font][font='times new roman'] [/font][font='times new roman']imaging of chemical synapses[/font][font='times new roman'] [/font][font='times new roman']in the brain[J][/font][font='times new roman'].[/font][font='times new roman']Neuron[/font][font='times new roman'],[/font][font='times new roman']2010[/font][font='times new roman'],[/font][font='times new roman']68(5)[/font][font='times new roman']:[/font][font='times new roman']843[/font][font='times new roman']—[/font][font='times new roman']856[/font][font='times new roman']PATTERSON[/font][font='times new roman'] [/font][font='times new roman']G[/font][font='times new roman'],[/font][font='times new roman']DAVIDSON[/font][font='times new roman'] [/font][font='times new roman']M[/font][font='times new roman'],[/font][font='times new roman']MANLEY[/font][font='times new roman'] [/font][font='times new roman']S[/font][font='times new roman'],[/font][font='times new roman']et[/font][font='times new roman'] [/font][font='times new roman']al[/font][font='times new roman']. [/font][font='times new roman']Superresolution[/font][font='times new roman'] imaging using single-molecule localization[/font][font='times new roman'][J][/font][font='times new roman'].[/font][font='times new roman']A[/font][font='times new roman']nnual Review of Chemistry[/font][font='times new roman'],[/font][font='times new roman']2010[/font][font='times new roman'],[/font][font='times new roman']6[/font][font='times new roman']1:345-367[/font]
请提供书名及购买地址,此书详细讲述低温电镜技术在生物医学应用的教科书,包括样品制备技术,试验操作技术, 设备维修和维护技术。以下是参考书单,不知哪本合适。1.《生物显微镜原理与维修 》--------[罗必胜编著. ] [1997 ] 2.《生物医学电子显微镜技术 》--------[程时,彭学敏主编. ] [1997 ] 3.《生物电子显微镜观察与分析 》--------[陈柏林主编. ] [1997 ] (点击:210次) 4.《生物电子显微镜实验技术 》--------[曹汉民编著. ] [] (点击:61次) 5.《生物医学超微结构与电子显微镜技术 》--------[洪涛主编. ] [1980 ] (点击:49次) 6.《电子显微镜生物标本制备技术 》--------[黄立编. ] [1982 ] (点击:136次) 7.《生物学中的电子显微镜技术 》--------[朱丽霞等编著. ] [1983 ] (点击:57次) 7.《医学生物学电子显微镜图谱 》--------[中国医学科学院主编. ] [1978 ] (点击:59次)很感谢