方案详情文
智能文字提取功能测试中
Metallurgical Analysis,2012,32(2):46-50 陶玲,孙焕,龚雁,等.温度滴定法测定铝材表面处理废水中总酸度和铝离子浓度.冶金分析,2012,32(2):46-50 温度滴定法测定铝材表面处理废水中总酸度和铝离子浓度 陶 玲,孙 焕,龚 雁,李 涛* (瑞士万通中国有限公司中心实验室,北京100005) 摘 要:铝材表面通常采取一些化学方法处理如酸处理以达到提高材料的防护性和功能性、扩大应用范围和延长使用寿命。铝材表面处理后所产生的废水中含有较高浓度的 H+和Al+,对二者含量进行有效监控,无论是在生产监控方面还是环境保护方面都具有很大意义。本文首次应用温度滴定方法对水溶液中的H+和Al3+进行定量检测,并将该方法应用到铝厂实际废水的检测中。结果表明,此方法的测定值与理论值或常规的手动滴定法的测定值相符。方法的加标回收率:H+和Al+分别为99.8%和104.1%。精密度试验中 H+和Al+测定结果的相对标准偏差(RSD,n=7)均小于2%。 关键词:温度滴定;废水;总酸度;铝离子;反应焓 中图分类号:O655.29 文献标识码:A 纯铝质地较软,耐磨性较差并且容易受到腐蚀,因此通常会对其表面进行处理以达到提高防护性和功能性,扩大应用范围,延长使用寿命的目的L1-3」。目前,常用的铝材表面处理方法有电化学方法,化学方法和热喷涂方法等L4-5],而这些方法无一例外的都需要使用大量混酸溶液(盐酸和硫酸)作为介质。因此,铝材表面处理所产生废水中的主要物质为 H+和Al+。对二者含量进行准确测定是制定废水处理标准和处理方案的先决条件L6-8」;另一方面,对酸液中 H+和Al3+浓度的监控也是调整表面处理工艺,评估表面处理效果的有效途径之一。所以,选择有效、便捷的测定方法具有重要意义。 现有的针对酸性铝溶液中H+和Al+的测定方法是平行取样、分别用传统的手工滴定方法。即取2份样品,其中1份样品直接用碱滴定,得到H+和Al3+共同消耗滴定剂的体积;另一份样品用 NaF 掩蔽 Al+后用碱滴定,得到对应总酸消耗滴定剂的体积,两者之差即可算出A1+浓度。然而,在实际操作中,该方法存在着种种问题。首 先,采用平行取样的方式,在取样过程中产生的误差会影响准确性和平行性。同时,以指示剂变色来作为终点判别依据,主观性较大,其结果的准确性与平行性也会受到较大影响。最后,该方法操作繁琐,难以自动化,效率较低。 本文首次采用一种全新的滴定方法 一油温度滴定法对酸性含铝溶液中的H+和Al+的含量同时进行了定量分析,并应用建立起来的分析方法对铝厂废水中的H+和AB+的含量进行了测定。实验结果显示,应用温度滴定方法通过一次取样在同一滴定杯中即可先后测定酸性含铝溶液中的H+和Al+含量,方法具有较高的准确性、分辨率及稳定性,同时操作便捷,可实现全自动操作,为铝材酸蚀废水重要指标 H+和Al+浓度的测定开辟了一条新途径。 实验部分 1.1 实验原理 温度滴定是一种应用得相对较少的滴定分析方法。众所周知,在任何化学反应中,反应焓、自 ( 作者简介:陶 玲(1983一),女,硕士研究生,主要研究方向为分析化学与催化剂制备 ) ( 通讯联系人:李 涛;Email: bj. lit@ metrohm. com. cn ) 由能和熵变是描述反应的3个相关参数:AH=AG'+TAS。电位滴定依赖于化学反应中自由能的变化。在任何反应中,焓变量越大,其基于温度变化的滴定曲线的偏转就越大。在实际滴定操作中,滴定剂以已知的固定速率加入到滴定杯中并与待测物质发生反应,反应放出(或吸收)的热量将导致整个反应体系发生温度变化,这种温度变化通过置入滴定杯中的高灵敏温度探头进行测定。仪器将对温度-体积(滴定剂)曲线进行二阶求导,并通过最终得到的二阶导数-体积(滴定剂)曲线上的出峰位置来进行滴定终点的识别。正是由于温度滴定在本质上与传统滴定的差异,使得温度滴定方法在进行物质测定,特别是复杂体系物质测定的时候,具有更高的准确度与灵敏度。由于温度探头的分辨率可以达到10-5K,这样的分辨率较肉眼观察指示剂变色的方法大大减小了误差和主观性因素的影响,从而提高测定的准确度和重现性。 待测溶液是混酸基质,其中含有一定量的Al3+。检测过程首先是氢氧化钠和酸的反应,加入离子缓冲剂后,使体系维持在 pH4~6之间,并且在有过量的钾离子存在的条件下,Al+含量可以被氟离子定量滴定,反应产物为 NaK, AlF6(见下面的化学反应方程式)。这两涉反应放热明显,温度变化较大,互不干扰,尤其是第二步反应利用温度变化的曲线将更有利于准确寻找反应终点。 与传统滴定不同,温度滴定所需要的温度信息其传送和处理都存在一定的时间延迟,由于滴定过程为恒速滴定过程,因此这样的时间延迟,可以表示为一定体积的滴定剂,即温度滴定方法的空白值。方法空白的测量是用不同浓度的被测物在先前优化好的条件下进行滴定,将被测物浓度与滴定剂消耗的等当点作图。方法的空白值,即为用所测的滴定数据作线性回归的y轴截距。改变方法的参数就要求重新作方法的空白值。因此本文中标定 NaOH 和用 NaOH 滴定总酸度均需做校准曲线,而标定 NaF 所作的校准曲线可以直接应用于之后的A13+测定。 1.2 仪器 Metrohm 温度滴定仪(瑞士万通公司):带耐氟温度探头; Dosino 加液驱动器:10 mL; Elga 超纯水仪(英国Elga 公司)。 1.3 试剂 硫酸(mos级,北京化学试剂研究所);盐酸(mos 级,北京化学试剂研究所);结晶氯化铝(AlCl3·6HzO,北京化学试剂公司);邻苯二甲酸氢钾(基准级,北京化工厂);NaF、NaOH、无水乙酸钠(国药集团化学试剂有限公司);氯化钾(优级纯,国药集团化学试剂有限公司);冰醋酸(天津市光复科技发展有限公司);铝屑(国药集团化学试剂北京有限公司);酸处理废水(某公司送样);NaOH 溶液:2 mol/L,称取 40 g NaOH固体,溶解于水中并用水稀释至500 mL,标定后待用;NaF 溶液:1 mol/L,称取 21 g NaF 固体,溶解于水中并用水稀释至500mL,标定后待用;离子缓冲液:将164g无水醋酸钠和75g氯化钾溶于700 mL纯水中,再加入115 mL冰醋酸,用纯水定容到1L;Al+标准储备溶液:0.4 mol/L,将铝屑(纯度为99.99%)的表面去油污,洗净并干燥,然后称取 10.8 g(0.4 mol)的铝屑于烧杯中,加入500 mL 200 g/L NaOH溶液溶解,将溶液移入1L 容量瓶中,用水定容;Al+标准工作溶液:0.04mol/L,用移液管吸取 50 mL Al+标准储备溶液于500mL容量瓶中,加入1mLHCl 出现A1(OH)s沉淀,再继续滴加入 HCl直至沉淀完全溶解,冷却后用纯水定容。 模拟样品 SH-1:取 4.165 mL HCl 和8.335mL HzSO,用纯水定容到50 mL;模拟样品 SM-1:精确称取5.22 g的 AlCl. 6H2O,用25mL纯水溶解,再加入4. 165 mL HCl 和8.335 mLH,SO4,用纯水定容到50mL;模拟样品 SH-2:取3.125 mL HCl 和 6. 25 mL HSO,用纯水定容到50 mL;模拟样品 SM-2:精确称取 5.22 g的AlClg. 6H2O,用25 mL纯水溶解,加入3.125mL HCl 和 6. 25 mL HSO,用纯水定容到50mL;模拟样品 SAl-1:精确称取 5.22 g AlCl.6HzO,用纯冰定容到50mL。 上述试剂除注明纯度外均为分析纯,实验用水均为超纯水(电阻>18.2MQ)。 1.4 实验方法 1.4.1 标定 1.4.1.1 NaOH 的标定 将邻苯二甲酸氢钾在105℃下烘2h,放在干燥器中冷却备用。精确称取1.2、1.6、2.0、2.4和2.8g邻苯二甲酸氢钾, 加入约 25 mL蒸馏水,依次用2 mol/L NaOH 溶液滴定,记录终点体积。以称样量为横坐标,消耗NaOH溶液的体积为纵坐标,作一校准曲线。NaOH 溶液的浓度为这条曲线斜率的倒数(反应方程式中OH-的系数为1)。 1.4.1.2 NaF 的标定 分别取 5、8、10、15、20mL 铝标准工作溶液(0.04mol/L),加入10 mL离子缓冲液后用一定量的纯水定容至30mL,得到的各溶液分别用1 mol/L NaF 溶液滴定至终点出现。以加入Al+的摩尔数为横坐标,消耗NaF溶液体积值为纵坐标,作一条校准曲线。NaF 溶液的浓度为这条曲线斜率倒数的6倍(反应方程式中F-的系数为6)。 1.4.2 分析步骤 1.4.2.1 模拟样 SH-1、SH-2 的分析 精确量取0.6、0.8、1、1.2、1.4mL 的 SH-1和SH-2,加入约 25 mL蒸馏水,依次用标定后的 NaOH 溶液滴定,记录终点体积。以取样体积为横坐标,消耗NaOH 溶液的体积为纵坐标,作一条校准曲线求出方法的空白值。按计算公式求出总酸度。 1.4.2.2 模拟样 SAl -1的分析 精确量取1mL的 SAl-1样品溶液,加入10 mL 离子缓冲液后用一定量的纯水定容至30 mL,用标定后的 NaF溶液滴定至终点出现。按计算公式求出A1+浓度。 1.4.2.3 模拟样 SM -1、SM-2和实际样品的分析 首先将不同体积的样品溶液加入滴定杯中,并用去离子水定容至40 mL。加液完成后用标定后的 NaOH 溶液滴定,出现滴定终点后立即停止。此时滴定终点指示的 NaOH 溶液消耗量用于计算溶液中的 H+。随后,仍在这个滴定杯中加入10 mL离子缓冲液,搅拌均匀,用标定后的NaF溶液滴定,出现滴定终点后停止(终点时会出现大量白色沉淀)。此时滴定终点指示的NaF溶液消耗量用于计算溶液中的A13+浓度。 1.5 计算 式中:KNaOH和KNaF分别为标定 NaOH时曲线的斜率和标定 NaF 时曲线的斜率;VNaOH 和VNaF分别为到达滴定终点时消耗滴定剂的体积;V blank 为不同方法对应的空白值; CNaOH 和 cNaF分别为标定后滴定剂的浓度;Vsample代表进样量。 2 结果与讨论 2.1 过滤系数的确定 曲线的平滑程度可通过过滤系数这个算法函数来调整。过滤系数越大,曲线越平滑;但过滤系数如果太大,也会导致等当点判断不准确。想得到准确的等当点就必须优化过滤系数,使等当点漂移最小,通常选择能使等当点体积稳定的过滤系数。不同的方法其过滤系数可能也不同。 为了考查 NaOH标定试验中过滤系数与等当点时消耗滴定剂体积之间的关系,选定过滤系数为20、30、40、50、60、70、80和90,则得到等当点时滴定剂消耗体积,如图1所示。从图1可以看出,当过滤系数为30~50时滴定剂在等当点的消耗体积最稳定,因此选择过滤系数为50。其他实验过滤系数的选择与上述相似。 图1 过滤系数的优化 Fig. 1 Optimization of filter factor 2.2 滴定曲线 温度滴定曲线又称为热谱图,它是在滴定反应过程中,以滴定剂的加入体积(V)为横坐标,以反应体系的温度(T)为Y轴纵坐标,以温度变化的二阶导数(ERC)为Y轴纵坐标绘制的 V-T-ERC 曲线。以 NaF 滴定 A1+为例,由图2可以看出,该反应为放热反应,当持续加入NaF 滴定剂到待测物中,体系的温度逐渐升高,当滴定到等当点EP1时,反应体系的温度变化趋于平缓,获得尖锐而对称的二阶导数峰,此峰值对应的就是终点体积。 2.3 空白值的确定 确定过滤系数后,按照上述试验方法的步骤操作,可以得到 NaOH标定的校准曲线和NaF滴定 Al+的校准曲线。NaOH 标定的校准曲线的线性方程为y=0.518x+0.019,R²=1,CNaOH=1/0.518=1.93mol/L,空白值为y轴截距0.0192 图2NaF 滴定 AI+曲线图 Fig.2The curve of titration of Al+ with NaF1.温度随加入滴定剂体积的变化曲线; 2.温度的变化率,即1线的二阶导数。 mL;同理,NaF 滴定Al+的校准曲线线性方程为y=5.209x+0.045,R²=0.999,由于1 mol A1+和6molF反应,所以 CNaF =6/5.2094=1.15mol/L,空白值为y轴截距0.045 7mL。其他实验空白值的确定与此类似。 2.44精密度试验 配制与模拟样品 SM-1浓度相同的7份样品,连续滴定总酸度和Al+浓度,其总酸度平均值为7.28 mol/L,RSD=1.4%;A1+浓度平均值 为 0.49mol/L,RSD=1.9%。结果表明该方法精密度很好,RSD 均在2%以内。 2.5 加标回收率 对模拟样品 SM-1进行了加标回收实验,结果如表1显示,H+和Al+的平均加标回收率分别为99.8%和104.1%。 表1 SM-1中 H+和 AI+回收试验结果 Table1 Recovery test results for H+ and Al+ 离子 原含量 加标量 回收量 回收率 Original Added Recovered Recovery Ion /(mmol/L) /(mmol/L) /(mmol/L) /% 7.26 7.89 7.87 99.7 H+ 7.986 8.679 8.664 99.8 8.712 9.468 9.448 99.8 0.494 0.478 0.498 104.2 A13+ 0.543 0.526 0.546 103.8 0.593 0.574 0.598 104.2 3样品分析 用本法对 SM-1,SM-2模拟样品和某铝厂废水的总酸度和A1+的浓度进行测定,结果如表2所示。 Table 2 Measurement results of total acid and concentration of Al in samples 样品 离子 理论值 测定值 平均值 相对标准偏差 Theoretical value Found Mean RSD Sample Ion /(mol/L) /(mol/L) /(mol/L) /% SM-1 H+ 7.23 7.31,7.24,7.24,7.27,7.27 7.26 0.39 A13+ 0.48 0.49,0.50,0.49 0.49 0.63 SM-2 H+ 5.5 5.42,5.40,5.43,5.47,5.44 5.43 0.50 A13+ 0.48 0.47,0.47,0.47 0.47 0.19 废水1 H+ 7.31* 7.686,7.646,7.673 7.668 0.22 Wastewater 1 A13+ 0.33* 0.303,0.304,0.302 0.303 0.67 废水2 H+ 7.39* 7.367,7.433,7.313 7.371 0.23 Wastewater 2 A13+ 0.5* 0.508,0.512,0.514 0.512 0.46 从表2可以看出,对于两个自配的模拟样SM-1和 SM-2,总酸度和A13+浓度的测定结果和理论值符合, RSD 均在1%以内;对于某铝厂的废水样,总酸度和A13+浓度的测定结果与常规的手工滴定法的测定结果相符。这进一步证明了本方法可以应用在实际样品测定中。 ( 参考文献: ) ( [ 1]吴敏,孙勇.铝及其合金表面处理的研究现状[J ] . 表面技术(Surface Technology), 2003, 32(3):13- 15. ) ( [ 2」Zhou W Q, Shan D, Han E H, et al. Structure and formation mechanism of phosphate conversion coatingon diecast AZ91D magnesium alloy [ J ] . Corrosion Science, 2008,50(2):329 - 337. ) ( [3] Watkims K G, Liu Z, Memahon M, et al. Influ-ence of the over lapped area on t he corrosion behav-iour of laser treated aluminum alloy [ J]. Materials Science and Engineering, 1998,A252:292-300. ) ( [4]张高会,黄国青,徐鹏,等.铝及铝合金表面处理研究进展[J].中国计量学院学报(Journal of China Jil- iang University), 2010, 21(2):174-178. ) ( [5]黄娜莎,倪益华,杨将新,等.铝合金表面改性技术的研究与进展[J].轻工机械(Light Industry Machin- ery), 2010, 28(4):4-11. ) ( [6]刘宏,向寓华,刘碧雄.铝型材表面处理废水治理的 ) ( 工艺条件探索 [ J ] .电镀与涂饰(Electroplating and Finishing), 2008,27(9):34-36. ) ( [ 7]唐海峰,唐基禄,李迅.铝合金表面处理的废水治理 [J].电镀与涂饰(Plating & Finishing), 2005, 27 (2):46-48. ) ( [ 8]朱祖芳.建筑铝型材的表面处理技术现状及发展趋 势 [ J ] .电镀与涂饰(Electroplating and Finishing), 2005,24(4):14-17. ) Determination of total acidity and aluminum ionconcentration in wastewater of aluminum profilesurface treatment by thermometric titration TAO Ling, SUN Huan, GONG Yan, LI Tao* (Metrohm China Ltd. , CCLab, Beijing 100005,China) Abstract: The aluminum profile surface was usually treated by some chemical methods such as acidtreatment to improve the protective property and functionality, enlarge the application range and prolong the use life. The wastewater generated in aluminum profile surface treatment contained high-con-centration H+and A13+Therefore, the effective monitoring of their content had important signifi-cance whether in process control or environmental protection. In this study, the content of H+andAl+ in wastewater was quantitatively determined by thermometric titration in first time. This methodwas applied to the determination of actual wastewater from aluminum factory. The results showedthat the found results of this method were consistent with the theoretical values or those obtained byconventional manual titration. The recoveries of method were 99.8% and 104.1% for H and Al+,respectively. The relative standard deviations (RSD, n=7) in precision test were both less than 2 %for H+ and A13+. Key words: thermometric titration; wastewater; total acidity; aluminum ion; reaction enthalpy
关闭-
1/5

-
2/5

还剩3页未读,是否继续阅读?
继续免费阅读全文产品配置单
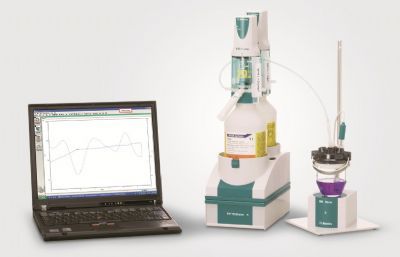
瑞士万通中国有限公司为您提供《废水中(类)金属及其化合物检测方案 》,该方案主要用于废水中(类)金属及其化合物检测,参考标准《暂无》,《废水中(类)金属及其化合物检测方案 》用到的仪器有859 Tiamo 温度滴定系统、瑞士万通859 温度滴定仪。
我要纠错
推荐专场
其它电化学仪
更多相关方案








 咨询
咨询




