

基于密度泛函理论研究四环素的电喷雾质谱裂解机理
摘要: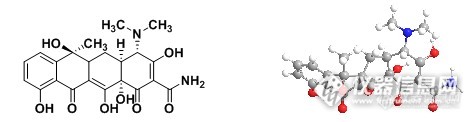
图1 Tetracycline结构及其空间立体构型
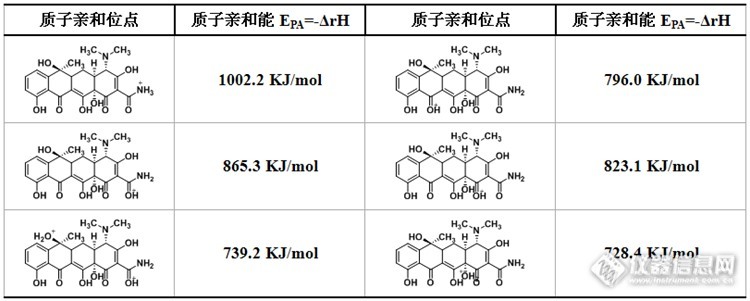
表1 四环素各质子结合位点的质子亲和能EPA
Tabel 1 Protonaffinity for proton binding sites of Tetracycline(EPA)
通过表1可以看出质子结合位点位于氨基上具有较高的质子亲和能,表明N上孤对电子可能占据HOMO轨道,所以质子化位点极可能位于氨基上。
2.2 四环素在LC-ESI-Q-Orbitrap-MS下的质谱裂解途分析
通过以上计算,以质子化位点位于氨基上为起点,并结合高分辨率质谱数据对其质谱裂解途径和机理进行分析,使用(LC-Q-Orbitrap-MS)获得准分子离子峰m/z 445.1594的二级谱,质谱碎片离子及相对丰度见表2
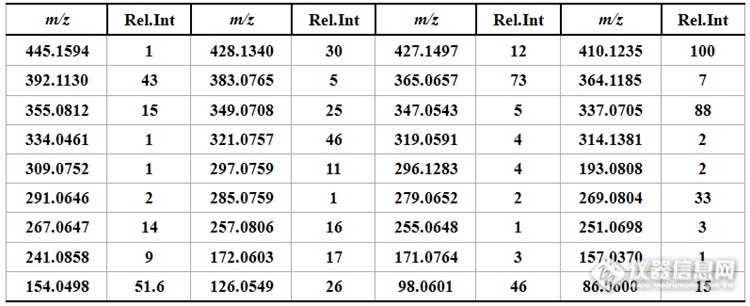
表2 四环素电喷雾离子源下准分子离子(MS2)的碎片离子及其相对丰度
Tabel 2 Relative abundancesof characteristic ions in the ESI(MS2) mass spectra of Tetracycline
依据表1计算结果,对比质子亲和能,质子最可能的结合位点为氨基上氮原子,氮原子的一对未成键电子最可能占据HOMO轨道,所以以质子结合到氨基上所形成的准分子离子峰为起始点(备注:只是最可能概率最大的,但是不排除其他小概率的质子结合位点所引发的裂解),对其可能的质谱裂解途径做以下分析。准分子离子峰失去H2O中性分子后得到碎片离子m/z427.1500,与理论误差为-2.61ppm。而失去H2O中性分子可能有多个不同位点,1.2-消除脱水和-2.4消除脱水,从空间立体构型中可以看到氢和羟基均位于一侧,所以有利于发生1.2-消除和2.4-消除,如此就有了三种可能的脱水方式,所以通过计算得到不同三种方式下脱水后生成离子的稳定构型及其能量,见表3。由表3可以看出第一种模式下生成的离子能量最低,表明此方式为主要途径,更容易进行。准分子离子通过正电荷转移失去NH3可以生成离子m/z 428.1340,与理论误差为0.02ppm,β为的氢重排到侧链氮原子上可以脱去侧链CH3NHCH3得到碎片离子m/z 383.0761,与理论值误差为1.01ppm。该离子进一步通过1.2-消除脱H2O后生成离子m/z 365.0656,与理论值误差为0.19ppm。后通过2.4-消除脱水生成离子m/z 347.0550,与理论值误差为-1.91ppm。,由于2.4-消除相比1.2-消除难所以生成的离子丰度相对较低,离子m/z 383.0761失去多个CO生成离子m/z 297.0757,进一步裂解生成离子m/z 269.0808,与理论值误差为-1.65ppm。 碎片离子m/z 383.0761,失去CO后生成碎片离子m/z 355.0812,与理论值误差为-0.19ppm。该离子通过1.2-消除反应脱水后得到离子m/z 337.0707,与理论值误差为-0.43ppm。后通过1.4-消除反应脱H2O得到离子m/z 319.0601,与理论值误差为-3.01ppm。准分子离子可以通过逆狄尔斯-阿德尔反应(Retro Diels-Alder reaction,RDA反应)生成离子m/z 171.0764,与理论值误差为-0.11ppm。该离子通过电荷转移脱去NH3后得到离子m/z 154.0499,与理论值误差为-0.39ppm。进一步失去CO得到离子m/z 126.0550,与理论值误差为-0.59ppm。准分子离子通过1.2-消除后发生RDA裂解反应得到离子m/z 257.0808。 准分子离子脱NH3后生成的离子通过两次1.2-消除后生成离子m/z 410.1124和离子m/z 392.1129,相对误差分别为0.13ppm和0.25ppm。离子m/z 392.1129脱去中性分子CO后生成离子m/z 364.1179,相对误差为1.49ppm,由离子m/z 365.0656脱H2O得到离子m/z 349.0707,后脱去CO得到离子m/z 321.0757。其可能的裂解途径见图2
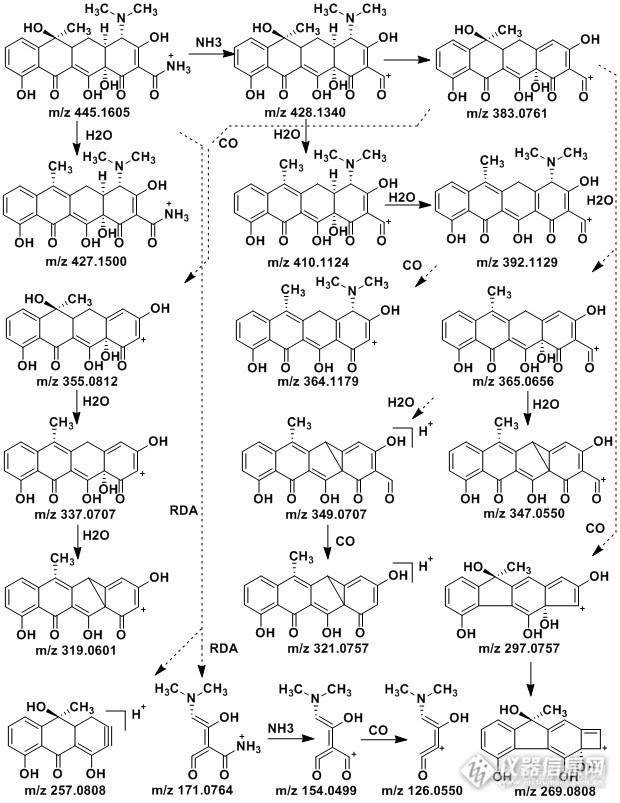
图2 四环素电喷雾离子源下(MS2)可能的质谱裂解途径
Fig.2 Possible cleavage pathways of Tetracycline in the ESI(MS2) mass spectra

表3 四环素正离子的总能量及脱水后离子能量计算基组及水平:B3LYP//6-311++G(3df,3pd)
Table 3aTotal energies(TEs) and binding energies (BEs) of Tetracycline
positive ion andloss H2O calculated at the B3LYP//6-311++G(3df,3pd) levelin gas phase
3 结论
本文通过使用LC-Q-Orbitrap-MS对四环素在电喷雾离子源,正离子模式下的质谱碎裂途径和机理做以解析,并使用密度泛函理论结合量子化学计算,运用Gaussian 03计算分析,计算了不同质子结合位点的质子亲和能,构建了准分子离子的优势构型。量子计算表明质子结合位点位于氨基上具有较高概率,以其为初始进行裂解途径分析与高分辨率质谱给出数据一致,同时对化合物结构中可能的脱水位点进行计算,发现1.2-消除脱水比2.4-消除脱水方式更加容易进行。通过研究发现化合物可以失去通过β位氢重排失去侧链二甲胺,失去水和一氧化碳等裂解过程,通过文中信息可以为此类化合物的结构鉴定提供理论指导依据。
参考文献:
1庞国芳, 曹彦忠, 张进杰,等. 高效液相色谱法同时测定禽肉中土霉素、四环素、金霉素、强力霉素残留的研究. 分析测试学报,2005, 24:61-63.
2贾薇, 孙璐, 史向国,等. 液相色谱-质谱联用法测定牛奶中4种四环素类药物残留量. 沈阳药科大学学报, 2002, 19:96-100.
3岳振峰, 邱月明, 林秀云,等. 高效液相色谱串联质谱法测定牛奶中四环素类抗生素及其代谢产物. 分析化学, 2006,34:1255-1259.
4孙广大, 苏仲毅, 陈猛,等. 固相萃取-超高压液相色谱-串联质谱同时分析环境水样中四环素类和喹诺酮类抗生素. 色谱, 2009,27:54-58.
5沈颖, 魏源送, 郭睿,等. 超高效液相色谱串联质谱检测猪粪中残留的四环素类抗生素. 环境化学, 2009,28(5):747-752.
6程雪梅, 苏青云, 胡炎明. 液相色谱-串联质谱法分析海产品中四环素类药物残留. 质谱学报, 2009,30(2):74-77.
7薛晓锋, 张金振, 赵静,等. 液相色谱质谱法测定蜂王浆中四环素族抗生素残留. 现代科学仪器,2007, 17(1):74-76.
8孙雷, 张骊, 刘琪,等. 猪肉组织中四环素类药物残留检测——高效液相色谱-串联质谱法研究. 中国兽药杂志, 2008, 42:27-29.
9刘正才, 杨方, 余孔捷,等. 超高效液相色谱-串联质谱法快速检测鳗鱼中磺胺类、喹诺酮类、四环素族抗生素药物残留. 食品科学, 2009, 30(14):167-170.
〇rbitrap
第10楼2015/10/09
1.色谱质谱联用为了扣除干扰,获得更加清晰的谱图,谱图采集和色谱有关么?谱图采集是质谱质量分析器扫描完成的无论DI直接进样还是色谱串联质谱进样分析对采集时间没有任何影响,串联只是为了更好的分离,减少杂质的干扰,获得完善的谱图,不然何必要有GCMS LCMS
2.量子计算是为了确定初始电离位点,跟质谱图无关,仅仅是分析母离子在二级裂解下碎片离子的行为和来源,所有特征离子及其丰度表2已给出
3.何所谓很多的分子离子峰?质谱图上只有一个准分子离子峰,当然不排除质子加和到不同位置,但是究竟哪一个位点的概率最大,可以通过计算得出,文章也是基于此的,而质谱采集只是根据质量数出峰的,所以无论加和到那个位点,质量数也是一样的,质谱图是无法区分的,这个如果懂得质谱相关理论你应该是明白的。而裂解行为来讲通过个人的经验,某一种化合物的裂解有时也并非由一个位点引发,但是有一个主要的裂解途径,而占据主导优势,举个简单的例子乙基苯乙酮在EI离子源下裂解会失去甲基自由基,那么会有两种可能,首先对于分子离子峰讲,电离的可能是羰基氧上的一对n电子,因为其电离能最低,但是也有可能是苯环上的一对π电子,那么一般怎么认为呢?我们只能计算其电离能来判断主要的方式,诚然,主要被电离的是杂原子氧上的一对非键合的n电子,所以这两种质谱图是无法区分的,或者只能说质谱图上的分子离子峰是这多种方式之和,再说掉甲基自由基,可能是苄基断裂失去甲基,也可能是乙酰基断裂失去的,那么我们对比羰基氧上电子被电离占据主导优势,所以因其引发的游离基中心诱导的α断裂占据主导,所以认为是羰基裂解失去的,当然其分子离子峰失去甲基在质谱图中表现的可能是两种方式加和的,但是另外一种我们没办法排除,只能说是竞争力不足概率微乎其微,所以一般对于此类不多加以考虑,我们只考虑主要的关键的。这么说不知是否认可
4.事无绝对这个问题3已经说了,我们不排除其他方式,但是只考虑主要的具有竞争力的方式,对于其他的小概率的不能一一考虑
您觉得还缺少那些数据?
liufeilzu
第11楼2015/10/10
不懂计算,看不懂请楼主见谅, 我做结构的时候,比如H/D交换,比如弱相互作用,我一般会用静态nano,选用比较纯的物质,不断调整参数(必要会调整溶剂),cid,hcd和etd步进调整,观察碎片丰度变化来判断碎裂过程和可能的结构信息。前段接分离设备,担心对物质的分析就是一个色谱峰宽的时间,看完楼主的讲解觉得可能这样做不是很恰当;
我做结构的时候,比如H/D交换,比如弱相互作用,我一般会用静态nano,选用比较纯的物质,不断调整参数(必要会调整溶剂),cid,hcd和etd步进调整,观察碎片丰度变化来判断碎裂过程和可能的结构信息。前段接分离设备,担心对物质的分析就是一个色谱峰宽的时间,看完楼主的讲解觉得可能这样做不是很恰当;
我说看楼主的文章算出来质子加在分子很多位置,就是我说的很多分子离子峰(抱歉我表述不好 ),在质谱上应该只观察到一个M+H,那么这些计算的指导意义是?或者楼主算出来的每个M+H后续有不同的裂解途径?因为大部分人看到第一眼就觉得质子会加在氨基上,那些不在氨基上的是否如计算那样存在呢?如何证明它们存在呢?
),在质谱上应该只观察到一个M+H,那么这些计算的指导意义是?或者楼主算出来的每个M+H后续有不同的裂解途径?因为大部分人看到第一眼就觉得质子会加在氨基上,那些不在氨基上的是否如计算那样存在呢?如何证明它们存在呢?
我觉得可以多做些结构类似物和同分异构体,在计算一下异同(个人意见,楼主不要生气)因为您说“为此类化合物的鉴定解析提供理论依据”,一个化合物有点太特殊,看过一些质谱碎片归属的免费软件算法,虽然我不是很明白,觉得是在某个理论指导下,统计和机器人学习很多化合物碎片,形成算法,推算碎片过程。。。