

探究水质中总溶解固体与电导率关系
吕炎 张艳艳 刘翔 王柳
(万华化学(宁波)有限公司,浙江省宁波市 315812)
循环水、锅炉水作为工业生产过程中常见的工业用水,在日常使用中,为保证水质安全,常会添加一些阻垢剂、缓蚀剂、抑泡剂等,这些助剂多为盐类物质,工艺生产过程中,为更好地控制助剂添加量,需要测定工业用水中总溶解固体(TDS)的含量。但目前国家标准中采用重量法分析总溶解固体(TDS)的含量,但该方法存在操作繁琐、耗时长等特点,影响样品的分析效率。目前市场上存在TDS计用于测定总溶解固体(TDS)含量,该方法主要通过测定溶液中电导率来折算溶液中存在的溶解性固体含量。一般情况下,电导率越高,盐份越高,TDS越高,实验室中也会采用“1ppmTDS=2μS/cm” 的关系,测定溶液电导率间接测定总溶解固体(TDS)含量。
但工艺生产的差异,考虑工业用水的助剂成份不同,完全采用上述的关系折算部可靠,本文通过实验研究水质中总溶解固体与电导率的关系。
2、总溶解固体与电导率介绍2.1 总溶解固体介绍总溶解性固体(TDS)是指溶解在水中的固体(如氯化物、硫酸盐、硝酸盐、重碳酸盐及硅酸盐等)的总量,TDS值越高,表示水中含有的溶解物越多。 总溶解固体指水中全部溶质的总量,包括无机物和有机物两者的含量。一般可用电导率值大概了解溶液中的盐份, 电导率越高,盐份越高,TDS越高。在无机物中,除溶解成离子状的成分外,还可能有呈分子状的无机物。由于天然水中所含的有机物以及呈分子状的无机物一般可以不考虑,所以一般也把含盐量称为总溶解固体。总溶解性固体(TDS)的测定:将待测水样用慢速定量滤纸或滤板孔径为2~5μm的玻璃砂芯漏斗过滤。用移液管移取100mL过滤后的水样,置于已于105~110℃干燥至恒重的蒸发皿中。将蒸发皿置于沸水浴上蒸发至干,再将蒸发皿于105~110℃下干燥至恒重。C=(W2-W1)*106/V
3.1.1 氯化钠溶液实验
配制一定梯度的氯化钠溶液,分别测定梯度溶液对应的电导率,形成如下表格:
| 氯化钠溶液实验数据统计 | |||
| 样品 | 质量浓度/mg/L | 理论电荷的物质的量浓度/mol/L | 电导率/μS/cm |
| 梯度1 | 32.035 | 0.0010964 | 55.7 |
| 梯度2 | 64.07 | 0.002192 | 109.4 |
| 梯度3 | 160.175 | 0.004386 | 217.8 |
| 梯度4 | 320.35 | 0.010964 | 522.5 |
| 梯度5 | 640.7 | 0.02192 | 975.1 |
表1:氯化钠溶液实验数据统计
结合上述数据,绘制电导率与质量浓度和理论电荷的物质的量浓度的关系图,如下: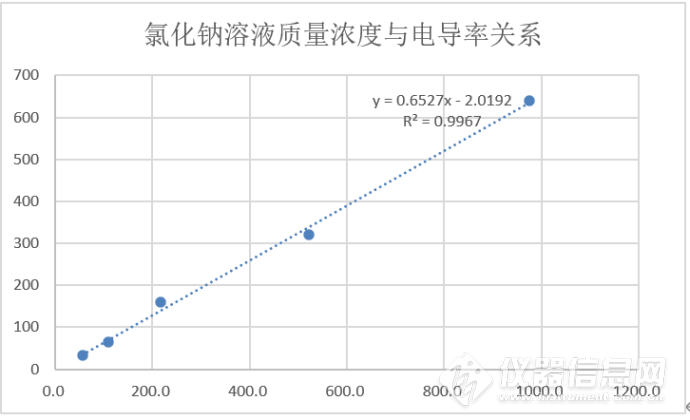
图1:氯化钠溶液质量浓度与电导率关系图
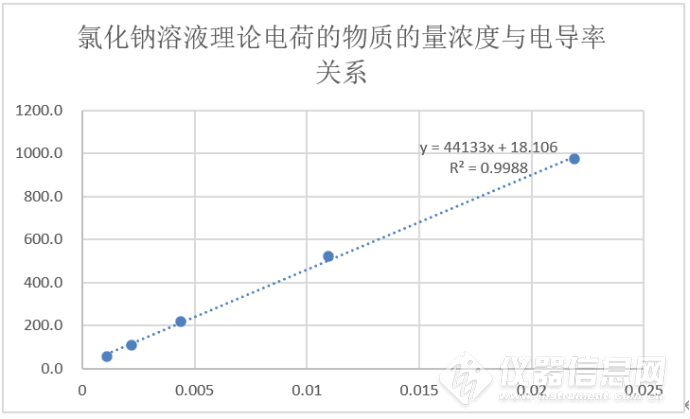
图2:氯化钠溶液理论电荷的物质的量浓度与电导率关系图
3.1.2氯化钾溶液实验
配制一定梯度的氯化钾溶液,分别测定梯度溶液对应的电导率,形成如下表格:
| 氯化钾溶液实验数据统计 | |||
| 样品 | 质量浓度/mg/L | 理论电荷的物质的量浓度/mol/L | 电导率/μS/cm |
| 梯度1 | 37.08 | 0.0009948 | 52.0 |
| 梯度2 | 74.16 | 0.0019896 | 116.6 |
| 梯度3 | 148.32 | 0.00398 | 233.6 |
| 梯度4 | 370.8 | 0.009948 | 569.2 |
| 梯度5 | 741.6 | 0.019896 | 1180.0 |
表2:氯化钾溶液实验数据统计
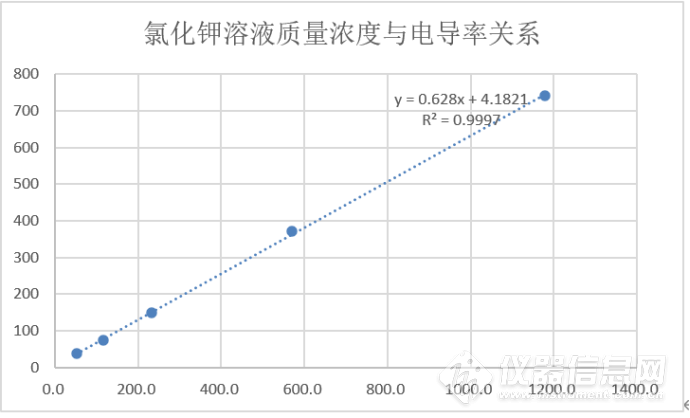
图3:氯化钾溶液质量浓度与电导率关系图
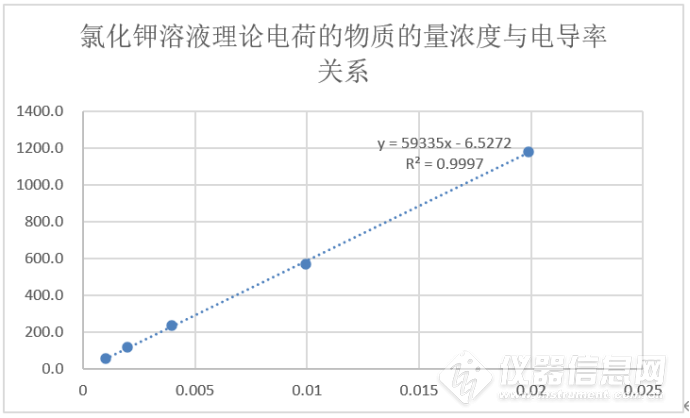
图4:氯化钾溶液理论电荷的物质的量浓度与电导率关系图
3.1.3硫酸钠溶液实验
配制一定梯度的硫酸钠溶液,分别测定梯度溶液对应的电导率,形成如下表格:
| 硫酸钠溶液实验数据统计 | |||
| 样品 | 质量浓度/mg/L | 理论电荷的物质的量浓度/mol/L | 电导率/μS/cm |
| 梯度1 | 71.205 | 0.0020052 | 88.9 |
| 梯度2 | 142.41 | 0.004012 | 199.1 |
| 梯度3 | 284.82 | 0.00802 | 403.2 |
| 梯度4 | 712.05 | 0.020052 | 942.6 |
| 梯度5 | 1424.1 | 0.04012 | 1823.0 |
表3:硫酸钠溶液实验数据统计
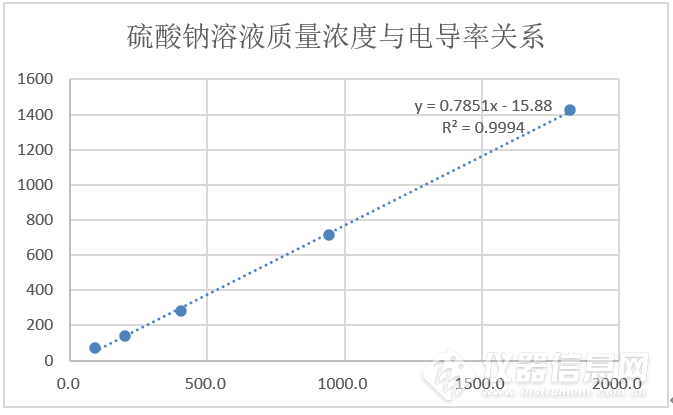
图5:硫酸钠溶液质量浓度与电导率关系图

图6:硫酸钠溶液理论电荷的物质的量浓度与电导率关系图
3.1.4乙酸钠溶液实验
配制一定梯度的乙酸钠溶液,分别测定梯度溶液对应的电导率,形成如下表格:
| 乙酸钠溶液实验数据统计 | |||
| 样品 | 质量浓度/mg/L | 理论电荷的物质的量浓度/mol/L | 电导率/μS/cm |
| 梯度1 | 42.83 | 0.0010442 | 29.7 |
| 梯度2 | 85.66 | 0.002088 | 69.6 |
| 梯度3 | 171.32 | 0.004176 | 139.6 |
| 梯度4 | 428.3 | 0.010442 | 371.4 |
| 梯度5 | 856.6 | 0.02088 | 716.5 |
表4:乙酸钠溶液实验数据统计
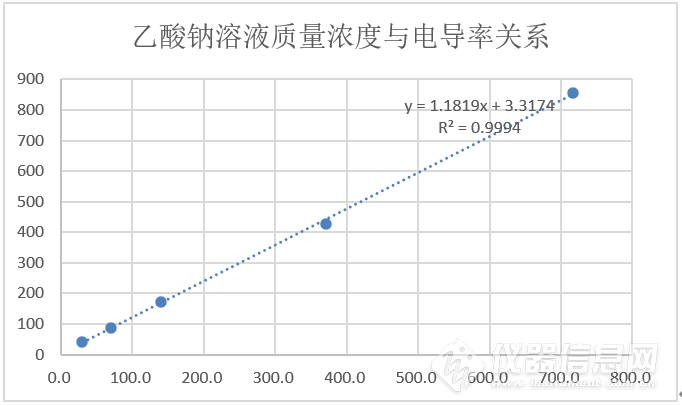
图7:乙酸钠溶液质量浓度与电导率关系图
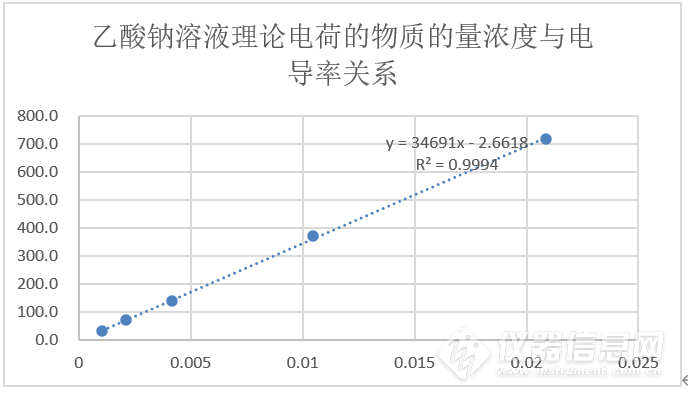
图8:乙酸钠溶液理论电荷的物质的量浓度与电导率关系图
3.1.5硫酸铜溶液实验
配制一定梯度的硫酸铜溶液,分别测定梯度溶液对应的电导率,形成如下表格:
| 硫酸铜溶液实验数据统计 | |||
| 样品 | 质量浓度/mg/L | 理论电荷的物质的量浓度/mol/L | 电导率/μS/cm |
| 梯度1 | 79.575 | 0.0019944 | 79.1 |
| 梯度2 | 159.15 | 0.0039884 | 178.8 |
| 梯度3 | 318.3 | 0.007976 | 333.4 |
| 梯度4 | 795.75 | 0.019944 | 722.7 |
| 梯度5 | 1591.5 | 0.039884 | 1250.1 |
表5:硫酸铜溶液实验数据统计
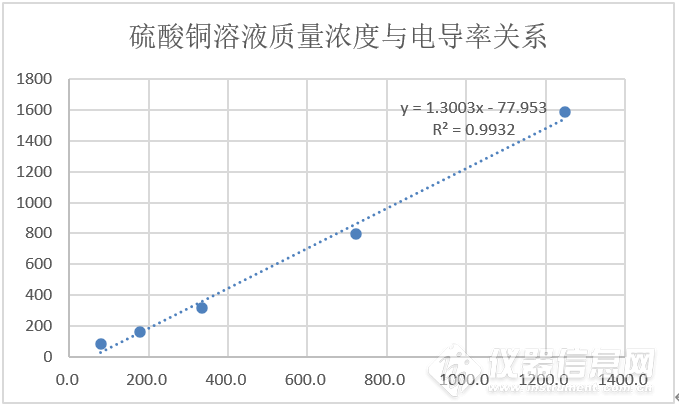
图9:硫酸铜溶液质量浓度与电导率关系图
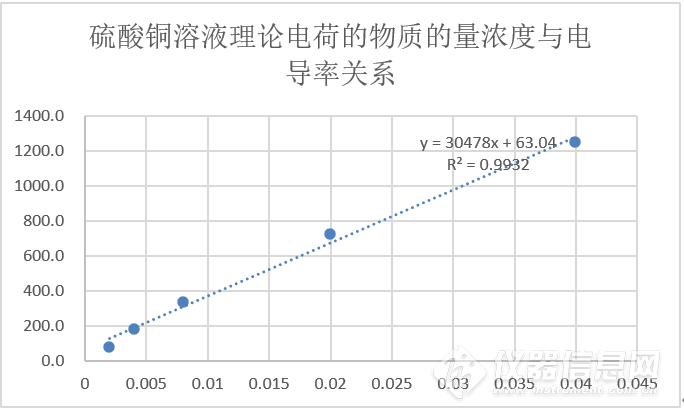
图10:硫酸铜溶液理论电荷的物质的量浓度与电导率关系图
3.1.6磷酸氢二钾溶液实验
配制一定梯度的磷酸氢二钾溶液,分别测定梯度溶液对应的电导率,形成如下表格:
| 磷酸氢二钾溶液实验数据统计 | |||
| 样品 | 质量浓度/mg/L | 理论电荷的物质的量浓度/mol/L | 电导率/μS/cm |
| 梯度1 | 68.12 | 0.0020024 | 47.4 |
| 梯度2 | 136.24 | 0.004004 | 84.3 |
| 梯度3 | 272.48 | 0.008008 | 173.6 |
| 梯度4 | 681.2 | 0.020024 | 432.9 |
| 梯度5 | 1362.4 | 0.04004 | 862.8 |
表6:磷酸氢二钾溶液实验数据统计
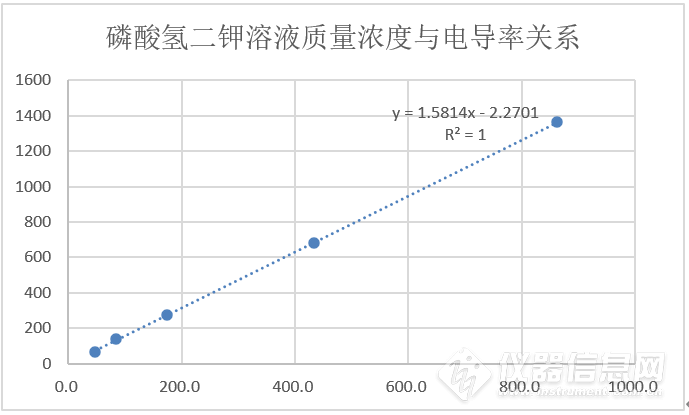
图11:磷酸氢二钾溶液质量浓度与电导率关系图
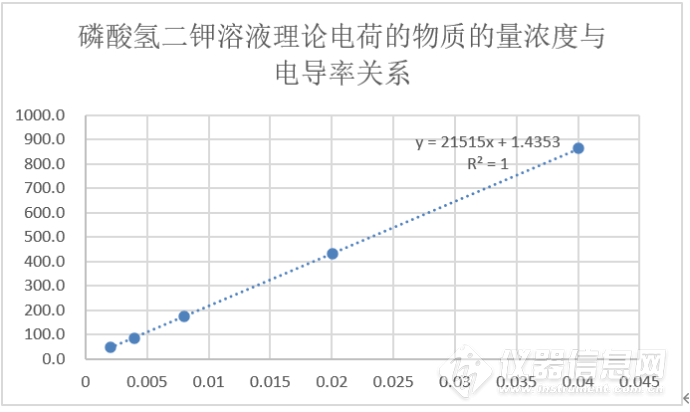
图12:磷酸氢二钾溶液理论电荷的物质的量浓度与电导率关系图
3.1.7 氯化钙溶液实验
配制一定梯度的氯化钙溶液,分别测定梯度溶液对应的电导率,形成如下表格:
| 氯化钙溶液实验数据统计 | |||
| 样品 | 质量浓度/mg/L | 理论电荷的物质的量浓度/mol/L | 电导率/μS/cm |
| 梯度1 | 55.5 | 0.0019896 | 97.1 |
| 梯度2 | 110.4 | 0.0039792 | 194.2 |
| 梯度3 | 220.8 | 0.00796 | 376.8 |
| 梯度4 | 552.0 | 0.019896 | 911.0 |
| 梯度5 | 1104.0 | 0.039792 | 1853.9 |
表7:氯化钙溶液实验数据统计
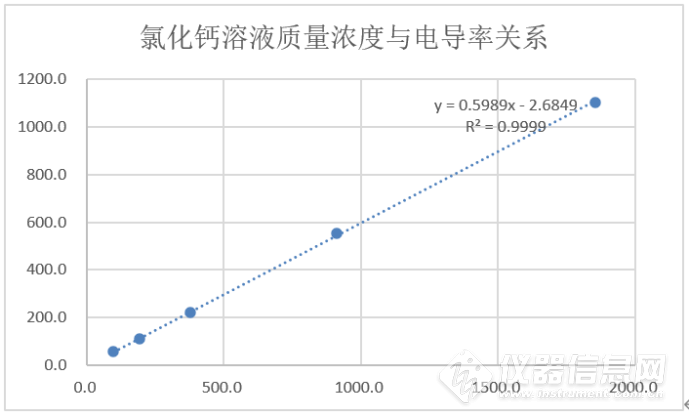
图13:氯化钙溶液质量浓度与电导率关系图
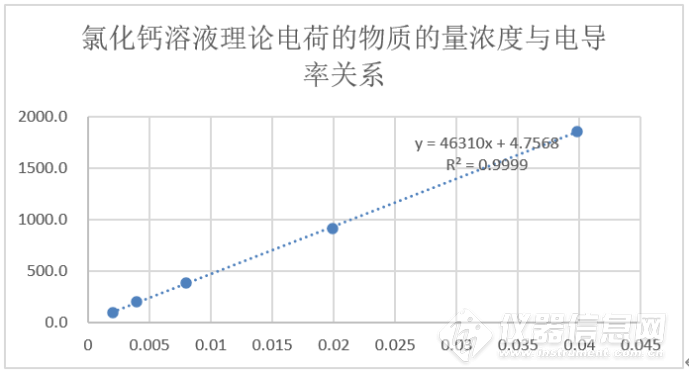
图14:氯化钙溶液理论电荷的物质的量浓度与电导率关系图
3.1.8 单一溶液实验总结
| 溶液名称 | 质量浓度/电导率 (mg/L/μS/cm) | 电导率/电荷物质的量浓度 (μS/cm/mol/L) |
| 氯化钠溶液 | 0.6527 | 44133 |
| 氯化钾溶液 | 0.628 | 59335 |
| 硫酸钠 | 0.7851 | 45183 |
| 乙酸钠 | 1.1819 | 34691 |
| 硫酸铜 | 1.3003 | 30478 |
| 磷酸氢二钾 | 1.5814 | 21515 |
| 氯化钙 | 0.5989 | 46310 |
表8:单一溶液实验汇总数据
3.2多组分盐类与电导率关系
从上述单一组分盐类的实验可以看出不同种类的盐类对于电导率的影响不同,因此需要通过实验进行探究不同离子浓度与电导率之间的关系。
3.2.1多组分盐类实验探究
目前我们装置上使用的助剂主要有磷酸盐类,同时我们的工业用水的体系中存在钠、钾、钙、氯和硫酸根等离子组分,通过采用上述离子配制相应浓度的溶液,并测定对应的电导率值,测定数据汇总如下:
| 样品 | 1 | 2 | 3 | 4 | 5 | 6 |
| Na+/mg/L | 46.12 | 92.24 | 60.85 | 94.37 | 81.78 | 140.49 |
| K+/mg/L | 78.04 | 97.61 | 19.57 | 39.14 | 97.61 | 39.02 |
| Ca2+/mg/L | 39.87 | 79.74 | 59.81 | 119.61 | 19.94 | 39.87 |
| Cl-/mg/L | 105.95 | 176.58 | 164.31 | 250.80 | 90.08 | 127.20 |
| SO42-/mg/L | 96.35 | 192.70 | 48.17 | 289.04 | 144.52 | 240.87 |
| PO43-/mg/L | 95.08 | 142.63 | 47.54 | 95.08 | 142.63 | 47.54 |
| 电导率/μS/cm | 561.4 | 994.0 | 581.0 | 1055.7 | 673.6 | 876.7 |
表8:多组分溶液实验数据统计
κ=4.285C(Na+)+2.079C(K+)+4.6988C(Ca2+)-0.07697C(Cl-)+0.02512C(SO42-)+0.2096C(PO43-)
3.2.2实验论证数学模型的可行性
| 样品 | 1 | 2 | 3 | 4 |
| Na+/mg/L | 92.24 | 0.00 | 115.29 | 46.12 |
| K+/mg/L | 78.28 | 156.56 | 0.00 | 97.85 |
| Ca2+/mg/L | 0.00 | 79.74 | 99.68 | 39.87 |
| Cl-/mg/L | 0.00 | 141.26 | 176.58 | 70.63 |
| SO42-/mg/L | 192.70 | 0.00 | 240.87 | 96.35 |
| PO43-/mg/L | 190.17 | 380.34 | 0.00 | 237.71 |
| 理论值/μS/cm | 602.67 | 769.02 | 954.87 | 635.20 |
| 实测值/μS/cm | 632.60 | 831.10 | 985.20 | 592.40 |
| 相对偏差/% | -2.42 | -3.88 | -1.56 | 3.49 |
4.实验总结
⑴单一溶液质量浓度/电导率值为变值,且与在用理论值0.5偏差大,因此实际操作中选用0.5倍的电导率值为TDS含量的结果是不准确的,结果偏低。
⑵单一电导率值/电荷物质的量浓度值也为为变值,因此相同电荷数条件下,不同物质对电导率影响也不相同,不同物质对电导率影响主要体现在以下3个因素:水化离子半径、离子价数和特殊迁移方式,一般情况下,半径r越大,则运动速度v越小,电导率越小;离子价数越大,则运动速度v越大,电导率越大;H+、OH-是一般离子导电能力5-8倍。
⑶实验所得的数学模型是可靠的,在相同体系条件下可以用于电导率与TDS之间的转化。
5.参考文献
[1]方志刚,杨岳平,周德佳.海水淡化与舰船淡水保障.国防工业出版社.2016.03.第18页.