酶催化新机制助力高效C-N键合成!
导读:本文报道了一种通过光酶催化实现高效、高立体选择性合成2,2-二取代吡咯烷的新方法,解决了传统方法在构建C-N键时的挑战。
【研究背景】
氮-碳键的形成在现代化学合成中至关重要,因为氮杂环广泛存在于小分子药物和农用化学品中。与传统的化学方法相比,烯烃的氢胺化是一种原子经济的策略,用于构建新的C–N键,尤其是在制备α-三级胺方面具有重要意义。然而,这些反应在实现不对称合成时存在挑战,尤其是当涉及到完全取代的碳立体中心时。虽然过渡金属催化的氢胺化反应已被广泛研究,但其在构建立体位阻较大的键方面效果不佳,且依赖自由基中间体的反应往往只能生成反Markovnikov产物。最近,布朗斯特酸催化剂在这一领域表现出潜力,但其官能团耐受性差,需要去活化的胺才能实现对映选择性,因此尚未在实际应用中得到广泛采用。
针对上述挑战,普林斯顿大学Todd K. Hyster等携手在酶催化的氢胺化反应中取得了新的进展。该团队通过蛋白质工程设计并制备了一个特定的酶突变体,利用Baeyer-Villiger单氧化酶实现了对2,2-二取代吡咯烷的高效合成。该过程通过光酶反应,显著提高了产物的产率和立体选择性,克服了传统方法的局限性。与相关的光化学氢胺化反应不同,该工作利用了还原生成的苯基自由基与氮原子孤对之间的通过空间相互作用,这一反键相互作用降低了自由基的氧化电位,从而促进了电子向黄素辅助因子的转移。
此外,分子动力学模拟表明,酶的微环境对于这一新型C–N键形成机制的实现至关重要,且这一机制在小分子催化中并无相似之处。这项研究展示了通过蛋白质工程增强新兴机制的潜力,提供了独特的机制解决方案,以应对化学合成中的未解挑战。这一进展不仅为合成化学提供了新的思路,也为生物催化剂在非自然反应中的应用奠定了基础。

【表征解读】
本文通过多种表征手段,如紫外-可见光谱(UV-Vis)、气相色谱-质谱(GC-MS)和核磁共振(NMR)等,发现了酶催化反应中还原型黄素(FADhq)在自由基发起中的关键作用,从而揭示了该反应的独特机制。针对酶催化反应中观察到的诱导期现象,通过紫外-可见光谱分析,作者确认了在光还原条件下产生的FADhq与通过二硫化钠还原的FAD在光谱特征上是相同的,这一发现为理解反应机理提供了重要的微观机理依据。特别是,观察到的诱导期的消失表明,反应的启动依赖于FAD的光还原,进一步挖掘了这一反应的复杂性。
在此基础上,作者通过气相色谱-质谱和核磁共振技术对相关反应产物进行分析,结果显示在特定条件下,形成的产物与文献中的已知反应机制不符,强调了在酶的催化作用下,底物的反应路径具有特殊性。此外,通过对底物和产物的进一步分析,探讨了FADhq与烯烃之间的还原反应的可能性。利用密度泛函理论(DFT)对反应中中间体的前线分子轨道(FMO)进行了计算,进一步揭示了产物形成的电子特性和反应机理。
总之,经过上述表征,作者深入分析了酶催化的氢氨化反应中自由基的生成和转化过程,进而制备了新的反应材料。这一研究不仅为理解氢氨化反应提供了新的视角,也为新材料的开发和应用推动了进步。特别是对酶的工程改造所带来的底物构象自由度的增加,为C–N键的高效形成提供了新的可能性,从而为未来的催化研究奠定了基础。通过多维度的表征手段和细致的机理分析,本文为理解复杂生化反应中的催化机制提供了重要的实验依据。
【图文速递】
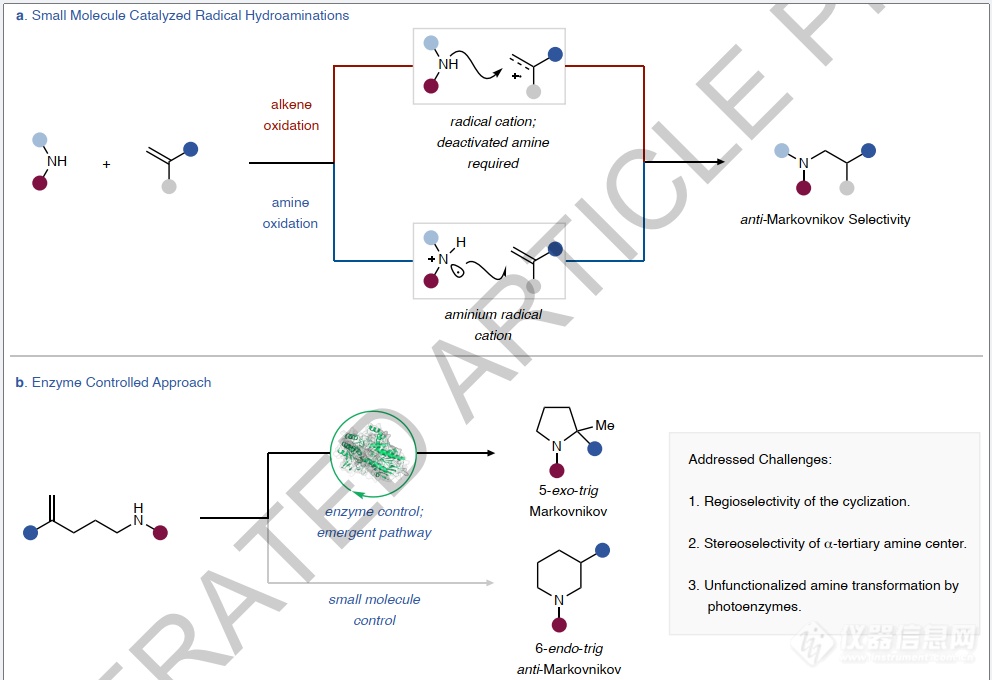
图1:自由基氢胺化的挑战。
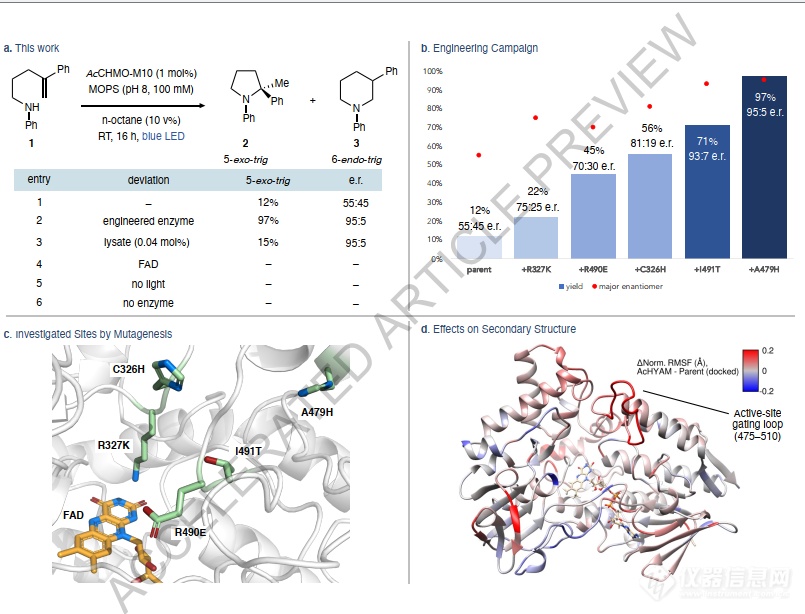
图2:蛋白质进化。
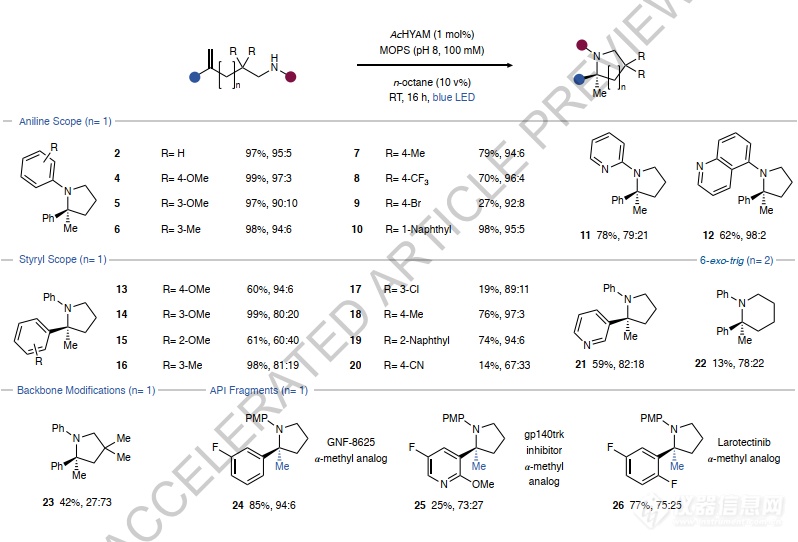
图3:C–N形成反应范围。
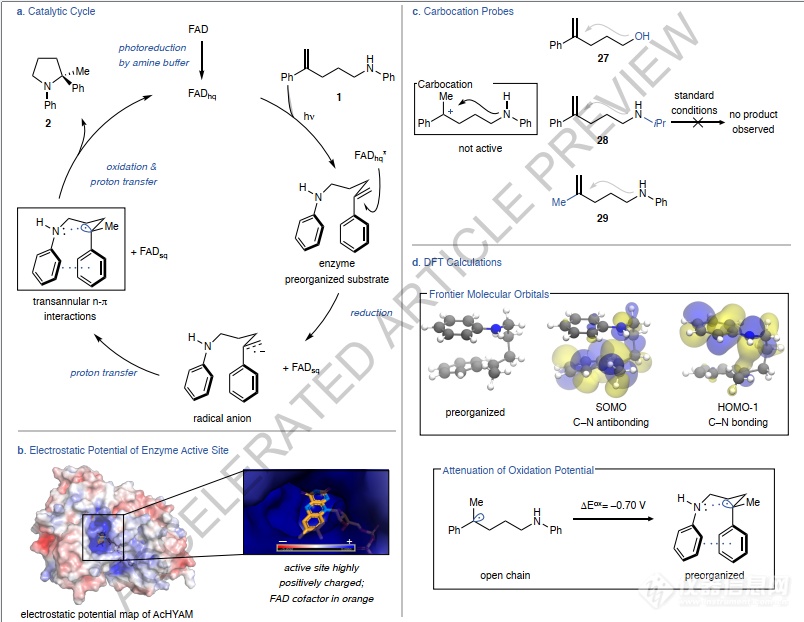
图4:基底探针和DFT机理研究。
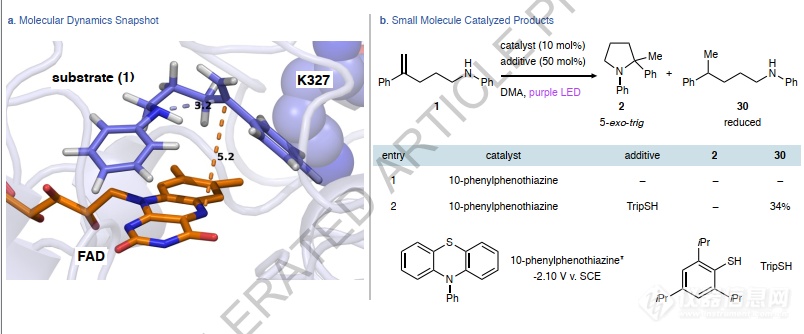
图5:用分子动力学和小分子研究底物结合测试。
【结论展望】
本文展示了酶在化学合成中作为理想支架的潜力,特别是在构建C–N键的氢胺化反应中。酶通过其独特的微环境和协同作用,能够实现自由基反应的高选择性,这是传统催化剂无法比拟的。这种涌现机制的应用,尤其是在非自然反应中,为催化领域提供了新的思路。文章中提到的光酶催化过程,利用未活化的自由基前体,成功实现了2,2-二取代吡咯烷的合成,表明通过蛋白质工程优化酶的活性和选择性是可行的。这一研究不仅拓宽了光酶催化的合成实用性,也为未来设计新型生物催化剂提供了新的视角。通过分子动力学模拟进一步验证了底物在酶活性位点中的相互作用,强调了酶的微环境在反应机制中的重要性。整体而言,这项研究为非自然生物催化的发展提供了新的机制理解,展现了利用蛋白质工程来解决化学合成中的未解挑战的巨大潜力。
文献信息:Raps, F.C., Rivas-Souchet, A., Jones, C.M. et al. Emergence of a distinct mechanism of C–N bond formation in photoenzymes. Nature (2024). https://doi.org/10.1038/s41586-024-08138-w
来源于:仪器信息网
热门评论
最新资讯
新闻专题
更多推荐