
方案摘要
方案下载| 应用领域 | 化药/中药/生物制药 |
| 检测样本 | 中药材和饮片 |
| 检测项目 | 限度检查 |
| 参考标准 | 2020版《中国药典》 |
本实验室按照2020版《中国药典》中分析方法,筛选合适的色谱柱,使地黄饮片和熟地黄中地黄苷D与其前后相邻杂质之间的分离度能够达到基线分离,同时,地黄苷D峰的理论塔板数应满足药典要求(不低于5000)。
2020版《中国药典》第一部 地黄饮片和熟地黄中地黄苷D的分析
客户向我们提供了地黄苷D标准品溶液(液体)、地黄饮片和熟地黄(固体粉末)。希望本实验室能够按照2020版《中国药典》中分析方法,筛选合适的色谱柱,使地黄饮片和熟地黄中地黄苷D与其前后相邻杂质之间的分离度能够达到基线分离,同时,地黄苷D峰的理论塔板数应满足药典要求(不低于5000)。
我们按照2020版《中国药典》熟地黄含量测定项下方法,对地黄饮片和熟地黄进行了提取处理,然后按照药典方法,
在CAPCELL PAK C18 MGII色谱柱上得到了良好的分析结果。
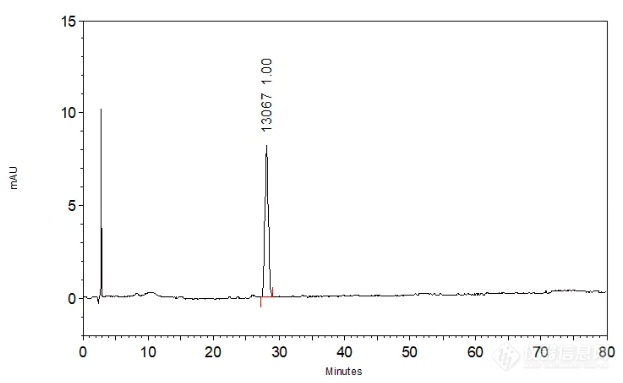
首先,下图为使用CAPCELL PAK C18 MGII S5; 4.6 mm i.d. × 250 mm色谱柱,对地黄苷D标准品的分析结果。
HPLC Conditions :
色谱柱:CAPCELL PAK C18 MGII S5; 4.6 mm i.d.×250 mm
流动相:0.1%磷酸/甲醇 = 95/5
流 速:1.0 mL/min
温 度:35°C
检 测:UV 203 nm
浓 度:客户提供
进样量:10 µL
结果中,地黄苷D的保留时间为28.135 min,理论塔板数为13067,满足药典不低于5000的要求,峰不对称因子为1.00,峰形良好。
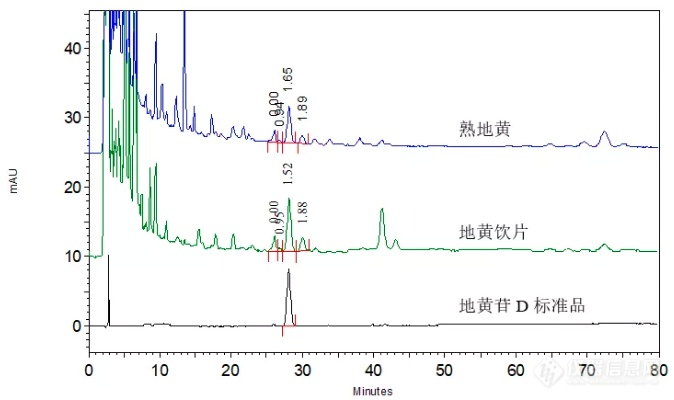
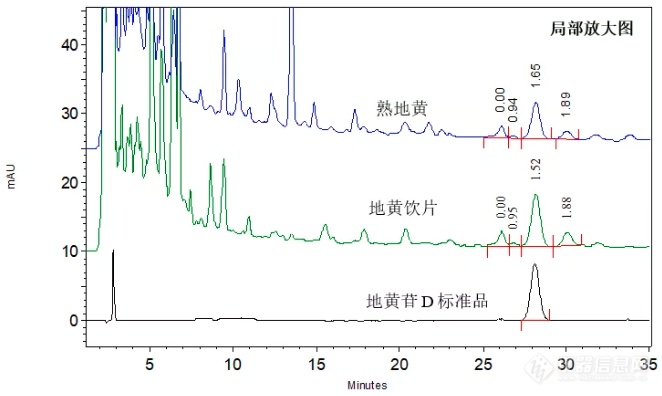
随后,我们使用同样方法对熟地黄和地黄饮片的实际样品进行了分析,结果如下图所示:
HPLC Conditions :
色谱柱:CAPCELL PAK C18 MGII S5; 4.6 mm i.d.×250 mm
流动相:0.1%磷酸/甲醇 = 95/5
流 速:1.0 mL/min
温 度:35 °C
检 测:UV 203 nm
浓 度:样品按药典方法处理
进样量:10 µL
地黄饮片中地黄苷D与其前后相邻杂质之间的分离度分别为1.52和1.88,熟地黄中地黄苷D与其前后相邻杂质之间的分离度分别为1.65和1.89,均可以得到基线分离。
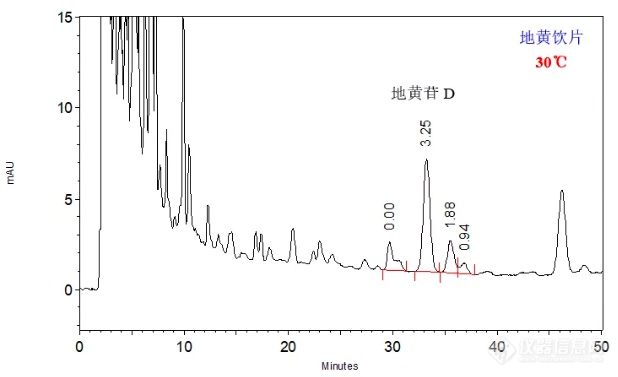
然而从上面实际样品的结果可以看到,地黄饮片样品中地黄苷D与其前相邻杂质之间的分离度仅为1.52,刚刚达到基线分离,为了使其得到更好的分离,我们尝试对柱温进行调整,分别在30℃和40℃对地黄饮片进行分析,结果如下面两张图所示:
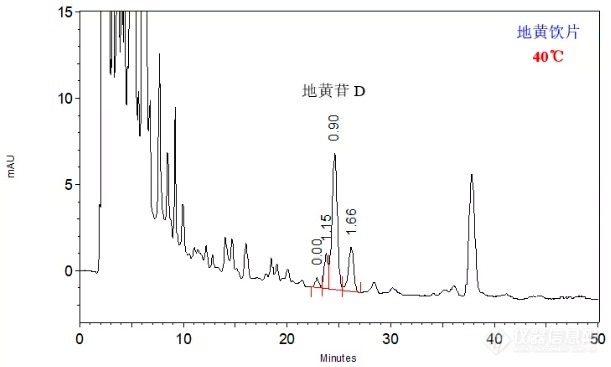
HPLC Conditions :
色谱柱:CAPCELL PAK C18 MGII S5; 4.6 mm i.d.×250 mm
流动相:0.1%磷酸/甲醇 = 95/5
流 速:1.0 mL/min
温 度:30°C / 40°C
检 测:UV 203 nm
浓 度:样品按药典方法处理
进样量:10 µL
在30℃柱温下,地黄苷D与其前后相邻杂质之间的分离度分别为3.25和1.88,能够得到良好的分离。在40℃柱温下,地黄苷D与其前后相邻杂质之间的分离度分别为0.90和1.66,地黄苷D与其前杂质未能达到基线分离,升温不利于分离。
针对药典中地黄饮片和熟地黄中地黄苷D的分析,我们总结了以下注意事项:
(1). 由于中药样品中成分比较复杂,在不同色谱柱上的分离情况差异比较大,建议客户在分析时,可根据具体分离情况,对有机相比例及柱温进行调整,以得到良好的分离。
(2). 地黄饮片及熟地黄中均含有疏水性较大的物质,我们进行80min的洗脱后,仍可能有疏水性物质未得到洗脱,建议使用高有机相进行冲洗。
综上所述,使用CAPCELL PAK C18 MGII色谱柱,按照2020版《中国药典》熟地黄含量测定项下方法,能够得到满足药典分离度和理论塔板数要求的分析结果。

2020版药典 药用辅料 山梨醇杂质分析CP+NQAD解决方案
2020版《中国药典》 药用辅料 三氯蔗糖的常规分析 & 快速分析
2020版《中国药典》 药用辅料 羟苯甲酯、羟苯乙酯、羟苯丙酯、羟苯丁酯、羟苯卞酯的分析
相关产品
气溶胶激光计数检测器
高压六通切换阀(2连)
DAISOPAK C18 SP-P 液相色谱柱
Ghost Cleaner I 鬼峰捕集柱
大曹帕克 SP-120-5-SIL-P Silica柱
大曹帕克 SP-100-5-SIL-P Silica柱
大曹帕克 SP-120-5-C8-P C8(MOS)柱
大曹帕克 SP-100-5-ODS-P C18(ODS)柱
大曹帕克 SP-120-5-APS-P 亲水柱
预柱芯MF Ph-1(原资生堂)
预柱芯NH2 UG80(原资生堂)
预柱卡套 4.0×20mm
预柱芯MF SCX(原资生堂)
超高压快速分析保护CAPCELL PAK(原资生堂)
预柱卡套

关注

拨打电话

留言咨询