推荐厂家
暂无
暂无
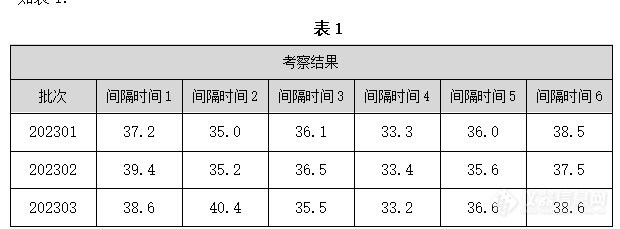
[align=center][b]食品叶酸检测分析[/b][/align][align=left][b]实验背景:[/b][font=宋体]检验过程中发现经过考察后,食品中叶酸检验结果有增长趋势,[/font][font=宋体]。[/font][font=宋体][b]对数据进行原因分析,结论为实验室之间检测误差导致。[/b][font=宋体]检验方法[/font][font=宋体]1.1仪器与用具:电热鼓风干燥箱、电子天平、旋涡混合仪、立式压力蒸汽灭菌器、紫外可见分光光度计、生物安全柜、生化培养箱、离心管、容量瓶、量筒、试管、[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url]。[/font][font=宋体][font=宋体]注:所用玻璃器皿使用前用盐酸浸泡液或月桂基磺酸钠洗涤剂清洗干净后,[/font][font=宋体]250℃干热1h~2h。[/font][/font][font=宋体]1.2试剂:20%乙醇溶液(2+8)、氢氧化钠乙醇溶液(0.01mol/L)、氢氧化钠溶液(1mol/L)。[/font][font=宋体]1.3培养基:琼脂培养基,叶酸测定培养基。[/font][font=宋体]1.4 标准品:叶酸标准品。[/font][font=宋体]1.5菌种的制备与保存:[/font][font=宋体]菌种:鼠李糖乳杆菌或等效菌株。[/font][font=宋体][font=宋体]储备菌种的制备:将菌种鼠李糖乳杆菌转接至菌种储备用琼脂培养基中,在[/font][font=宋体]36℃±1℃恒温培养箱中培养20h~24h,连续转种2代~3代。取出后放入2℃~4℃冰箱作为储备菌株保存。[/font][/font][font=宋体][font=宋体]实验前将储备菌株接种至菌种储备用琼脂培养基中,在[/font][font=宋体]36℃±1℃恒温培养箱中培养20h~24h以活化菌株,用于接种液的制备。[/font][/font][font=宋体][font=宋体]注:保存[/font][font=宋体]2周以上的储备菌种,不能立即用作接种液制备,实验前宜连续传种2代~3代以保证细菌活力。[/font][/font][font=宋体]1.6接种液的制备:实验前一天,取2mL叶酸标准工作液与4mL叶酸测定用培养基混匀,分装至2支试管中,于121℃(0.10MPa~0.12MPa)高压灭菌15min(或根据培养基标签标识进行灭菌)后即为种子培养液。冷却后用接种环将活化的菌株转种至2支种子培养液中,于36℃±1℃恒温培养箱中培养20h~24h。取出后将种子培养液混悬,无菌操作下吸取0.5mL转种至5mL不加叶酸标准工作液的无菌叶酸测定培养基中,于36℃±1℃再培养6h,以消耗种子培养液中残存在菌株中的多余叶酸,制成接种液。[/font][font=宋体]1.7分析步骤(所有操作均需避光进行)[/font][font=宋体][font=宋体]试样提取:准确称取液体试样[/font][font=宋体]0.5mL~2mL,精确至0.001g,转入锥形瓶中,加入80mL氢氧化钠乙醇溶液,具塞,超声振荡0.5h~4h至试样完全溶解或分散,转入100mL容量瓶中,用水定容至刻度。[/font][/font][font=宋体][font=宋体]稀释:根据试样中叶酸含量用水对试样提取液进行适当稀释,使试样稀释液中叶酸含量在[/font][font=宋体]0.2ng/mL~0.3ng/mL范围内。[/font][/font][font=宋体]1.8试样测定[/font][font=宋体][font=宋体]试样系列管:取[/font][font=宋体]3支试管,分别加入1.0mL、2.0mL、3.0mL试样稀释液(Vx),补水至5.0mL,混匀。每个梯度做2个平行。[/font][/font][font=宋体][font=宋体]标准系列管:取试管分别加入叶酸标准工作溶液[/font][font=宋体]0.00mL、0.25mL、0.50mL、1.00mL、1.50mL、2.00mL、2.50mL、3.00mL、4.00mL和5.00mL,补水至5.00mL,相当于标准系列管中叶酸含量为0.00ng、0.05ng、0.10ng、0.20ng、0.30ng、0.40ng、0.50ng、0.60ng、0.80ng和1.00ng,混匀。制备2套~3套标准系列管,绘制标准曲线时,以每个标准点平均值计算。[/font][/font][font=宋体][font=宋体]灭菌:将所有测定系列管、叶酸测定培养基于[/font][font=宋体]121℃(0.10MPa~0.12MPa)高压灭菌15min(或根据培养基要求进行灭菌)。[/font][/font][font=宋体][font=宋体]接种和培养:待测定系列管冷却至室温后,在无菌操作条件下,每[/font][font=宋体]10mL叶酸测定培养基加入接种液40μL,混匀,每支测定管中加入接种后的叶酸测定培养基5mL,混匀。置于36℃±1℃恒温培养箱中培养20h~40h,获最大混浊度时终止培养。另准备一支标准0管(含0.00ng叶酸)不接种作为0对照管。[/font][/font][font=宋体][font=宋体]测定:将培养好的标准系列管、试样系列管用旋涡混合仪混匀。用[/font][font=宋体]1cm比色杯,于540nm处,以未接种0对照管调节透光率为100%(或吸光度值为0),依次测定标准系列管、试样系列管的透光率(或吸光度值)。如果0对照管出现浑浊,说明可能有杂菌污染,需重做实验。[/font][/font][font=宋体][font=宋体]注:适宜的测定光谱范围为[/font][font=宋体]540nm~610nm。[/font][/font][font=宋体]1.9分析结果表述:[/font][font=宋体] [font=宋体]标准曲线:以标准系列管叶酸含量为横坐标,每个标准点透光率(或吸光度值)均值为纵坐标,绘制标准曲线。[/font][/font][font=宋体][font=宋体]试样结果计算:从标准曲线计算试样系列管中叶酸的相应含量([/font][font=宋体]cx),如果3支试样系列管中有2支叶酸含量在0.10ng~0.80ng范围内,且各管之间折合为每毫升试样提取液中叶酸含量的偏差小于10%,则可继续按式进行结果计算,否则需重新取样测定。[/font][/font][font=宋体] [/font][font=宋体]2.检验结果[/font][font=宋体]分析的数据,叶酸含量没有降解趋势,结果符合[/font][font=宋体]GB 29922-2013[/font][font=宋体][font=宋体]的规定,结果如表[/font][font=宋体]1:[/font][/font][img=,620,229]https://ng1.17img.cn/bbsfiles/images/2023/07/202307011003010672_7959_2227357_3.png!w620x229.jpg[/img][b]3.[font=宋体]原因分析[/font][/b][font=宋体]GB 5009.211-2014《[/font][font=宋体][font=宋体]食品安全国家标准[/font] [/font][font=宋体]食品中叶酸的测定[/font][font=宋体][font=宋体]》方法为微生物法,实验过程需要将鼠李糖乳杆菌接种至含有样品的培养液中,培养后测定其吸光值,根据含量与透光率的关系,绘制标准曲线并计算出试样中的叶酸含量,整个实验过程人员、所处的环境、菌液的生长差异、吸光值测定时设备台间差,都直接影响检验结果。考察期叶酸含量稳定没有增长[/font][font=宋体]/降解趋势;综合分析[/font][/font][font=宋体]叶酸检验结果有增长趋势,系实验室之间检测误差导致。[/font]实验也是解决问题的过程,持续改进方法,不断增强技术。[font=宋体][font=宋体][/font][/font][/font][/align]
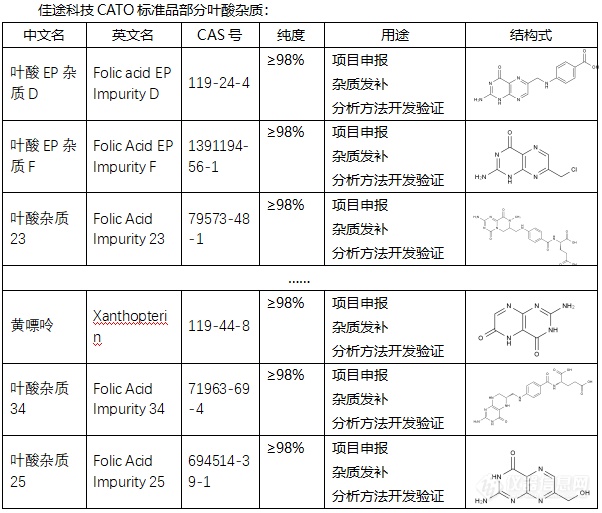
[font=宋体]◇叶酸杂质[/font][font='Segoe UI'][color=#05073b][font=Segoe UI] 叶酸杂质通常是指在叶酸的生产或保存过程中产生的非目标化合物。这些杂质可能会影响叶酸的纯度和效果,因此在叶酸的生产和质量控制过程中需要严格控制其含量。叶酸杂质有多种类型,每一种都具有不同的化学特性,如[/font]CAS号、分子式、分子量等。例如,有一种叶酸杂质CAS号为82778-08-3,分子式为C7H7ClN6HCl,分子量为247.08。另一种叶酸杂质G的CAS号为6810-75-9,英文名称为Folinic Acid Impurity G。此外,叶酸杂质5的CAS号为873397-19-4,纯度为98% HPLC。[/color][/font][font=宋体][font=Calibri] CATO[/font][font=宋体]标准品提供的叶酸全套的杂质[/font][/font][font=宋体],[/font][font=宋体]这些杂质对于药物的纯度和稳定性研究至关重要,也是药物研发过程中不可或缺的一部分[/font][font=宋体]。[img=,602,513]https://ng1.17img.cn/bbsfiles/images/2024/02/202402182015587706_5356_6381607_3.png!w602x513.jpg[/img][/font][font=宋体][color=#05073b][back=#fdfdfe] 广州[/back][/color][/font][font='Segoe UI'][color=#05073b][back=#fdfdfe]佳途科技[/back][/color][/font][font=宋体][color=#05073b][back=#fdfdfe]股份有限公司[/back][/color][/font][font='Segoe UI'][color=#05073b][back=#fdfdfe]深知药物研发与质量控制的重要性[/back][/color][/font][font=宋体][font=宋体],[/font][font=Calibri]CATO[/font][font=宋体]标准品厂家,提供叶酸全套[/font][/font][font=宋体]的[/font][font=宋体]杂质,为客户提供更加精准、可靠的分析标准品,助力药物研发事业的快速发展[/font][font=宋体],[/font][font=宋体]以满足客户在药物研发和质量控制方面的需求。[/font]
GB 5009.211-2014微生物法测定叶酸标准3.5.1叶酸标准储备液20.5ug/mL的配制:精确称取20.mg叶酸标准品,用氢氧化钠乙醇溶液定容至1000mL,然后在256nm处进行了标定,得到浓度为c1。然后3.5.2配制叶酸标准中间液(0.200ug/mL)时,是吸取1mL上述储备液定容至100mL,但没有用到标定浓度c1啊,这不符合试剂配制原理吧,还是说有什么特殊情况?6.7测定 部分,测定时采用的是540nm,但是标定时采用的254nm,为什么不一样呢?问题1:标准储备液标定的作用是什么?问题2:标定和检测时的波长为什么不一致?







 400-696-6689
400-696-6689
 留言咨询
留言咨询
 400-629-8889
400-629-8889
 留言咨询
留言咨询

 400-803-2799
400-803-2799
 留言咨询
留言咨询