推荐厂家
暂无
暂无
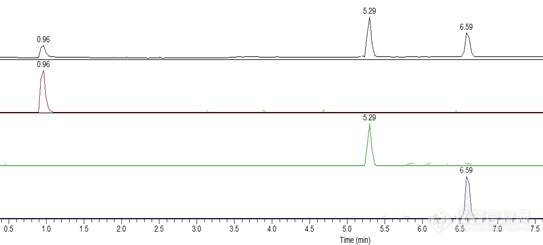
[align=center][b][font=黑体]建立液相质谱联用法测定生姜提取液中米诺地尔、度他雄胺与非那雄胺的含量方法[/font][/b][/align][align=center][font=楷体_GB2312]黄锦波[/font]1[font=楷体_GB2312],罗杰鸿[/font]2[/align][align=center](1.[font=宋体]吉姆斯(广州)实验技术有限公司;[/font]2.[font=宋体]广东安纳检测技术有限公司[/font][font=宋体]广州[/font] [url=http://www.cqvip.com/main/search.aspx?o=%e5%b9%bf%e5%b7%9e510520][color=windowtext]510000[/color][/url])[/align][align=left][b][font=黑体]摘要[/font]:[font=黑体]目的[/font][/b][font=宋体]建立液相串联质谱法测定生姜提取液中米诺地尔,度他雄胺与非那雄胺含量的方法。[/font][b][font=黑体]方法[/font][/b][font=宋体]样品经过乙腈溶解,超声[/font]15 min[font=宋体],再经过[/font]Oasis HLB[font=宋体]固相萃取柱净化,最终以甲醇洗脱并定容于[/font]10 ml[font=宋体]容量瓶。采用电喷雾离子源,全扫描模式,取适量样品上机测试。选择[/font]Extend-C18[font=宋体]为分离柱,[/font]90 %[font=宋体]甲醇[/font]-0.1 %[font=宋体]甲酸水为流动相。[/font][b][font=黑体]结果[/font][/b][font=宋体]米诺地尔,度他雄胺与非那雄胺的检出浓度分别为[/font]0.020mg/kg[font=宋体],[/font]0.019mg/kg[font=宋体],[/font]0.022 mg/kg[font=宋体],线性良好,[/font]R[sup]2[/sup][font=宋体]均大于[/font]0.995[font=宋体]。以空白样品为基质,回收率在[/font]89.0%-99.8%[font=宋体]之间,相对标准偏差在[/font]0.5-4.1 %[font=宋体]之间。[/font][b][font=黑体]结论[/font][/b][font=宋体]该方法的能[/font][/align][b][font=楷体]关键词[/font]:[/b] [font=宋体]液相串联质谱法;生姜提取液;米诺地尔;度他雄胺;非那雄胺;[/font][align=center][b][color=black]Determination ofthree prohibited hormones in hair cosmetics by LC-MS[/color][/b][/align][align=center][color=#2B2B2B]Huang Jin-bo 1[/color][font=黑体][color=#2B2B2B],[/color][/font][color=#2B2B2B]Luo Jie-hong2[/color][/align][align=center][color=#2B2B2B](1.Jims (Guangzhou) Experimental Technology Co., Ltd. 2. Guangdong Anna TestingTechnology Co., Ltd., Guangzhou 510000)[/color][/align][align=left][b][color=#2B2B2B]ABSTRACT: [/color][/b]Objective to establish a liquid phase tandem massspectrometry method for the determination of minoxidil, dutasteride andfinasteride in ginger extract. Methods The samples were dissolved inacetonitrile, sonicated for 15min, and then purified by Oasis HLB column.Finally, the samples were eluted with methanol and fixed in a 10 mlvolume-volume flask. Using electrospray ion source, full scan mode, takeappropriate samples on the machine test. Extend-c18 was selected as theseparation column, and 90 % methanol-0.1 % formic acid water was used as themobile phase. Results The detectable concentrations of minoxidil, dutasterideand finasteride were 0.020mg/kg, 0.019mg/kg and0.022mg/kg, respectively, withgood linearity and R[sup]2[/sup] greater than 0.995. Using blank sample assubstrate, the recoveries were 89.0%-99.8%and the relative standard deviationswere 0.5-4.1%. Conclusion This method can accurately analyze the contents ofthree prohibited hormones in ginger extract.[/align][b]Key words: [/b]LC-MSMS gingerextract Minoxidil Dutasteride finasteride [align=left][font=宋体]生姜提取液可通过刺激头皮血液,使得毛囊活跃,有助于毛发生长,减少脱发断发[/font][sup][1][/sup][font=宋体],往往被用作生发原料。米诺地尔或雄胺激素类激素可被用于治疗脱发症状,但根据《化妆品安全技术规范》([/font]2015[font=宋体]年版)中规定,米诺地尔或雄胺激素类激素禁止添加到日化用品中,若长期使用含有这三种激素的日化用品,很有可能导致头屑增多、皮肤瘙痒、脱发加剧等[/font][sup][2][/sup][font=宋体],因此需建立相关的检测方法,以监测相关的产品。[/font][/align][align=left][font=宋体]目前,检测米诺地尔,非那雄胺与度他雄胺的主要方法为液相色谱仪[/font][sup][3-4][/sup][font=宋体]、液相质谱联用法[/font][sup][5-6][/sup][font=宋体]。液相色谱仪在检测的过程中对分离条件要求高,不同基质的样品有可能需要开发不同的分离方法,同时容易出现假阳性。液相色谱[/font]-[font=宋体]串联质谱法,能同时检测几十种激素[/font][sup][7][/sup][font=宋体],这有利于缩短分析时间,有利于辨别假阳性,因此,在实际工作中,首选液相串联质谱测定激素。[/font][/align][align=left][font=宋体]目前质谱法测定米诺地尔与非那雄胺的检测方法相对较多[/font][sup][8-9][/sup][font=宋体],但是检测度他雄胺的检测方法较少,因此本实验通过优化前处理条件,色谱条件与质谱条件,建立了液相质谱联用测定生姜提取液中米诺地尔、度他雄胺与非那雄胺含量的方法。[/font][/align][align=left]1 [font=仿宋]试验[/font][/align][align=left]1.1 [font=黑体]仪器和试剂[/font][/align][align=left][font=宋体]赛默飞液相色谱质谱联用仪[/font]TSQ Quantum Ultra&Access MAX[font=宋体],吉姆斯[/font]ZY-1001[font=宋体]超声波清洗器、[/font]TDL-5A[font=宋体]台式离心机。[/font][/align][align=left][font=宋体]米诺地尔标准品(纯度为[/font]99.5 %[font=宋体])、非那雄胺标准品(纯度为[/font]99.7 %[font=宋体])、度他雄胺标准品(纯度为[/font]99.9 %[font=宋体])[/font]([font=宋体]均购于上海安谱实验科技有限公司[/font])[font=宋体]。[/font][/align][align=left][font=宋体]样品:市售[/font][/align][align=left][font=宋体]试剂:甲醇、乙醇、乙腈均为色谱纯,三氯甲烷为分析纯。[/font][/align][align=left][font=宋体]耗材:[/font]Oasis HLB[font=宋体]固相萃取小柱,[/font]Aisimo WAX[font=宋体]固相萃取小柱。[/font][/align][align=left]1.2 [font=黑体]溶液配制[/font][/align][align=left][font=仿宋]1.2.1 3[/font][font=仿宋]种激素的混合对照品储备液[/font][/align][align=left][font=宋体]分别称取米诺地尔、非那雄胺、度他雄胺对照品适量,用甲醇溶解并稀释成各组分质量浓度分别约为[/font]10μg/ml[font=宋体]的混合对照品储备液。[/font][/align][align=left][font=仿宋]1.2.2 3[/font][font=仿宋]种激素的系列混合标准工作溶液[/font][/align][align=left][font=宋体]精密[/font]3[font=宋体]种激素的混合对照品储备液[/font]0.01[font=宋体]、[/font]0.02[font=宋体]、[/font]0.04[font=宋体]、[/font]0.06[font=宋体]、[/font]0.08[font=宋体]、[/font]0.1ml [font=宋体],分别置于[/font]6[font=宋体]只[/font]10ml[font=宋体]棕色容量瓶中,用甲醇稀释至标线,配制成各组分质量浓度均分别为[/font]10[font=宋体]、[/font]20[font=宋体]、[/font]40[font=宋体]、[/font]20[font=宋体]、[/font]40[font=宋体]、[/font]60[font=宋体]、[/font]80[font=宋体]、[/font]100μg/l[font=宋体]的系列混合标准工作溶液,[/font][/align][align=left]1.3 [font=黑体]仪器工作条件[/font][/align][align=left]1[font=宋体])色谱条件[/font] [font=宋体]色谱柱:[/font]Extend-C18[font=宋体]色谱柱([/font]100mm×0.46 cm×0.25 μm[font=宋体]),柱温:[/font][font=宋体]35℃[/font][font=宋体];进样体积[/font]5μl[font=宋体];流速为[/font]0.2ml/min[font=宋体]。流动相[/font]A[font=宋体]为甲醇,流动相[/font]B[font=宋体]为[/font]0.1 %[font=宋体]甲酸水,等度洗脱,[/font]A:B=90 %:10 %[font=宋体]。[/font][/align][align=left]2[font=宋体])质谱条件[/font][font=宋体]电喷雾离子源([/font]ESI[sup]+[/sup][font=宋体]),全扫描模式([/font]scan[font=宋体]),碰撞气为氩气,雾化气为氮气,雾化室温度:[/font]350[font=宋体]℃[/font][font=宋体],接口温度为[/font]250[font=宋体]℃[/font][font=宋体],接口电压为[/font]3.5 kV[font=宋体],其余质谱参数见表[/font]1[font=宋体]。[/font][/align][align=left][font=黑体]表[/font]1 [font=黑体]质谱参数[/font][/align] [table][tr][td=1,2] [align=center][b][font=宋体]化合物[/font][/b][/align] [/td][td=3,1] [align=center][b][font=宋体]质荷比[/font][i]m/z[/i][/b][/align] [/td][td=1,2] [align=center][b][font=宋体]碰撞电压[/font]/V[/b][/align] [/td][/tr][tr][td] [align=center][b][font=宋体]分子量[/font][/b][/align] [/td][td] [align=center][b]M+H[sup]+[/sup][/b][/align] [/td][td] [align=center][b]M+Na[sup]+[/sup][/b][/align] [/td][/tr][tr][td] [align=center][font=宋体]米诺地尔[/font][/align] [/td][td] [align=center]209.2[/align] [/td][td] [align=center]210.2[/align] [/td][td] [align=center][color=black]/[/color][/align] [/td][td] [align=center]25[/align] [/td][/tr][tr][td] [align=center][font=宋体]非那雄胺[/font][/align] [/td][td] [align=center]372.5[/align] [/td][td] [align=center]373.4[/align] [/td][td] [align=center]395.3[/align] [/td][td] [align=center]30[/align] [/td][/tr][tr][td] [align=center][font=宋体]度他雄胺[/font][/align] [/td][td] [align=center]528.5[/align] [/td][td] [align=center]529.3[/align] [/td][td] [align=center][color=black]551.3[/color][/align] [/td][td] [align=center]22[/align] [/td][/tr][/table][align=left] [/align][align=left]1.4 [font=黑体]试验方法[/font][/align] [font=宋体]准确称取均匀的样品[/font]0.5 g[font=宋体]于[/font]10 ml[font=宋体]离心管中,加入[/font]3 ml[font=宋体]乙腈进行提取,振荡[/font]1 min[font=宋体],超声[/font]10 min[font=宋体]后,于[/font]5000 r/min[font=宋体]的离心机上进行离心,有机相经[/font]Oasis HLB[font=宋体]固相萃取小柱(提前分别以[/font]5 ml[font=宋体]甲醇,[/font]10ml[font=宋体]水活化)净化,待样品液体流尽后,以甲醇进行自然流下洗脱,最终以甲醇定容于[/font]10 ml[font=宋体]容量瓶中,供试品经过有机滤膜过滤后,上机待测。[/font][align=left] [/align][align=left]2 [font=仿宋]结果与讨论[/font][/align][align=left]2.1 [font=黑体]色谱行为[/font][/align][font=宋体]在优化的色谱条件下,[/font]3[font=宋体]种激素的混合标准溶液的色谱图见图[/font]1[align=center][sub][img=total-map 拷贝,362,163]https://ng1.17img.cn/bbsfiles/images/2022/12/202212151650413053_6906_3237657_3.jpg!w543x245.jpg[/img][/sub][/align][align=center][font=宋体]图[/font]1-1 3[font=宋体]种激素的总离子色谱图[/font][/align][align=center][img=mi-背景白色-离子,108,162]https://ng1.17img.cn/bbsfiles/images/2022/12/202212151650558752_9924_3237657_3.jpg!w162x243.jpg[/img] [img=fei-背影白色-离子,130,185]https://ng1.17img.cn/bbsfiles/images/2022/12/202212151651059044_5407_3237657_3.jpg!w195x277.jpg[/img] [img=du-背影白色-离子,91,195]https://ng1.17img.cn/bbsfiles/images/2022/12/202212151651141788_8226_3237657_3.jpg!w136x292.jpg[/img][/align][align=center][font=宋体]图[/font]1-2 [font=宋体]米诺地尔,非那雄胺与度他雄胺(从左到右)标准溶液的总离子色谱图与相关离子柱状图[/font][/align][b][font='Times New Roman',serif] [/font][font='Times New Roman',serif]2.2 [/font][font=黑体]仪器条件的优化[/font][/b][align=left][font=仿宋]2.2.1[/font][font=仿宋]流动相的选择[/font][/align][align=left][font=宋体]本试验以常见的甲醇[/font]-0.1 %[font=宋体]甲酸水作为流动相,分别设置[/font]10 %[font=宋体]甲醇[/font]-0.1 %[font=宋体]甲酸水,[/font]30 %[font=宋体]甲醇[/font]-0.1%[font=宋体]甲酸水、[/font]50 %[font=宋体]甲醇[/font]-0.1%[font=宋体]甲酸水、[/font]70 %[font=宋体]甲醇[/font]-0.1%[font=宋体]甲酸水,[/font]90 %[font=宋体]甲醇[/font]-0.1%[font=宋体]甲酸水进行测试,查看各个目标峰的响应值(响应值以同浓度下的峰面积大小判断)。结果发现,流动相的变化,对度他雄胺的响应值无明显影响,但有机相的占比越高,米诺地尔与非那雄胺的响应值越高,因此本试验的流动相采用[/font]90 %[font=宋体]的甲醇[/font]-0.1%[font=宋体]甲酸水。[/font][/align][align=left][font=仿宋]2.2.2 [/font][font=仿宋]质谱条件的优化[/font][/align][font=宋体]以[/font]0.1μg/ml[font=宋体]的混合标准溶液以注射进样的方式进行全扫描分析,通过优化雾化室温度、碰撞能量、毛细管电压等参数,得到[/font]3[font=宋体]种激素的最优分析条件。结果表明,这三种激素在正模式下响应更高。米诺地尔、非那雄胺、度他雄胺的最佳碰撞电压分别为[/font]25V[font=宋体]、[/font]30V[font=宋体]、[/font]22 V[font=宋体]。[/font]M+H[sup]+[/sup][font=宋体]分别为[/font]210.3[font=宋体]、[/font]373.4[font=宋体]、[/font]529.3[font=宋体]、[/font]551.3[font=宋体]。[/font][b][font='Times New Roman',serif]2.4 [/font][font=黑体]样品前处理条件的优化[/font][/b][align=left][font=仿宋]2.4.1[/font][font=仿宋]提取溶剂的选择[/font][/align][font=宋体]本试验以甲醇、乙醇、乙腈与三氯甲烷作为提取剂,分别考察不同提取剂对目标物的回收率影响。结果表明,这甲醇与乙醇对米诺地尔的回收率较低,而三氯甲烷对非那雄胺与度他雄胺的回收率相对偏高,而乙腈作为提取剂时,三个目标物的回收率均较好(如表[/font]2[font=宋体]所示),因此本实验选择的样品提取剂为乙腈。[/font][align=left] [/align][align=left] [/align][align=left][font=黑体]表[/font]2 [font=黑体]考察不同溶剂作为提取剂的回收率结果[/font][/align] [table][tr][td=1,2] [align=center][font=宋体]化合物[/font][/align] [/td][td=4,1] [align=center][font=宋体]米诺地尔加标量为[/font]0.10 μg[font=宋体]、非那雄胺加标量为[/font]0.10 μg[font=宋体]、与度他雄胺加标量为[/font]0.11 μg[/align] [/td][/tr][tr][td] [align=center][font=宋体]甲醇[/font][/align] [/td][td] [align=center][font=宋体]乙醇[/font][/align] [/td][td] [align=center][font=宋体]乙腈[/font][/align] [/td][td] [align=center][font=宋体]三氯甲烷[/font][/align] [/td][/tr][tr][td] [align=center][font=宋体]米诺地尔[/font][/align] [/td][td] [align=center][color=black]85.4 [/color]%[/align] [/td][td] [align=center]84.4 %[/align] [/td][td] [align=center][color=black]90.5 [/color]%[/align] [/td][td] [align=center]109.4 %[/align] [/td][/tr][tr][td] [align=center][font=宋体]非那雄胺[/font][/align] [/td][td] [align=center]92.5 %[/align] [/td][td] [align=center]91.4 %[/align] [/td][td] [align=center]92.5 %[/align] [/td][td] [align=center]105.4 %[/align] [/td][/tr][tr][td] [align=center][font=宋体]度他雄胺[/font][/align] [/td][td] [align=center][color=black]90.9 [/color]%[/align] [/td][td] [align=center]93.4 %[/align] [/td][td] [align=center][color=black]95.9 [/color]%[/align] [/td][td] [align=center]110.4 %[/align] [/td][/tr][/table][align=left][font=仿宋] [/font][/align][align=left][font=仿宋]2.4.2 [/font][font=仿宋]超声时间的确定[/font][/align][font=宋体]本实验设计超声[/font]1 min[font=宋体],[/font]5 min[font=宋体],[/font]10min[font=宋体],[/font]15 min[font=宋体],[/font]20 min,[font=宋体]与[/font]30min[font=宋体]进行对比实验,以一定浓度的质控样作为提取样品,参考[/font]1.3[font=宋体]的方法进行前处理,以回收率的高低作为判断的标准。结果发现,米诺地尔在超声[/font]10 min[font=宋体]内,回收率呈上升阶段,而[/font]10min[font=宋体]到[/font]15 min[font=宋体]内无明显的变化,大于[/font]15 min[font=宋体]后,有往下的趋势,而非那雄胺与度他雄胺在超声[/font]15 min[font=宋体]内,呈上升的阶段,而大于[/font]15 min[font=宋体]后,并无明显的变化。因此本试验,采用超声提取时间为[/font]15 min[font=宋体]。具体如图[/font]4-[font=宋体]图[/font]6[font=宋体]所示[/font][align=center][img=,305,115]https://ng1.17img.cn/bbsfiles/images/2022/12/202212151651368262_41_3237657_3.png!w457x172.jpg[/img][/align][align=center][font=黑体]图[/font] 4 [font=黑体]米诺地尔的超声提取时间与回收率的趋势图[/font][/align][align=left] [/align][align=center][img=,325,129]https://ng1.17img.cn/bbsfiles/images/2022/12/202212151651483537_5445_3237657_3.png!w487x193.jpg[/img][/align][align=center][font=黑体]图[/font] 5 [font=黑体]非那雄胺的超声提取时间与回收率的趋势图[/font][/align][align=center][img=,333,129]https://ng1.17img.cn/bbsfiles/images/2022/12/202212151651573213_2787_3237657_3.png!w499x193.jpg[/img][/align][align=center][font=黑体]图[/font] 6 [font=黑体]度他雄胺[/font][font=黑体]超声提取时间与回收率的趋势图[/font][/align][align=left][font=仿宋]2.4.3[/font][font=仿宋]净化条件的选择[/font][/align][font=宋体]本试验考察两种固相萃取柱对质控样中的目标物的净化能力,分别为[/font]Oasis HLB[font=宋体]固相萃取柱与[/font]Aisimo WAX[font=宋体]固相萃取柱,结果发现采用[/font]Aisimo WAX[font=宋体]固相萃取小柱进行净化时,三种目标物的回收率范围在[/font]58.4 %[font=宋体]至[/font]75.9 %[font=宋体]之间,而采用[/font]Oasis HLB[font=宋体]固相萃取柱时,回收率的范围在[/font]89.1 %[font=宋体]到[/font]96.4 %[font=宋体]之间,因此本实验选用[/font]Oasis HLB[font=宋体]固相萃取柱作为净化柱。[/font][b][font='Times New Roman',serif]2.5[/font][font=黑体]标准曲线与检出浓度[/font][/b][font=宋体]配制[/font]0.1[font=宋体],[/font]0.5[font=宋体],[/font]2.0[font=宋体],[/font]5.0[font=宋体],[/font]10.0[font=宋体],[/font]50.0[font=宋体],[/font]100 μg/l[font=宋体]的混合标准溶液系列,按优化后的色谱条件对其进行测定,以目标物的配置浓度为横坐标,峰面积为纵坐标。线性范围,回归方程与相关系数详见表[/font]3[font=宋体]。[/font][font=宋体]检出限以[/font]3[font=宋体]倍信噪比([/font]3S/N[font=宋体])时所对应的浓度计算、[/font][align=left][font=黑体]表[/font]3 3[font=黑体]种激素标准曲线考察结果[/font][/align] [table=569][tr][td] [align=center][font=宋体][color=black]峰号[/color][/font][/align] [/td][td] [align=center][font=宋体][color=black]目标物[/color][/font][/align] [/td][td] [align=center][font=宋体][color=black]线性范围([/color][/font][color=black]μg/l[/color][font=宋体][color=black])[/color][/font][/align] [/td][td] [align=center][font=宋体][color=black]线性回归方程[/color][/font][/align] [/td][td] [align=center][font=宋体][color=black]相关系数[/color][/font][/align] [/td][td] [align=center][font=宋体][color=black]检出限[/color][/font][color=black] (mg/kg)[/color][/align] [/td][/tr][tr][td] [align=center][color=black]1[/color][/align] [/td][td] [align=center][font=宋体][color=black]米诺地尔[/color][/font][/align] [/td][td] [align=center]10.05-100.5[/align] [/td][td] [align=center]Y =53460X-329[/align] [/td][td] [align=center]0.9998[/align] [/td][td] [align=center]0.020[/align] [/td][/tr][tr][td] [align=center][color=black]2[/color][/align] [/td][td] [align=center][font=宋体][color=black]非那雄胺[/color][/font][/align] [/td][td] [align=center]9.77-97.7[/align] [/td][td] [align=center]Y =99878X-1472[/align] [/td][td] [align=center]0.9999[/align] [/td][td] [align=center]0.019[/align] [/td][/tr][tr][td] [align=center][color=black]3[/color][/align] [/td][td] [align=center][font=宋体][color=black]度他雄胺[/color][/font][/align] [/td][td] [align=center]10.99-109.9[/align] [/td][td] [align=center]Y =43944X-3072[/align] [/td][td] [align=center]0.9994[/align] [/td][td] [align=center]0.022[/align] [/td][/tr][/table][b][font='Times New Roman',serif]2.6 [/font][font=黑体]回收试验与精密度[/font][/b][font=宋体]以不含的生姜提取液作为空白基质,分别对其添加低、中、高三个水平的混合标准溶液,每个水平测试[/font]6[font=宋体]次,回收率和测定值的相对标准偏差[/font](RSD)[font=宋体]见表[/font]4[font=宋体]。[/font][align=left][font=黑体]表[/font]4 [font=黑体]精密度和回收率实验结果([/font]n=6[font=黑体])[/font][/align] [table][tr][td=1,2] [align=center][font=宋体]化合物[/font][/align] [/td][td=2,1] [align=center][font=宋体]加标量[/font]0.02 μg[/align] [/td][td=2,1] [align=center][font=宋体]加标量[/font]0.04 μg[/align] [/td][td=2,1] [align=center][font=宋体]加标量[/font]0.2 μg[/align] [/td][/tr][tr][td] [align=center][font=宋体]回收率[/font]%[/align] [/td][td] [align=center]RSD %[/align] [/td][td] [align=center][font=宋体]回收率[/font] %[/align] [/td][td] [align=center]RSD %[/align] [/td][td] [align=center][font=宋体]回收率[/font] %[/align] [/td][td] [align=center]RSD %[/align] [/td][/tr][tr][td] [align=center][font=宋体][color=black]米诺地尔[/color][/font][/align] [/td][td] [align=center][color=black]92.8%[/color][/align] [/td][td] [align=center]4.1[/align] [/td][td] [align=center][color=black]92.7[/color][/align] [/td][td] [align=center]3.6[/align] [/td][td] [align=center][color=black]99.8[/color][/align] [/td][td] [align=center]1.3[/align] [/td][/tr][tr][td] [align=center][font=宋体][color=black]非那雄胺[/color][/font][/align] [/td][td] [align=center]89.0%[/align] [/td][td] [align=center]3.4[/align] [/td][td] [align=center]95.0[/align] [/td][td] [align=center]2.5[/align] [/td][td] [align=center][color=black]97.9[/color][/align] [/td][td] [align=center]0.5[/align] [/td][/tr][tr][td] [align=center][font=宋体][color=black]度他雄胺[/color][/font][/align] [/td][td] [align=center][color=black]90.4%[/color][/align] [/td][td] [align=center][color=black]3.9[/color][/align] [/td][td] [align=center][color=black]93.5[/color][/align] [/td][td] [align=center][color=black]3.1[/color][/align] [/td][td] [align=center][color=black]98.8[/color][/align] [/td][td] [align=center][color=black]2.6[/color][/align] [/td][/tr][/table][align=left]3 [font=仿宋]总结[/font][/align][font=宋体]本实验通过优化样品前处理与色谱仪器条件,探索出适合液相质谱法测定生姜提取液中[/font]3[font=宋体]种激素含量的检测方法,本实验方法具有较高的准确度和精密度,能准确的检测生姜提取液中米诺地尔,非那雄胺与度他雄胺含量。[/font][align=left][b][font=黑体]参考文献[/font][/b][/align][1] [font=宋体]高合意[/font],[font=宋体]黄健聪[/font],[font=宋体]等[/font].[font=宋体]复配植物防脱生发原料的制备与功效评价研究[/font][J].[font=宋体]日用化学工业[/font]. 2018,48(09)[font=宋体],[/font]521-526[2] [font=宋体]张朝辉[/font].[font=宋体]非那雄胺与米诺地尔治疗男性雄激素性秃发疗效分析[/font][J]. [font=宋体]临床研究[/font],2017,03(25):39-42.[3] [font=宋体]高媛[/font].HPLC[font=宋体]法测定米诺地尔洗剂含量及温度对含量影响的考察[/font][J]. [font=宋体]中国药师[/font],2018,07:1284-1286.[4] [font=宋体]刘亚雄[/font].[font=宋体]高效液相色谱法检测防脱、育发类化妆品中的非那雄胺[/font][J]. [font=宋体]日用化学工业[/font],2014,01:54-56.[5] [font=宋体]赵薇[/font],[font=宋体]等[/font]. [font=宋体]超高效液相色谱[/font]-[font=宋体]串联质谱法测定婴幼儿化妆品中米诺地尔等[/font]7[font=宋体]种成分[/font][J]. [font=宋体]食品安全质量检测学报[/font], 2019, 09: 2765-2770.[6] [font=宋体]许文佳[/font].HPLC-MS/MS[font=宋体]法同时测定生姜提取液中的[/font]13[font=宋体]种违禁成分[/font][J]. [font=宋体]药物分析杂志[/font],2019,08:1483-1488.[7] [font=宋体]郑磊[/font],[font=宋体]等[/font].[font=宋体]育发产品中斑蝥素和氮芥及米诺地尔的液相色谱[/font]-[font=宋体]串联质谱测定法[/font][J]. [font=宋体]环境与健康杂志[/font],2016,01[font=宋体]:[/font]66-68.[8] [font=宋体]吴川彦[/font],[font=宋体]等[/font].HPLC-Q-TOF-MS[font=宋体]法对米诺地尔及凝胶有关物质的分:中国药师[/font],2017,12:2267-2272.[9] [font=宋体]龚越强[/font].HPLC[font=宋体]测定中草药育发类化妆品中非法添加的米诺地尔[/font][J]. [font=宋体]食品与药品[/font],2014,04:267-269.
2024年1月8日,根据《化妆品监督管理条例》,国家药监局批准发布《化妆品中非那雄胺等10种组分的测定》化妆品补充检验方法。[align=center][img=2.png,600,247]https://img1.17img.cn/17img/images/202401/uepic/e4bb2749-7324-4c9f-873e-29cc7146c224.jpg[/img][/align]非那雄胺为一种4-氮杂甾体化合物,能有效地减少血液和前列腺内的二氢睾丸酮,用于治疗前列腺增生症。但是[b]妇女、儿童和对本品过敏者禁用非那雄胺。[/b]本标准的起草单位为上海市食品药品检验研究院起草,验证单位为山东省食品药品检验研究院、广东省药品检验所和江西省药品检验检测研究院。[b]本标准规定采用高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-三重四极杆质谱联用仪测定化妆品中羟基氟他胺、非那雄胺、尼鲁米特、比卡鲁胺、氟罗地尔、氟他胺、环丙孕酮、醋酸环丙孕酮、度他雄胺、依立雄胺的含量,适用于膏霜乳类、液体类(水、油)、凝胶类、蜡基类、粉剂类化妆品中非那雄胺等10种组分的定性和定量测定。[/b]详细检测方法详见附件。附件:[img]https://img1.17img.cn/17img/images/202101/pic/3961461f-2698-4217-8a94-55eaaa9d6966.gif[/img][url=https://img1.17img.cn/17img/files/202401/attachment/55d31a89-80c2-4d2f-bcd4-c385e1eb14c0.doc]《化妆品中非那雄胺等10种组分的测定》[/url][来源:仪器信息网] 未经授权不得转载[align=right][/align]
2009年的最后一天,来自上海市食品安全联席会议办公室的消息,让“三聚氰胺”的字眼再次拨动了公众的神经:一家位于上海的乳品有限公司因涉嫌生产、销售三聚氰胺超过国家标准的乳制品,被监管部门依法查处。此时已经距离发生在2008年9月的全国性的三聚氰胺事件一年有余,中国乳业已经全面复苏。由中经产业景气指数研究中心和国家统计局中国经济景气监测中心联合发布的数据显示,2009年前三季度,国内乳品产量累计高达1423万吨,同比增长3.42%,乳业产品销售率整体超过95%,行业景气指数为95.5点,距离最高点仅差4.5点。然而,这家名为上海熊猫乳品有限公司(下称“上海熊猫”)的企业却让外界再次感受到三聚氰胺幽灵飘荡的丝丝寒意。就在20多天前,位于陕西的金桥乳业有限公司也被查出5.25吨问题奶粉,其中11袋275公斤奶粉三聚氰胺超标。记者了解到,此次问题依然出现在奶源上,而且可能是使用了当年的遗留有毒奶源。业内专家王丁棉介绍,一批当时处于生产与终端之间的中间领域的问题奶粉并没有被给予足够的监管,这令人对此次事态的范围是否会进一步扩大抱有疑虑。据本报记者了解,对于上海熊猫乳品问题的查处,早在2009年4月已经进行,但在之后长达8个月的时间内,一直处于对公众“保密”状态。对于,此前负责调查此事的上海市质量技术监督局宣传部人士表示,一切情况说明,均要以此前政府的新闻稿为参考。但记者在新闻稿中也并未看到对于延迟通知的任何解释。在熊猫乳品被曝光的第二天,也是2010年新年的第一天,全国许多手机用户都收到了一条来自三鹿等22家奶制品责任企业对问题奶粉事件的道歉短信。短信中写道:“决心以此为戒,杜绝不合格产品,诚恳接受社会监督。”行业乱局重新抬头无论是上海熊猫还是陕西金桥,被查出的问题产品,均是使用了此前被查出含有三聚氰胺的奶源所致。根据陕西方面公布的信息,金桥乳业的问题奶源来自在2008年10月复检时,将不合格样品偷梁换柱后,一直存放在库房中,并在去年再度拿出使用。而上海熊猫也是使用回收炼乳,但来源不明。“这说明在2008年三聚氰胺事件之后,对于一大批流通在市场上的问题产品的监控仍存在空白。”王丁棉告诉记者,早在去年6月,曾有一饲料商向他透露,自己从一奶粉经销商手中购买了六七万吨三聚氰胺严重超标的奶粉,准备用作饲料。当时,王丁棉给他的警告是,“小心坐牢”。在王丁棉看来,政府有关部门对于一批当时处于生产与终端之间的中间领域的问题奶粉并没有给予足够的监管,包括问题产品从企业售出后,卖给了谁,并没有真正跟进落实下去。而这一空白,也直接导致了金桥和上海熊猫事件的发生。事实上,在2008年的三聚氰胺事件中,曾被公众所质疑的一个地方在于,回收的近万吨的三鹿奶粉如何销毁、销毁途径,大部分没有完全公开的信息。也有多位网友发帖询问,三鹿之外的涉嫌三聚氰胺的乳品企业,为何听到的是召回信息,却惟独没有销毁公告。此前,包括王丁棉在内的业内人士的另一个担忧是,目前紧俏的奶源问题不得到解决,也势必影响未来乳业的安全。乳业的复苏、企业的扩建,正带动对于奶源新一轮的争夺。事实上,上海熊猫与陕西金桥事发于中国奶业整体复苏之际,或非偶然,“一旦竞争加剧,奶源重新紧俏缺,就容易有企业铤而走险。尤其是不掌握奶源的小企业。”王丁棉忧心忡忡,“这种状况下,最不能大意的就是质量检测。奶源一旦紧缺,就会加水,或者添加其他什么物质;另一方面,企业因为抢奶,则可能会对产品的质量尺度放宽。”8个月前的案件而上海熊猫事件另一疑问是,为何政府部门在查处了8个月之后,才把情况通报给公众?有上海当地的业内人士向记者透露,一些行业内人士其实也在此前就知道了这一事件,但是被告知要“保密”,“不能说”。对于原因,他仅表示,“目前乳业恢复形势很好”。在去年年底案件公开之前,上海熊猫乳品已在系统内被几次点名,但外界所知寥寥。而最先给予极大关注的,乃是一家名为浙江熊猫乳品有限公司(下称“浙江熊猫”)的企业。两家企业均为乳品生产企业,且名称相同,仅是所在地有所不同。浙江熊猫一位负责人告诉记者,公司早在去年4月底就在国家质检总局的一份杂志中看到了这一消息,但并未引起多大注意。去年11月26日,全国食品安全整顿工作办公室主任、卫生部部长陈竺在电视电话会议上表示,对于顶风作案、屡教不改的食品生产经营者,一定要重拳打击,严厉处罚,并在会议上特别点到了“公安部挂牌督办了上海‘熊猫’炼乳使用含三聚氰胺原料案”。陈竺的“点名”,让浙江熊猫感到不安,于是,他们“赶紧出了一个律师声明给经销商”。上述浙江熊猫人士口中的杂志消息,实质乃是国家质检总局在2009年4月29日下发给各省、自治区、直辖市等地质监局的《关于上海质监局查处上海熊猫乳品有限公司违法生产伪劣乳制品情况的通报》(国质检执函【2009】201号,下称“《通报》”)。根据记者获得的这份《通报》,上海市质监局在4月23日,发现了“上海熊猫乳品有限公司生产的少数批次中老年高钙奶粉(标称生产日期2009年4月1日)、含乳调味品和原料中三聚氰胺含量超过临时管理限量值规定”。《通报》同时表示,上海质监局在当时随即按照市政府的指示会同有关部门对该企业全面进行检查,并发现了其使用回收的炼乳作为生产原料的恶劣情况。此后,上海市质监局已责令上海熊猫乳品停止生产,封存了所有的问题成品和原料,并组织力量查清问题成品流向、全力组织召回工作。而上海市公安机关已对涉案人员立案侦察。据悉,目前上海熊猫乳品的食品卫生许可证、食品生产许可证和营业执照已被吊销,公司法人代表、总经理及副总经理等3名犯罪嫌疑人已被依法起诉。“现在处于公诉阶段。”上海市质监局宣传部方面告诉记者。问题企业起底元旦前的案件披露,让浙江熊猫再次遭遇误会。一个重要原因是,浙江熊猫的名气远大于上海熊猫。资料显示, 浙江熊猫是中国规模最大的炼乳生产企业,位居同行业第一。浙江熊猫方面的人士告诉记者,在发布法律声明之前,公司已经对上海熊猫的情况做过调查。上海熊猫为原籍在温州苍南的几个自然人股东投资组建,其注册地在上海奉贤区,为独立法人。上海熊猫乳品有限公司原名为上海宝熊乳品有限公司,后经四川省一家企业授权、许可使用了“熊猫”字号(该企业注册了奶粉类的“熊猫”牌商标),更名为上海熊猫乳品有限公司。而浙江熊猫为浙江省粮油食品进出口股份有限公司控股投资组建的有限责任公司,其公司字号“熊猫”来源于浙江省粮油食品进出口股份有限公司授权许可的注册商标“熊猫”牌(注:该商标注册产品范围:炼乳等)。“浙江熊猫公司和上海熊猫公司为不同的投资主体在不同的地区组建的有限责任公司,均为独立的企业法人,两者之间没有任何的投资或产权的法律关系。”据记者了解到的情况显示,上海熊猫由温州人王岳超在2001年创立,王岳超是大股东,其他的3名股东均是他的亲戚。王曾自称自己从事乳品生产经营有10多年,在来上海前,他在温州即生产乳品。上海熊猫与三聚氰胺的瓜葛,在2008年9月三聚氰胺事件中已经展现。在那年9月16日晚上,中央电视台《新闻联播》公布了国家质监总局对全国婴幼儿奶粉生产企业的491批次产品的紧急专项检查结果,有22家企业69批次产品检出三聚氰胺,上海熊猫生产的“熊猫可宝牌”婴幼儿配方奶粉抽查了5件,有3件不合格,其三聚氰胺的最高含量达到619.00毫克/公斤,仅次于三鹿牌婴幼儿配方奶粉(三聚氰胺最高含量2563.00毫克/公斤)。记者联系到转让商标的四川雅安熊猫乳业有限公司,其一位工作人员告诉记者,公司在1999年初将自己所拥有的“熊猫”商标使用权转让给了上海熊猫,允许其生产“熊猫”品牌的奶粉。不过,这一商标使用权为十年,在2009年1月2日已经过期了。





 400-827-8618
400-827-8618
 留言咨询
留言咨询

 400-860-5168转0843
400-860-5168转0843
 留言咨询
留言咨询

 400-860-5586
400-860-5586
 留言咨询
留言咨询


