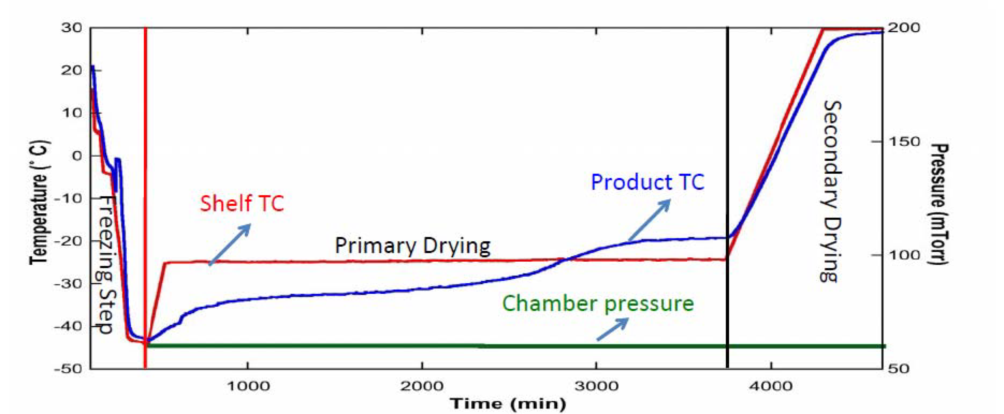
“蛋白样品冻干过程”干货分享!——深度解析相分离现象及影响因素
冻干可以通过去除样品中的水分,限制分子的流动性,减慢药物成分的物理/化学反应来延长产品的保质期,然而固体状态的配方也不是一直稳定的,由于在干燥过程中,蛋白质暴露在许多应力作用下,在长期的储存过程中,仍然容易发生物理/化学反应。在冻干及储存过程中,我们常常会加入一些稳定剂来保护蛋白免受应力的影响,主要有两种稳定机理来解释:水替代假说和玻璃化假说;但是两种稳定机制都需要将蛋白质分子分散在稳定剂中,使得蛋白质和稳定剂都处于相同的单一无定形相,即不发生相分离。那么相分离是如何发生的?为什么会发生?相分离主要发生在冻干的预冻步骤,在一定程度上取决于冻干的工艺和配方成分。1、相分离的机理 图1:冻干分为三个步骤冻干主要分为三个步骤:预冻,主干燥及次级干燥。(如图1所示)在预冻过程中,溶液被降到一个很低的温度,晶核形成并且生长,样品中的溶质浓度不断浓缩,可以达到初始浓度的约50倍,如果在热力学和动力学上均利于反应发生的条件下,高浓度的溶质可以导致相分离。2、相分离热力学当溶液为成分A 和成分B的混合物,会发生下面的相互作用(如图2所示)。熵和焓之间的竞争决定了相分离的过程。相分离的热力学基于混合物的自由能(弗洛里-哈金斯理论),聚合物由于尺寸大小和连通性,不能充分利用可用体积,大分子量聚合物的熵变化较小,因此,混合物热力学更容易受到较大焓贡献的支配,当ΔGmix 0: 热力学上有利于相分离 (A-A和B-B相互作用优于A-B相互作用)。 图2:溶液A和B发生的相互作用如果相分离是热力学自发以及动力学上利于反应(足够的移动性和时间),蛋白和稳定剂会分离成两个不同的相,富含稳定剂的无定形相以及富含蛋白的无定形相,后者由于缺乏稳定剂的保护,蛋白更易于降解。(如图3所示)图3:蛋白和稳定剂会分离成两个不同的相3、相分离的检测方法无定形-无定形物质的相分离不容易检测,由于检测方法有限,证据不足,目前主要有如下检测方法:检测技术方法局限性调制DSC配方中有多个Tg’表示有多个无定形相通常,富含蛋白的相不能被DSC检测到,因为在Tg’温度下具有较小的ΔCP;要求高浓度的蛋白配方。拉曼成像技术非重叠成分峰的线谱分析范围:2-50微米;不能检出低于检测限的成分波动。固体核磁共振利用弛豫时间来探测2-5 nm, 20-50 nm分子大小物质的混溶性动态实验需要大量的样品。X射线衍射/散射在纳米尺度上探测结构特征对于两个组分,均包含重要的结构层次,无法区分相分离;成本高,动态实验。SEM肉眼观察物质的形态结果会存在模棱两可的现象;需要较大的容易辨认的相。电介质技术依赖于电场中的分子迁移率响应存在不确定性。4、工艺参数对相分离的影响过冷度-----成核温度❖热力学冻结温度和首次成核温度之间的差值为过冷度;(如图4所示)❖较高的成核温度会更易导致相分离;(由于溶质在远高于Tg’温度下进行浓缩) 图4:过冷度冷却速度❖控制达到给定过冷度的速度;❖缓慢的冻结速度会更容易导致相分离;退火❖主要用于填充剂结晶,控制冰晶形态或增加冰晶体的大小,缩短一次干燥时间;❖如果两相热力学更稳定,退火时间和迁移率的增加可能会提供相分离的机会;灌装体积❖较大的灌装体积会对相分离有较大的影响,因为在样品中具有较大的热梯度。案例分享成核温度和冷却速度对相分离的影响对已知的相分离聚合物体系 1:1 PVP29K:DEX10K(100 mg/ml) 进行研究,将冷却台放在拉曼显微镜下进行观察。(如图5所示) 图5:已知相分离聚合物体系在拉曼显微镜下的观察成核温度对相分离的影响 图6:成核温度对相分离的影响与每个单一组分相比,成核温度较高的一组(-5℃)对相分离具有较大的影响;其余的成核温度对相分离影响较小。(如图6所示)冷却速度对相分离的影响 图7:冷却速度对相分离的影响所有的冷却速度均会在一定程度上提高相分离的倾向,但是影响较小。(如图7所示)*结论在没有热历史的情况下,成核温度和冷却速率对相分离的影响较小。成核温度和灌装体积对相分离的影响 图8:成核温度和灌装体积对相分离的影响较大的灌装体积(1ml VS 0.2ml)和较高的成核温度(-5℃ VS -10 ℃)会导致相分离,可能是由于样品内部存在较大的温度梯度。(如图8所示)5、配方成分对相分离的影响在冻干过程中配方成分的兼容性是阻止相分离的关键,如研究表明聚合物体系的不混溶性随着聚合物分子量的增加而增加。对于蛋白而言,相分离的倾向性可能与稳定剂大小,静电相互作用(盐类),稳定剂类型(填充剂、表面活性剂),稳定剂浓度,蛋白质特性(等电点,大小),配方PH值等有关。案例分享——配方组分对相分离的影响❖实验进行了系统的研究,探索蛋白质:糖的比例以及蛋白质(分子量,电荷)和糖(分子量,单糖亚基和长度)的特性如何影响配方在冻干过程中的混溶性。(如图9,10,11所示)❖蛋白质和糖(200mg /mL)的混合物按以下比例(w:w):蛋白质:糖——0:1,1:9,1:4,1:2.3,1:1.5,1:1,1:5:1,2.3:1,4:1,9:1❖多个Tg’的存在表明存在相分离。 图9 图10 图11实验表明● 在所有的蛋白-糖体系均观察到了相分离现象(两个不同的Tg’),尽管不同的比例出现相分离的时间不同;● 不同蛋白-糖混合物Tg’的宽度不同,有可能多个Tg’会重叠在一起,形成一个较宽的Tg’, 导致无法检测到相分离现象;● 其中在牛血清蛋白和海藻糖混合物中,当二者比例为1:1.5和1:1 时,观察到存在相分离现象;(如图12所示) 图12● 对于蛋白-糖体系中,二者比例从1:2.3 到4:1 均观察到存在相分离现象;(如图13所示)图13结论● 对于几乎所有被研究的体系中,当配方中蛋白质和糖的比例为1:1和1.5:1时确定会发生相分离现象,这表明蛋白质和糖的比例和系统的相分离倾向之间可能存在相关性;● 在系统的相分离趋势和以下属性之间似乎没有明显的相关性: # 蛋白质电荷/等电点 # 蛋白质分子量 # 糖的分子量 # 单糖亚基;● 在几乎所有研究的配方中,当蛋白和糖的比例为1:1时会发生相分离;● 本研究结果表明,冻干蛋白配方中应加入过量的稳定剂。6、冻干蛋白配方中相分离的重要性● 相分离取决于具体的操作过程和组分;● 在预冻过程中,温度/时间和浓度是关键因素,会影响系统相分离的趋势;● 蛋白和稳定剂的物理化学特性会影响相分离;● 在冻干过程中保护不足会导致长期储藏过程中不稳定性的增加;● 当缺乏稳定剂时,蛋白在干燥过程中会发生改变(即形成反应型结构),这可能会导致储存过程中潜在的稳定性问题;● 需要了解相分离如何影响冻干制剂的保质期;● 相分离检测是稳定性欠佳的指标;● 未检测到的相分离会影响蛋白质稳定性和整体产品质量;● 需要更好的检测方法!当前的方法可以证明样品存在相分离,但不能证明样品不存在相分离。参考文献[1] Padilla,A.M.et.Al.(2011).”The Study of Phase Separation in a Model Polymer Phase Separating System Using Raman Microscopy and a Low-Temperature Stage: Effect of Cooling Rate and



 400-628-5299
400-628-5299
 留言咨询
留言咨询

 400-805-0826
400-805-0826
 留言咨询
留言咨询

 留言咨询
留言咨询