方案详情文
智能文字提取功能测试中
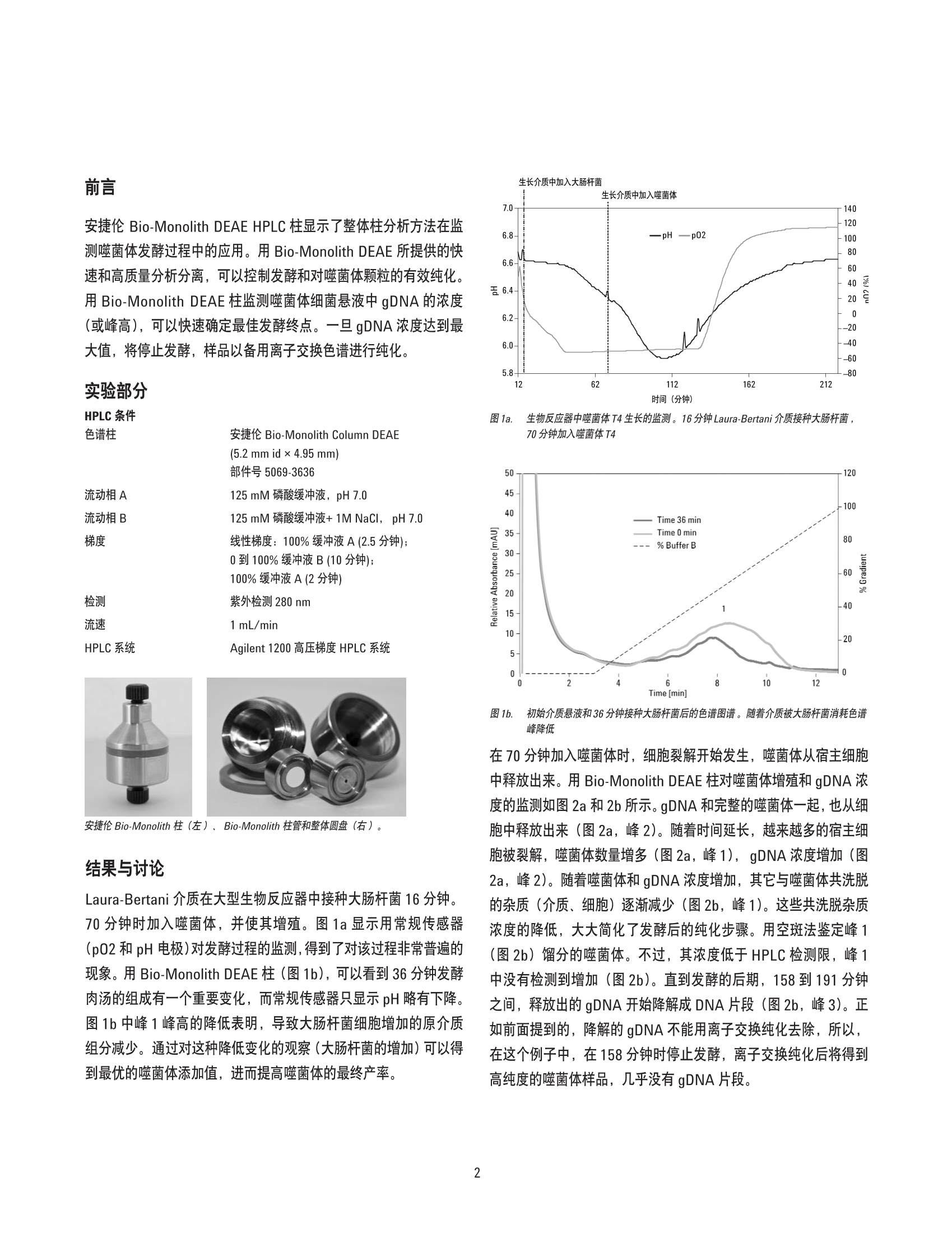
用安捷伦 Bio-Monolith HPLC 柱快速监测噬菌体生产 应用报告生物制药 作者 摘要 Franci Smrekar、 Ales Podgornik、Mateja Ciringer 和 Lidija Urbas BIA Separations Teslova 30 SI-1000 卢布尔雅那 斯洛文尼亚 Peter Raspor 卢布尔雅那大学,生物技术学院, 食品科学与技术系 20世纪初发现的噬菌体是一类侵害细菌的病毒。现在,噬菌体已被作为抗菌制剂,用于噬菌体展示筛选、噬菌体载体开发,作为目标基因治疗的传递系统,以及用于特殊类细菌分型等。为了在这些应用中使用噬菌体,通常要用液相色谱进行纯化,去除所有杂质。最近开发了一种使用离子交交整体柱的纯化和浓缩工艺[1]。宿主细胞增殖和裂解后,噬菌体从其生长介质中释放出来。其它宿主成分和这些噬菌体一起,也释放到生长介质中,其中就有会带来问题的宿主基因组 DNA(gDNA), 因为它不久将降解成更小的片段。用离子交换色谱纯化噬菌体时,至关重要的是包含噬菌体的介质中不能含任何 DNA 片段。游离 DNA 片段可能干扰体外噬菌体应用,噬菌体展示和细菌分型,可以给治疗噬菌体应用、载体生产和基因传递带来毒性。安捷伦 Bio-Monolith DEAE 柱(弱阴离子交换)可用于检测发酵过程,并评价整个纯化工艺中降解 gDNA 的量。 Jamnikarjeva 101 SI-1000 卢布尔雅那 斯洛文尼亚 Taegen Clary 安捷伦科技公司 5301 Stevens Creek Blvd. Santa Clara, CA 95052 USA Agilent Technologies 前言 安捷伦 Bio-Monolith DEAE HPLC 柱显示了整体柱分析方法在监测噬菌体发酵过程中的程用。用 Bio-Monolith DEAE 所提供的快速和高质量分析分离,可以控制发酵和对噬菌体颗粒的有效纯化。用 Bio-Monolith DEAE 柱监测噬菌体细菌悬液中 gDNA 的浓度(或峰高),可以快速确定最佳发酵终点。一旦gDNA 浓度达到最大值,将停止发酵,样品以备用离子交换色谱进行纯化。 实验部分 HPLC 系统 Agilent 1200 高压梯度 HPLC系统 安捷伦 Bio-Monolith柱(左)、Bio-Monolith 柱管和整体圆盘(右)。 结果与讨论 Laura-Bertani 介质在大型生物反应器中接种大肠杆菌16分钟。70分钟时加入噬菌体,并使其增殖。图1a显示用常规传感器(p02和pH电极)对发酵过程的监测,得到了对该过程非常普遍的现象。用 Bio-Monolith DEAE 柱(图1b),可以看到36分钟发酒肉汤的组成有一个重要变化,而常规传感器器显示pH略有下降。图1b中峰1峰高的降低表明,导致大肠杆菌细胞增加的原介质组分减少。通过对这种降低变化的观察(大肠杆菌的增加)可以得到最优的噬菌体添加值,进而提高噬菌体的最终产率。 生长介质中加入大肠杆菌 图1a. 生物反应器中噬菌体T4生长的监测。16分钟Laura-Bertani介质接种大肠杆菌,70分钟加入噬菌体 T4 图1b. 初始介质悬液和36分钟接种大肠杆菌后的色谱图谱。随着介质被大肠杆菌消耗色谱峰降低 在70分钟加入噬菌体时,细胞裂解开始发生,噬菌体从宿主细胞中释放出来。用 Bio-Monolith DEAE 柱对噬菌体增殖和 gDNA浓度的监测如图 2a和2b所示。gDNA 和完整的噬菌体一起,也从细胞中释放出来(图2a,峰2)。随着时间延长,越来越多的宿主细胞被裂解,噬菌体数量增多(图2a,峰1), gDNA浓度增加(图2a, 峰2)。随着噬菌体和gDNA浓度增加,其它与噬菌体共洗脱的杂质(介质、细胞)逐渐减少(图2b,峰1)。这些共洗脱杂质浓度的降低,大大简化了发酵后的纯化步骤。用空斑法鉴定峰1(图2b)馏分的噬菌体。不过,其浓度低于 HPLC检测限,峰1中没有检测到增加(图2b)。直到发酵的后期,158到191分钟之间,释放出的 gDNA 开始降解成 DNA 片段(图2b,峰3)。正如前面提到的,降解的 gDNA 不能用离子交换纯化去除,所以,在这个例子中,在158分钟时停止发酵,离子交换纯化后将得到高纯度的噬菌体样品,几乎没有 gDNA 片段。 图2a. 色谱峰代表噬菌体、细胞和介质悬液(1)和gDNA (2) 结论 安捷伦 Bio-Monolith DEAE 柱可以有效地用于监测发酵过程中的噬菌体增殖。根据用该色谱柱监测得到的结果,可以在噬菌体纯化的最佳点终止发酵。该方法可以用于发酵工艺的前期开发和后期的监测与质量控制。 ( 参考文献 ) 1. F. Smrekar, M. Ciringer, M. Peterka, A. Podgornik, andA. Strancar, J. Chromatogr. B, 861(2008) 177-180 更多信息 如需了解我们产品和服务的更多信息,请访问我们的网站www.agilent.com/chem/cn。 www.agilent.com/chem/cn 安捷伦对本资料中出现的错误,以及由于提供或使用本资料所造成的相关损失不承担责任。 本资料中涉及的信息、描述和规格,如有变更,恕不另行通告。 C安捷伦科技公司,2007年 2009年1月12日中国印刷 5990-3247CHCN Agilent Technologies 20 世纪初发现的噬菌体是一类侵害细菌的病毒。现在,噬菌体已被作为抗菌制剂,用于噬菌体展示筛选、噬菌体载体开发,作为目标基因治疗的传递系统,以及用于特殊类细菌分型等。为了在这些应用中使用噬菌体,通常要用液相色谱进行纯化,去除所有杂质。最近开发了一种使用离子交换整体柱的纯化和浓缩工艺。宿主细胞增殖和裂解后,噬菌体从其生长介质中释放出来。其它宿主成分和这些噬菌体一起,也释放到生长介质中,其中就有会带来问题的宿主基因组DNA(gDNA),因为它不久将降解成更小的片段。用离子交换色谱纯化噬菌体时,至关重要的是包含噬菌体的介质中不能含任何DNA 片段。游离DNA 片段可能干扰体外噬菌体应用,噬菌体展示和细菌分型,可以给治疗噬菌体应用、载体生产和基因传递带来毒性。安捷伦Bio-Monolith DEAE 柱(弱阴离子交换)可用于检测发酵过程,并评价整个纯化工艺中降解gDNA 的量。
关闭-
1/4

-
2/4
还剩2页未读,是否继续阅读?
继续免费阅读全文产品配置单
安捷伦科技(中国)有限公司为您提供《噬菌体细菌悬液中gDNA检测方案(液相色谱仪)》,该方案主要用于体外诊断类生物药品中含量测定检测,参考标准《暂无》,《噬菌体细菌悬液中gDNA检测方案(液相色谱仪)》用到的仪器有Agilent 1290 Infinity II 液相色谱系统、Agilent 1290 Infinity II Multisampler。
我要纠错
推荐专场
相关方案










 咨询
咨询


