方案详情文
智能文字提取功能测试中
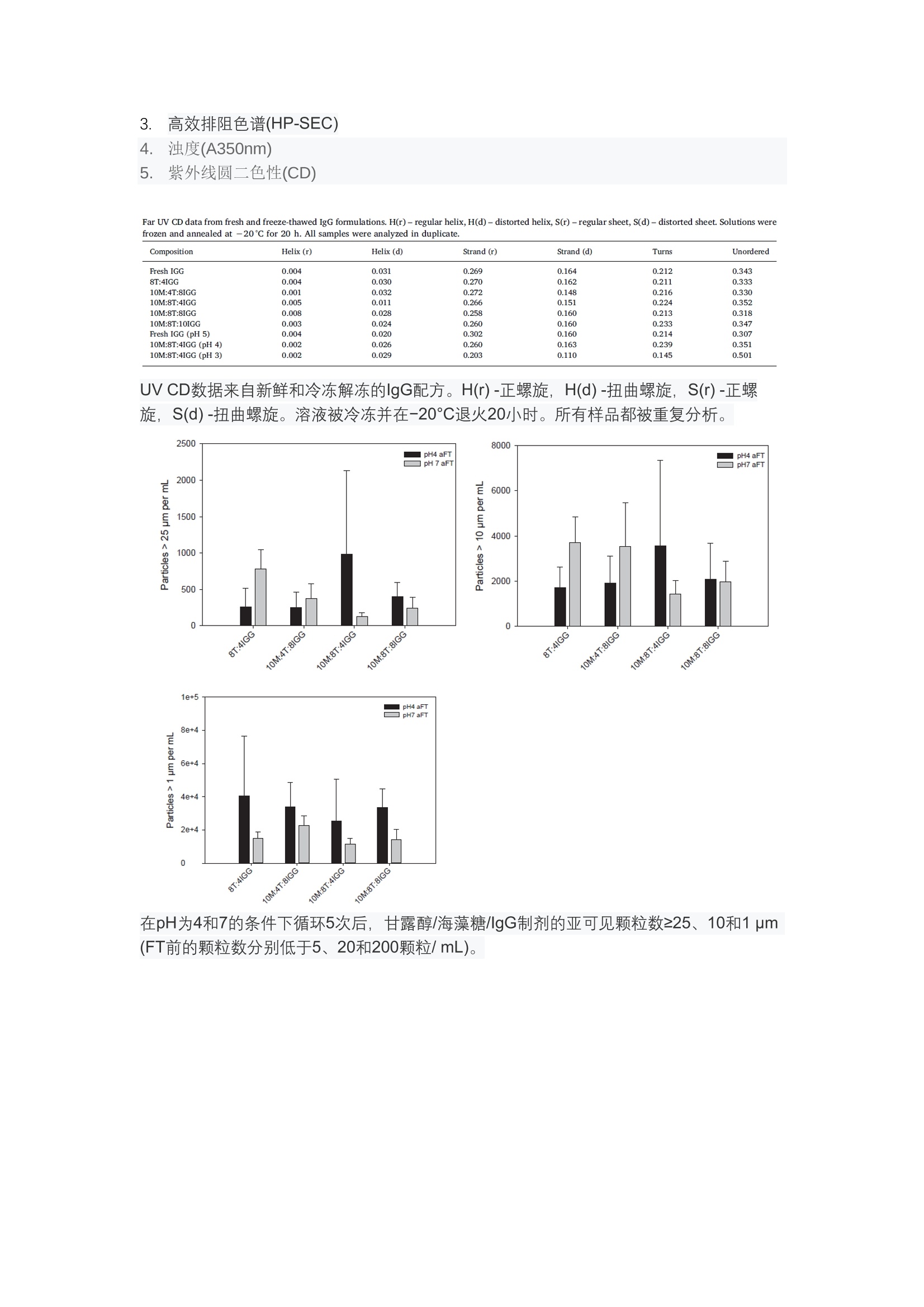
IGG 溶液冻融实验 引言 本研究探讨了甘露醇和海藻糖结晶对单克隆抗体IgG1在不同pH条件下反复冻融状态下的影响。配方在-20℃下退火20小时5次(通过冻融中断)。这样做是为了诱导赋形剂结晶。冻融样品的特征是通过圆形二色、颗粒分析和尺寸排除色谱进行的。在pH为3时,观察到不溶性和可溶性聚集物的形成,但这些可以通过使用表面活性剂来减少。不含冷冻保护剂的配方在冷冻/解冻后单体含量更高。在pH值为5的情况下,单个冻融循环不会导致颗粒数量的显著增加。在pH值为4-7的条件下,经过5次冻融循环后,在1-25pm的粒径范围内均有团 介绍 在冷冻状态储存和冻干的蛋白质配方中,冷冻步骤是关键,因为它决定了蛋白质的稳定性。很好地表明,在稳定的配方中,像甘露醇这样的膨化剂会结晶,而在冷冻和储存过程中,如海藻糖这样的低温防护剂应该保持无定形。增殖剂和冷冻的结晶作用取决于它们的相对浓度以及在配方中蛋白质的浓度。例如,在配方中,一种更高的牛血清白蛋白(BSA)浓度会抑制,甚至完全抑制结晶。其他添加剂,如表面活性剂,也会影响蛋白质的稳定性。目前还不知道,如果所有蛋白质对配方的状态有类似的影响,在冷冻过程中表现得类似。在本研究中,通过改变对甘露醇比的不同配方,探讨了单克隆IgG1抗体的冷冻反应。由于pH值对抗体稳定性的影响,pH值的影响也参与到了研究。该研究的关键参数是抗体的形成、聚集和颗粒的形成,以及冻融后配方的宏观外观。 材料 D-(+)-海藻糖二水合物(MW 378.33 kDa,99.9%纯度, Sigma-Aldrich, St. Louis, MO),Tween 20 (MW 1227.54 Da, >98.0%纯度, Biorad Laboratories, Hercules, CA),和D-甘露醇(MW 182.17 Da,298%纯度, Sigma-Aldrich)。原液在10mM磷酸钠缓冲液中按重量法配制pH(梅特勒- toledo MP220 pH计, Greifensee, 瑞士)。以单克隆抗体(IgG1)作为模型蛋白。所有配方在使用前均通过0.2 pm聚醚砜膜注射器过滤器(VWR InternationalGmbH, Ismaning, Germany)过滤。 冻融实验 冻融实验使用FTS LyoStarTM3冻干机(SP Scientific, Stone Ridge, NY, USA)进行。2R小瓶(FiolaxTMclear, MGlas AG, Munnerstadt, 德国)填充2.0mL样品溶液和塞(塞类型:WestarQ, West Pharmaceutical Services, Eschweiler, 德国)。将架子温度提高到-20℃(1℃/min),然后等温保存20h,以冷却样品。在-20℃保存20h, 我们假设完全冰结晶,任何非晶相的流动性和海藻糖的结晶都是有利的。将架子温度提高到20℃, 以1°C/min解冻样品。在选定的小瓶中通过热电偶监测产品温度。冻融循环最多重复五次。 检测方法 1..流式颗粒成像分析法 (FIA) FlowCAMQ8000系列成像仪(Fluid Imaging Technologies, Yarmouth, ME USA)配备了高分辨率相机(1920×1200像素, 10倍放大),用于可视化和计数每毫升样品的亚可见颗粒。样品体积为0.20mL, 流速为0.15 mL/min。系统在测量之间用纯净水冲洗,或用HelmanexQ去除流池中的残留蛋白。使用VisualSpreadsheet@软件进行数据分析。 2.光阻法(LO) 3. 高效排阻色谱(HP-SEC) 4. 浊度(A350nm) 5.紫外线圆二色性(CD) Far UV CD data from fresh and freeze-thawed IgG formulations. H(r)-regular helix,H(d)-distorted helix, S(r)-regular sheet, S(d)- distorted sheet. Solutions werefrozen and annealed at -20℃ for 20 h. All samples were analyzed in duplicate. Composition Helix (r) Helix (d) Strand (r) Strand(d) Turns Unordered Fresh IGG 0.004 0.031 0.269 0.164 0.212 0.343 8T:4IGG 0.004 0.030 0.270 0.162 0.211 0.333 10M:4T:8IGG 0.001 0.032 0.272 0.148 0.216 0.330 10M:8T:4IGG 0.005 0.011 0.266 0.151 0.224 0.352 10M:8T:8IGG 0.008 0.028 0.258 0.160 0.213 0.318 10M:8T:10IGG 0.003 0.024 0.260 0.160 0.233 0.347 Fresh IGG (pH 5) 0.004 0.020 0.302 0.160 0.214 0.307 10M:8T:4IGG (pH 4) 0.002 0.026 0.260 0.163 0.239 0.351 10M:8T:4IGG (pH 3) 0.002 0.029 0.203 0.110 0.145 0.501 UV CD数据来自新鲜和冷冻解冻的lgG配方。H(r)-正螺旋, H(d)-扭曲螺旋, S(r)-正螺旋, S(d)-扭曲螺旋。溶液被冷冻并在-20℃退火20小时。所有样品都被重复分析。 在pH为4和7的条件下循环5次后,甘露醇/海藻糖/lgG制剂的亚可见颗粒数≥25、10和1 um(FT前的颗粒数分别低于5、20和200颗粒/mL)。 经过5次FT循环后,配方和pH值4(上一行)和pH值7(下一行)的外观。 +4%IGG 经过5次FT循环后, pH为3的配方的外观(上排)和0.1%的ps20(下排)。 在pH为3的条件下,在不添加或添加0.1%PS20的情况下,5次FT循环后,亚可见颗粒数≥25、20和1 pm。 结论 在pH为3的条件下,在不添加或添加0.1%PS20的情况下,5次FT循环后,可溶性团聚体和单体含量增加。 溶液中的颗粒数只有在pH为5的条件下经过多次冻融循环后才会增加。可溶聚体含量、浑浊度和宏观外观在pH为4和7时无明显差异。在pH3时,单体回收率大大降低,但与pH4或pH7时相比,没有引起聚集或颗粒数增加。ps20通过覆盖冰液界面,在很大程度上可以阻止可见和亚可见颗粒的形成。成分对颗粒形成和浊度的影响可以忽略不计。然而,无辅料配方的单体回收率要高得多,这意味着甘露醇和海藻糖结晶有助于蛋白质的展开,类似于BSA的结果。选择甘露醇和海藻糖的比例,甘露醇和海藻糖很可能结晶。因此, lgG1在没有甘露醇和海藻糖晶体的情况下似乎更稳定。IgG1的展开强烈地依赖于配方的pH,但不能直接与不溶性和可溶性团聚体的形成联系。以牛血清白蛋白作为模型蛋白的研究也显示了类似的结果。因此,我们观察到不同类型的蛋白质(球状和抗体)之间的相似性。pH值、 FT循环次数、表面活性剂的添加和结晶赋形剂的影响是多方面的。其中一个参数的变化可以以不同的方式影响不同的分析,并表明使用正交方法进行表征的重要性。 引言本研究探讨了甘露醇和海藻糖结晶对单克隆抗体IgG1在不同pH条件下反复冻融状态下的影响。配方在−20°C下退火20小时5次(通过冻融中断)。这样做是为了诱导赋形剂结晶。冻融样品的特征是通过圆形二色、颗粒分析和尺寸排除色谱进行的。介绍在冷冻状态储存和冻干的蛋白质配方中,冷冻步骤是关键,因为它决定了蛋白质的稳定性。很好地表明,在稳定的配方中,像甘露醇这样的膨化剂会结晶,而在冷冻和储存过程中,如海藻糖这样的低温防护剂应该保持无定形。增殖剂和冷冻的结晶作用取决于它们的相对浓度以及在配方中蛋白质的浓度。例如,在配方中,一种更高的牛血清白蛋白(BSA)浓度会抑制,甚至完全抑制结晶。其他添加剂,如表面活性剂,也会影响蛋白质的稳定性。目前还不知道,如果所有蛋白质对配方的状态有类似的影响,在冷冻过程中表现得类似。在本研究中,通过改变对甘露醇比的不同配方,探讨了单克隆IgG1抗体的冷冻反应。由于pH值对抗体稳定性的影响,pH值的影响也参与到了研究。该研究的关键参数是抗体的形成、聚集和颗粒的形成,以及冻融后配方的宏观外观。材料D-(+)-海藻糖二水合物(MW 378.33 kDa, 99.9%纯度,Sigma-Aldrich, St. Louis, MO), Tween 20 (MW 1227.54 Da,>98.0%纯度,Biorad Laboratories, Hercules, CA),和D-甘露醇(MW 182.17 Da,≥98%纯度,Sigma-Aldrich)。原液在10mM磷酸钠缓冲液中按重量法配制pH (梅特勒- toledo MP220 pH计,Greifensee,瑞士)。以单克隆抗体(IgG1)作为模型蛋白。所有配方在使用前均通过0.2 μm聚醚砜膜注射器过滤器(VWR International GmbH, Ismaning, Germany)过滤。 冻融实验冻融实验使用FTS LyoStar™3冻干机(SP Scientific, Stone Ridge, NY, USA)进行。2 R小瓶(Fiolax™clear, MGlas AG, Münnerstadt,德国)填充2.0 mL样品溶液和塞(塞类型:Westar®,West Pharmaceutical Services, Eschweiler,德国)。将架子温度提高到−20℃(1℃/min),然后等温保存20 h,以冷却样品。在−20℃保存20 h,我们假设完全冰结晶,任何非晶相的流动性和海藻糖的结晶都是有利的。将架子温度提高到20°C,以1°C/min解冻样品。在选定的小瓶中通过热电偶监测产品温度。冻融循环最多重复五次。检测方法1. 流式颗粒成像分析法(FIA)FlowCAM®8100系列成像仪配备了高分辨率相机(1920×1200像素,10倍放大),用于可视化和计数每毫升样品的亚可见颗粒。样品体积为0.20 mL,流速为0.15 mL/min。系统在测量之间用纯净水冲洗,或用Helmanex®去除流池中的残留蛋白。使用VisualSpreadsheet®软件进行数据分析。2. 光阻法(LO)3. 高效排阻色谱(HP-SEC)4. 浊度(A350nm)5. 紫外线圆二色性(CD)UV CD数据来自新鲜和冷冻解冻的IgG配方。H(r) -正螺旋,H(d) -扭曲螺旋,S(r) -正螺旋,S(d) -扭曲螺旋。溶液被冷冻并在−20°C退火20小时。所有样品都被重复分析。在pH为4和7的条件下循环5次后,甘露醇/海藻糖/IgG制剂的亚可见颗粒数≥25、10和1 μm (FT前的颗粒数分别低于5、20和200颗粒/ mL)。经过5次FT循环后,配方和pH值4(上一行)和pH值7(下一行)的外观。经过5次FT循环后,pH为3的配方的外观(上排)和0.1%的ps20(下排)。在pH为3的条件下,在不添加或添加0.1% PS20的情况下,5次FT循环后,亚可见颗粒数≥25、20和1 μm。结论在pH为3的条件下,在不添加或添加0.1% PS20的情况下,5次FT循环后,可溶性团聚体和单体含量增加。 溶液中的颗粒数只有在pH为5的条件下经过多次冻融循环后才会增加。可溶聚体含量、浑浊度和宏观外观在pH为4和7时无明显差异。在pH 3时,单体回收率大大降低,但与pH 4或pH 7时相比,没有引起聚集或颗粒数增加。ps20通过覆盖冰液界面,在很大程度上可以阻止可见和亚可见颗粒的形成。成分对颗粒形成和浊度的影响可以忽略不计。然而,无辅料配方的单体回收率要高得多,这意味着甘露醇和海藻糖结晶有助于蛋白质的展开,类似于BSA的结果。选择甘露醇和海藻糖的比例,甘露醇和海藻糖很可能结晶。因此,IgG1在没有甘露醇和海藻糖晶体的情况下似乎更稳定。IgG1的展开强烈地依赖于配方的pH,但不能直接与不溶性和可溶性团聚体的形成联系。以牛血清白蛋白作为模型蛋白的研究也显示了类似的结果。因此,我们观察到不同类型的蛋白质(球状和抗体)之间的相似性。pH值、FT循环次数、表面活性剂的添加和结晶赋形剂的影响是多方面的。其中一个参数的变化可以以不同的方式影响不同的分析,并表明使用正交方法进行表征的重要性。
关闭-
1/5

-
2/5
还剩3页未读,是否继续阅读?
继续免费阅读全文产品配置单
大昌华嘉科学仪器为您提供《冻融实验中甘露醇和海藻糖结晶检测方案(图像粒度粒形)》,该方案主要用于其他中其他检测,参考标准《暂无》,《冻融实验中甘露醇和海藻糖结晶检测方案(图像粒度粒形)》用到的仪器有流式颗粒成像分析系统FlowCam®8100、FlowCam® 5000颗粒分析仪、颗粒成像法+光阻法分析系统 FlowCam® + LO。
我要纠错
推荐专场
图像粒度粒形分析仪
更多相关方案











 咨询
咨询
