wangke_wj
第4楼2011/03/31
按照计量关系n(NaOH)=n(HAc)+n(HCl)+4n(Zr),则CH3COOH%=(C(NaOH)V(NaOH)-C(HCl)V(HCL))*60.05/(10m)-4*60.05X/M(ZrO2),其中,60.05为醋酸的分子量,m为样品重量,X和M(ZrO2)分别为ZrO2的含量和式量132.22
我测定了几个样, 计量关系n(NaOH)=n(HAc)+n(HCl)+4n(Zr)好象不正确,数据如下:C(NaOH)=0.4993mol/L,c(HCl)=0.5101mol/L,加50ml氢氧化钠
1#样:样重=4.8104g,v(HCl)=9.70ml,2#样:样重=4.9527g,v(HCl)=11.70ml,3#样:样重=4.8849g,v(HCl)=11.29ml。去掉公式中最后一项进行计算,结果为:1#:24.99%,2#:23.03,3#:23.61。最后一项的的值约40,计算进去,则结果均为负。所以说计量关系n(NaOH)=n(HAc)+n(HCl)+4n(Zr)好象不正确。没有最后一项也许对,究竟如何对?
另一方面,醋酸锆溶液中的醋酸锆分子式,大多写为Zr(CH3COO)2,也有写为Zr(CH3COO)4,和计量关系有关吗?
老化验工
第5楼2011/03/31
如果锆是四价锆,Zr(Ac)4,最终的沉淀是Zr(OH)4,则计量关系是不会错的。这是按质子条件写出的,关系并不复杂。我查过许多商家的醋酸锆是四价锆,所以有4n(Zr)。现在影响结果的原因有两个:
你的锆是不是四价,如果是二价则计量关系改为2n(Zr).
微碱性到碱性的锆会不会生成碱式盐(按《重要无机化学反应》所述,所有碱性溶液反应都是Zr(OH)4),如果生成了碱式盐的话,n(Zr)前后的系数就小于4,而且碱式盐的比例是多大,这是不可知,也是不确定的,因而就无法给出n的系数,也就无法准确计算。我估计,锆在碱性会生成碱式盐,而非百分百的正盐,这就难计算了。
不管锆是否二价还是四价,也不管是生成正盐还是碱式盐,它要消耗NaOH是必然的,因此算式必须含氢氧化锆或碱式醋酸锆这一项(系数取何值取决于它生成什么沉淀,各类锆盐沉淀比例如何)。你滴定的醋酸锆溶液中锆的量是多少?这是要参加计算的。另外,你的醋酸浓度用百分数表示是什么与什么之比?因为计算时最直接的浓度是摩尔浓度,要算成%浓度,需用密度换算或直接称一定体积的溶液质量来计算(你的样重是溶液的质量吗?)。你的氧化锆含量x是指什么,是溶液中的氧化锆百分含量吗?计算式中必须代指定样重(如4.8104g溶液)的溶液中含有的氧化锆的质量,而不是含量。
下面的公式就是计算时的完整公式(假定最终生成的是四价氢氧化锆,标液体积为mL):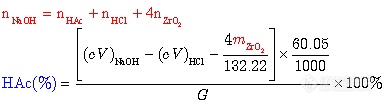
只要生成的锆沉淀是四价氢氧化锆,上面的公式就是正确的。如果是二价锆,如果生成碱式盐,则上式不适用。
wangke_wj
第6楼2011/04/01
你和我的计算公式本质上完全一致。醋酸浓度为重量浓度,样重是溶液的质量。氧化锆含量x是样品中氧化锆占样品的重量百分率,约22(%)。在测定中确实生成了许多白色沉淀。