

草根能力比对之果汁中柠檬黄、日落黄的检测能力验证经验分享
一、前言
6月底报名参加了仪器信息网组织的第四十期草根能力比对:果汁中柠檬黄、日落黄的检测,7月3日收到组织方寄来的包裹,主要包含一瓶果汁样品和一包聚酰胺固相萃取柱(500mg/6mL×6支)(以下简称试用柱)。按照惯例,先检查样品的外包装、瓶口的密封性、核对实验室代码、样品编号等信息;测试之前认真阅读参试指导书和测试结果报告单,了解组织方对测试和结果报告的要求,例如测试方法、对数据结果的要求、检测结果上报日期等。

食品中合成着色剂的测定对我们而言是非常常规的项目,几乎每周都会有样品要求做此类检测,之前也多次参加过类似项目的能力验证,因此对于此次的能力验证还是胸有成竹的。
能力验证样品非常规食品,样品中待测物质的浓度可能超过或者低于常规样品的检测浓度,因此需要先对样品中待测物质的浓度做个粗略的测试,以确定后期前处理过程的取样量和标准溶液的浓度范围。此次能力验证的基质为果汁,依据以往的经验,果汁测定合成着色剂时的干扰组分较少,因此采取直接稀释、过滤膜的方式对样品进行粗略的测定。其目的有两个,一是计算待测组分的大概浓度范围;二是检查待测组分附近是否有干扰物。
二、材料与方法
仪器条件:按照GB/T 5009.35-2003中的液相条件进行测试
色谱柱:CNW Athena C18-WP(250mm×4.6mm ,5μm)
流动相:甲醇:乙酸铵(0.02mol/L)
梯度洗脱:甲醇:20%~35%,3%/min;35%~98%,9%/min;98%继续保持2min
流速:1.0mL/min
柱温:30℃
检测器:测试波长为254nm
三、实验与讨论
实验一:样品稀释后直接进样
称取约5g果汁样品于25mL容量瓶中,用水稀释、混匀、定容,经0.45μm滤膜过滤后进样测定,测定结果见下图。
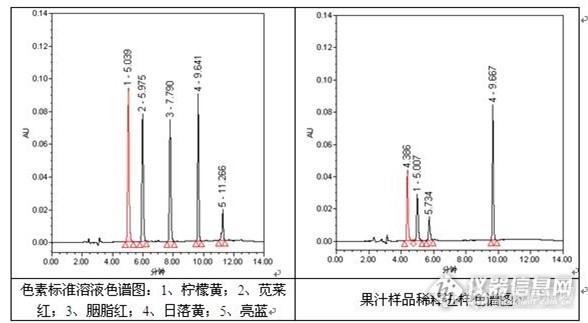
通过测试可以发现,果汁样品中待测组分柠檬黄的浓度较小,且附近有干扰物质存在,日落黄的浓度较高,不存在干扰峰,计算后得到果汁样品中柠檬黄的浓度大约为28mg/kg,日落黄的浓度大约为98mg/kg。
有些版友看了果汁样品稀释后进样的色谱图,可能觉得待测组分与干扰峰的分离度和峰形都还不错,应该可以直接定量了,如果真的这么做,很可能会出错,原因有两点:(1)果汁中不仅含有着色剂,通常还会含有甜味剂、防腐剂等添加剂,在此色谱条件下,这些物质也会出峰,如果仪器或者色谱柱等原因导致两者出峰完全重叠,则可能会出现定量不准确;(2)着色剂包含人工合成着色剂和天然着色剂两大类,GB 5009.35 测定的是人工合成着色剂,如果有天然着色剂也会产生干扰,从而引起定量的不准确,GB 5009.35中采用甲醇-甲酸混合溶液和水洗涤就是为了去除天然着色剂和一些水溶性的干扰物。
实验二:参照GB 5009.35的方法进行样品前处理
称取约5g果汁样品于100mL烧杯中,加入少量水,加热到60℃,将1g聚酰胺粉倒入样品溶液中,搅拌,以G3垂融漏斗抽滤,然后用甲醇-甲酸(V:V=6:4)混合溶液洗涤,再用水洗至中性,抽干后用乙醇-氨水(V:V=7:3))混合溶液解析,直到色素完全解析,收集解析液,60℃砂浴中氮吹至近干,加水溶解并定容至25mL,经0.45μm微孔滤膜过滤后进样分析。
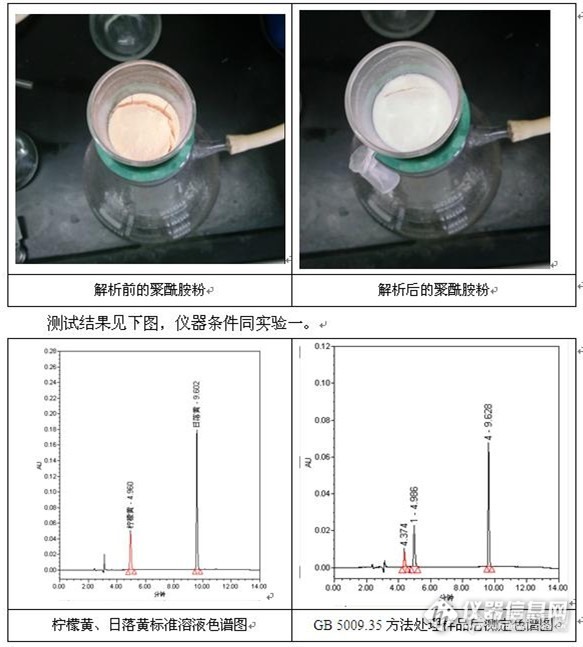
果汁样品经GB 5009.35方法处理后,4.3min的干扰峰明显变小,5.7min的干扰峰完全消失,5.0min和9.6min的色谱峰略有减小。
实验三:CNW Poly-sery PA SPE柱净化样品
尽管此次草根能力比对的组织者提供了聚酰胺固相萃取柱,但是数量有限,没敢轻易使用,而实验室备有从上海安谱实验科技股份有限公司(以下简称上海安谱)采购的CNW Poly-sery PA SPE固相萃取柱,数量充足,而且在平时测定人工合成着色剂时也有很好的表现,因此先用上海安谱的CNW Poly-sery PA SPE固相萃取柱对样品进行前处理。
称取约1g果汁样品于5mL试管中,用水将果汁样品转移至聚酰胺固相萃取柱中,并用水洗涤试管2~3次,洗涤液一并转移到固相萃取柱中,抽滤至近干,用甲醇-甲酸(V:V=6:4)混合溶液洗涤,再用水洗至中性,抽干后用乙醇-氨水(V:V=7:3)混合溶液解析,直到色素完全解析,收集解析液,60℃砂浴中氮吹至近干,加水溶解并定容至5mL,经0.45μm微孔滤膜过滤后进样分析。

测试结果见下图,仪器条件同实验一。
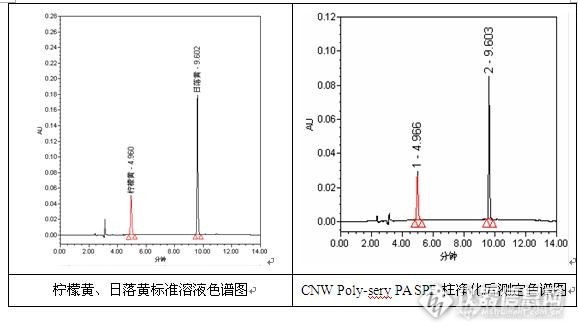
实验四:试用柱净化样品
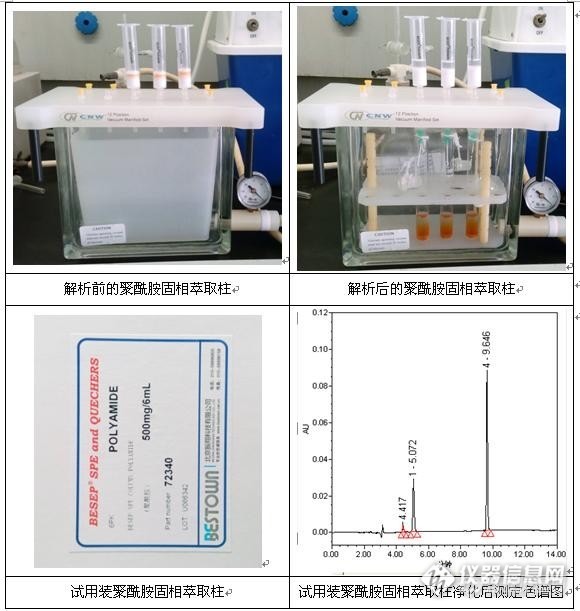
样品净化过程和仪器条件同实验三,实验过程和实验结果见下图。
实验五:自制聚酰胺固相萃取柱净化样品
实验中用到的样品量很少,做完上述实验还剩许多样品,而且距离上报结果的时间还很宽裕,于是突发奇想,决定利用实验室采购的聚酰胺粉自制聚酰胺固相萃取柱,并对样品进行测定,一方面考察自制聚酰胺固相萃取柱的性能,另一方面与上述实验结果进行比对验证。
聚酰胺固相萃取柱的制作过程如下:
1、准备好原材料:锋利的剪刀、废弃的固相萃取柱、同规格的针筒、聚酰胺粉

2、用剪刀或美工刀等工具对固相萃取柱进行破拆,取出固相萃取柱中的筛板。筛板在使用前需要用甲醇、水、氨化乙醇等溶液进行清洗,防止有污染,同时防止之前使用过程中筛板有堵塞,影响后续的过柱。筛板烘干后装入合适的针筒中。
3、依据实验用量,称重装入适量的聚酰胺粉,夯实针筒中的聚酰胺粉,此次实验装入的聚酰胺粉质量为500mg。可以在聚酰胺粉上端再装入一个筛板,防止在使用和存放过程中填料发生松动。

到此,仅仅简单的几步就将聚酰胺固相萃取柱制作完成了,效果如何呢,用实验数据进行验证。样品净化过程和仪器条件同实验三,实验过程和实验结果见下图。

从上述实验可以看出:(1)三款聚酰胺固相萃取柱对待测人工合成着色剂均具有很好的吸附作用;(2)上样量选择1g时未发生柱容量饱和的现象;(3)乙醇-氨水(V:V=7:3)对待测人工合成着色剂具有很好的解析效果,解析液颜色为下深上浅,而且经过解析后聚酰胺固相萃取柱又恢复了原来的本色,解析非常完全;(4)采用聚酰胺固相萃取柱净化后5.7min的干扰峰完全消失,5.0min和9.6min处色谱峰的测定结果相近;(5)不同聚酰胺固相萃取柱对样品的净化效果略有差别,主要体现在4.3min干扰峰的净化效果方面,自制的聚酰胺固相萃取柱净化后4.3min处的干扰峰仍然很大,其峰高和峰面积与采用聚酰胺粉净化的结果相近,试用装聚酰胺固相萃取柱净化后4.3min处干扰峰明显减小,而用CNW Poly-sery PA SPE柱净化后4.3min处干扰峰完全消失,同时不影响5.0min和9.6min处待测组分的峰面积。
实验六:标准曲线的绘制与含量计算
根据上述测定结果重新配制标准溶液,绘制标准曲线,进行含量计算。

实验七:回收率实验
取实验室中不含待测组分的果汁样品,称取一定质量的果汁样品5份,往样品中加入一定体积的柠檬黄、日落黄标准溶液,然后分别按照实验一、实验二、实验三、实验四和实验五的方法进行样品前处理,测定方法的回收率,测定结果如下表。
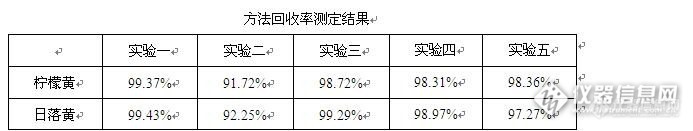
回收率测定结果表明,直接稀释进样和聚酰胺固相萃取柱净化样品后的回收率较高,聚酰胺粉吸附净化样品的回收率略低于其他两种方法。聚酰胺粉净化样品回收率低的原因有以下4种:(1)上样量或者聚酰胺粉的用量不合适,出现聚酰胺粉吸附过载或不完全吸附;(2)聚酰胺粉的质量要求不合适,未达到标准要求,从而出现不完全吸附;(3)解析过程中未完全解析;(4)其他操作过程中的损失,如样品转移、定容、酸洗、水洗等。
本次能力验证样品基质相对简单,而且实验一表明样品直接稀释后进样待测组分与干扰物质的分离度达到检测要求,实验三、实验四和实验五表明待测组分保留时间处没有其它成份的干扰,因此最终决定采用实验一的方法进行测定,并采用实验一的数据做为最终结果,避免做的多错的多,减少操作过程中的损失。
能力验证的实验到此结束,然而爱折腾的人会折腾个没完没了。测完柠檬黄、日落黄后想知道其他两个干扰峰是什么物质。凭借以往的经验,这两种物质为色素、甜味剂和防腐剂的可能性比较大,这三类物质是果汁中的常见添加剂。人工合成着色剂的可能性排除,原因为:(1)与5种人工合成着色剂的保留时间不一致;(2)酸洗、水洗后峰面积明显变小,GB 5009.35中除了赤藓红,其它人工合成着色剂不会出现这种情况。
排除了其他人工合成着色剂存在的可能,于是在上述仪器条件下测定甜味剂糖精钠和安赛蜜,防腐剂山梨酸和苯甲酸的单标及混合标准溶液,测定结果如下图。
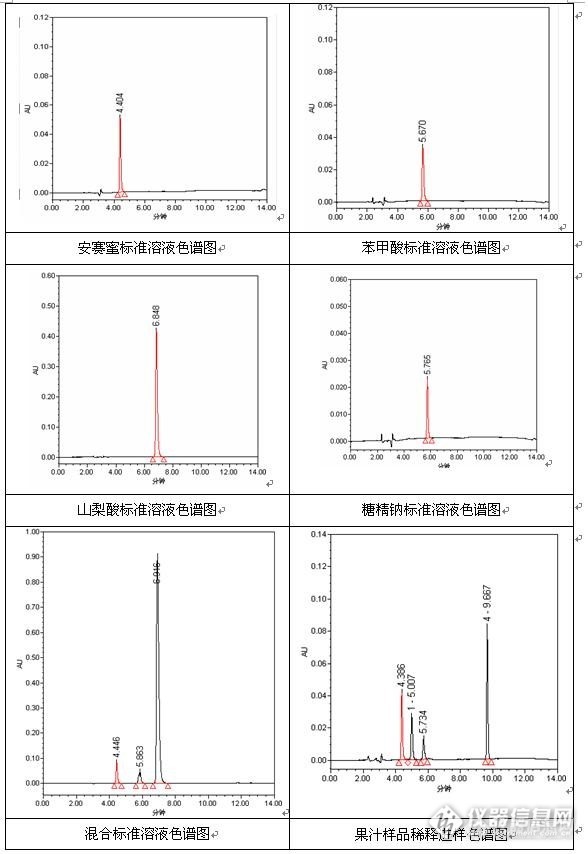
通过上述测定,依据保留时间定性,4.4min的干扰物质可能为安赛蜜,5.7min的干扰物质可能是苯甲酸或糖精钠。实验室没有质谱,因此只能通过保留时间做个简单的判断。在此仪器条件下,糖精钠和苯甲酸的色谱峰发生了重叠,从而进一步表明,测定人工合成着色剂时需要通过酸洗和水洗来排除干扰,避免出现类似于糖精钠和苯甲酸重叠的现象。
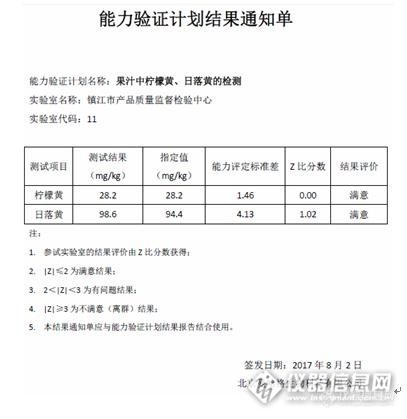
8月初收到结果通知单,两种待测物质的结果评价均为满意,其中柠檬黄的测定值与指定值相同,进一步表明上述实验方法与结果的正确性。
四、小结
针对此次能力验证做个简单的小结,小结如下:
(1)采用聚酰胺固相萃取柱净化样品测定人工合成着色剂时回收率高,试剂用量少,适用于样品的批量处理;
(2)样品处理过程中吸附和解析的时候控制流速,可以先让其吸附/解析一会再抽滤,以保证吸附/解析完全;
(3)不同聚酰胺固相萃取柱对样品的净化效果产生差别的原因,一方面可能与填料有关,因为实验二和实验五采用的是相同填料,4.3min处都存在较大的干扰峰,另一方面可能与水洗有关,标准中要求水洗至中性,因此水洗的次数会有差别,而安赛蜜是水溶性的,不同剂量的水对安赛蜜的去处能力也是不同的;
(4)自制聚酰胺固相萃取柱的填料松散不一,填料上端不加筛板时,在样品前处理以及存放的过程中容易出现填料松动,以及填料随着试剂浮动的现象,可能会影响实验到实验数据的重复性;
(5)破拆筛板的过程需要注意安全,如果想省事,可以直接购买筛板或者带筛板的空柱,然后自行装填填料;
(6)GB/T 5009.35-2003方法已经失效,但是前处理方法与新标准相似,梯度方法略有差别,以往实验中采用旧标准的梯度洗脱条件对人工合成着色剂的分离状况可以满足实验要求,因此本次试验方法依然采用了GB/T 5009.35-2003的分析方法。
问题123
第7楼2018/11/23
酰胺吸附法:样品溶液加柠檬酸溶液调pH到6,加热至60?C,将1g聚酰胺粉加少许水调成粥状,倒入样品溶液中,搅拌片刻,以G3垂融漏斗抽滤,用60?CpH为4的水洗涤3次~5次,然后用甲醇-甲酸混合溶液洗涤3次~5次(含赤藓红的样品用5.2.2法处理),再用水洗至中性,用乙醇-氨水-水混合溶液解吸3次~5次,直至色素完全解吸,收集解吸液,加乙酸中和,蒸发至近干,加水溶解,定容至5mL。经0.45μm微孔滤膜过滤,进高效液相色谱仪分析。
老师这是新标准中的净化方法,开始样品中加入柠檬酸调Ph值是什么目的,还有就是收集的解析液加乙酸中和的目的是什么?
夏天的雪
第8楼2018/11/23
加柠檬酸是为了调节pH值,酸性条件下,聚酰胺的吸附性能更好,加乙酸中和是也是为了调节pH值,如果最终上机液的pH与流动相或者标准溶液相差太大,会出现保留时间的漂移。