离子色谱法测定镍锰酸锂正极材料中的硫酸根含量
邓 蓓*1,2,彭桂香1,2
(1、宜春市锂电产业研究院,江西宜春,336000;2、江西省锂电产品质量监督检验中心,江西宜春,336000)
摘 要 采用离子色谱法测定镍锰酸锂中硫酸根离子的含量,用盐酸和双氧水溶解试样,通过固相萃取柱净化后至离子色谱仪上进样测试,通过多次对比实验,优化了试验方法;在优化的试验条件下,硫酸根在0~20.0μg?L-1范围内具有良好的线性关系,其线性相关系数为0.9998。对4个不同含量的样品分别进行了11次平行测定,相对标准偏差(RSD)为1.6~5.9%。在镍锰酸锂试样中加入硫酸根标液进行加标回收实验,硫酸根离子的加标回收率在96.1%~106.3%之间。与传统的硫酸钡比浊法相比,离子色谱法操作简便快捷,方法检出限低,测量范围更宽,干扰少,测定结果可靠,再现性良好,适合大批量快速样品分析。
关键词 镍锰酸锂;离子色谱法;硫酸根离子
Determination of sulfate in LiNi0.5Mn1.5O4 cathode materials by Ion chromatography
DENG Bei*1,2,PENG Guixiang1,2
(1. Yichun research institute of lithium battery industry,Yichun,Jiangxi,336000,China;
2.Jiangxi Province Litium Product Quality Supervision and Inspection Center, Yichun, Jiangxi, 336000, China )
Abstract: The component of sulfate in LiNi0.5Mn1.5O4 were determined by Ion chromatography,The samples were dissolved in hydrochloric acid and hydrogen peroxide, purified by solid phase extraction column and injected into ion chromatography for test. The mass concentration of sulfate ion in the range of 0~20.0μg?L-1 had a good linear relationship with correlation coefficients of 0.9998.Under the optimal conditions,the relative standard deviations (RSD) of four different mass concentration samples were 1.6~5.9% for 11 parallel measurements. For recovery tests, sulfate ion were added into the LiNi0.5Mn1.5O4 samples and the recovery rates of sulfate ions were in the range of 99.4%~100.2%. Compared with the double indicator titration method, the ion chromatography method is convenient and fast. At the same time, this method has the advantages of simple operation,a lower detection limit,a wider measurement range,less interference, high precision, reliable determination results and good reproducibility. It is suitable for rapid analysis of large quantities of samples.
Keywords: LiNi0.5Mn1.5O4;ion chromatography;sulfate ion
摘要 随着锂离子电池在新能源汽车领域的应用扩展[1]以及“双碳”政策[2]的深入。人们对锂电池性能的要求越来越高[1]。锂电池的性能很大程度上取决于正极材料[3],而镍锰酸锂正极材料具有资源丰富、成本低、环境友好、电压高且能量密度高等优势,在大功率领域中得到了广泛应用,从而成为了研究热点[4-8]。在制备镍锰酸锂的过程中,会残留一定量的硫酸盐,因此,硫酸根含量是其成品的一项重要技术指标。现有的测定硫酸根的方法主要有:离子色谱法、分光光度法和电位滴定法[9-12]。其中,分光光度法[11]需严格控制操作条件,且测定镍锰类等有色金属化合物时,本底值有颜色需要差减法扣除,含量较低时精密度不够好;电位滴定法[12]只适合高含量的硫酸根离子测定;而离子色谱法[9-10]检出限低、操作便捷高速效率高且样品前处理简单。因此,在镍锰酸锂中测定硫酸根时选择离子色谱法。
1实验部分
1.1主要仪器与试剂
除非另有说明,本文中实验用水均为去离子水(18.25MΩ?cm)。
Metrohm ECO-IC离子色谱仪(瑞士万通公司);Metrosep A Supp 5-250/4.0色谱柱(瑞士万通公司);H型预处理柱:AnL Pre IC-H-1cc(宁波鸿谱仪器科技有限公司);Ag型预处理柱:AnL Pre IC-Ag-2.5cc(宁波鸿谱仪器科技有限公司);水系微孔过滤滤膜:50(mm)×0.45(μm);聚醚砜(PES)针筒式过滤器:13(mm)×0.22(μm);万分之一天平(梅特勒MS205DU);Milli-Q去离子水制备装置(德国默克密理博);真空抽滤装置(天津市津腾实验设备有限公司)无水碳酸氢钠(优级纯);无水碳酸钠(优级纯);浓硫酸(优级纯);浓盐酸(优级纯);30%过氧化氢(分析纯);7种阴离子(氟离子、氯离子、硝酸根离子、亚硝酸根离子、溴离子、硫酸根离子、磷酸根离子)混合标准溶液(质量浓度为1000mg?L-1) 国家标准物质中心。
1.2 实验方法
1.2.1 标准溶液的配制
储备液的配制:用移液枪准确移取10mL混合标准溶液于100mL容量瓶中,加水稀释至终点刻度,摇匀,静置备用,放置于4℃冰箱中保存。此溶液1.00mL相当于100μg硫酸根。
标准曲线溶液的配制:用移液枪分别准确移取0mL、0.50mL、1.25mL、2.50mL、5.0mL和10.0mL储备液,分别置于50mL容量瓶中,加水稀释至终点刻度,摇匀,静置备测。该系列溶液1.00mL分别相当于0.00μg、1.00μg、2.50μg、5.00μg、10.00μg、20.00μg硫酸根。在本方法确定的最佳实验条件下依次从浓度低到高的顺序进样,绘制标准曲线。
1.2.2 色谱条件
色谱柱选用 Metrosep A Supp 5-250/4.0色谱柱;流速0.7mL?min-1 ;流动相4.5mmol?L-1NaHCO3-4.5mmol?L-1Na2CO3溶液;进样体积20μL;电导检测器。
1.2.3 样品测定
将镍锰酸锂样品在105-110 ℃下烘干2h,然后置于干燥器内,冷却至室温,备用。准确称取 0.2000g(精确至0.0001g)镍锰酸锂试样于100 mL 烧杯中,缓慢加入3.0mL盐酸(1+1),再加入4-5滴过氧化氢,低温加热至完全溶解且蒸发至近干,冷却,加5-10mL水溶解,转移至100mL容量瓶中,用水洗涤烧杯3-5次,同时将洗涤液转移至容量瓶中,用水稀释至刻度,摇匀,待净化。
将H柱和Ag柱用10mL水活化,静置10min,将上述溶液缓慢通过活化好的H柱和Ag柱,弃去前3mL滤出液,获取后续2mL滤出液,过0.22μm聚醚砜(PES)针筒式过滤器,上机待测。
2 结果与讨论
2.1 淋洗液浓度的选择
为了检验其他阴离子对硫酸根离子峰积分的干扰,选择了7种阴离子(氟离子、氯离子、硝酸根离子、亚硝酸根离子、溴离子、硫酸根离子、磷酸根离子)混合标准溶液进行分离,分别使用三种不同浓度的淋洗液对待测标准溶液进行淋洗分离。实验结果如图1所示,具体浓度等信息见表1。
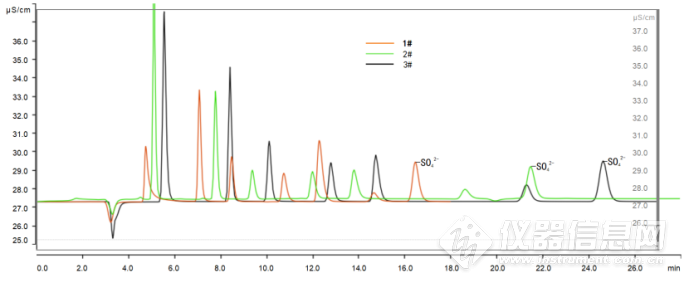
图1 不同浓度淋洗液的离子色谱图
Fig. 1 Ion chromatograms of different concentrations of eluent
表1 不同浓度淋洗液的出峰时间
Table 1 Peak time of different concentrations
编号 No. | 淋洗液浓度 concentrations of eluent | 7种阴离子 分离情况 Separation of 7 anions | SO42-出峰时间 Peak time/min |
Na2CO3 /(mmol/L) | NaHCO3 /(mmol/L) |
1# | 4.54 | 0.8 | 好 | 16.3 |
2# | 3.2 | 1.0 | 好 | 21.8 |
3# | 4.5 | 1.4 | 好 | 24.5 |
由图1和表1可知,三种浓度的淋洗液都能很好的将7种阴离子分离,但是,从时间、资源和环境的角度,我们选择了更早出峰的1#淋洗液(4.54mmol/LNa2CO3-0.8mmol/LNaHCO3 ),这样既节省时间、节约资源,同时更少的淋洗液减少了废液的处理从而对环境更友好。
2.2 溶样方法的选择
采用硝酸和盐酸加双氧水的方式溶样,称样量均为0.2g时的试验结果见表2。由表2可知,硝酸较难溶解样品,盐酸能够溶解样品但是速度缓慢,盐酸和双氧水加入样品混匀,在低温电热板上微热数分钟即可将样品完全溶解。
表2 溶样方法
Table 2 Methods of sample dissolving
溶样介质 Sample dissolving medium | 溶解状态 Dissolved state | 溶样介质 Sample dissolving medium | 溶解状态 Dissolved state |
HNO3 | 难溶 | HCl | 溶解缓慢 |
HNO3 + H2O2 | 溶解缓慢 | HCl + H2O2 | 溶解,澄清 |
2.3 盐酸+双氧水加入量试验
由于离子色谱仪测定时,氯离子也会出峰,浓度过大会造成拖尾并且会严重影响硫酸根离子的出峰和积分。溶解样品的盐酸中含有大量的氯离子,因此,盐酸的加入量在保证能够溶解样品的条件下应当越少越好。所以,做了盐酸和双氧水加入量的一系列试验。表3是称样量为0.2g时不同盐酸和双氧水加入量的试验结果。由表3中结果可知,当称样量为0.2g,盐酸(1+1)用量3mL、双氧水用量0.5mL时,样品在低温电热板上微热数分钟刚好能够完全溶解,满足测定分析要求。因此,当称样量为0.2g时,选择3mL盐酸(1+1)、0.5mL双氧水作为溶样体系。
表3 盐酸+双氧水加入量试验
Table 3 Hydrochloric acid + hydrogen peroxide addition test
盐酸(1+1)加入量 Addition of HCl(1+1) | 双氧水加入量 Addition of H2O2 | 溶解状态 Dissolved state |
1.00mL | 0.50mL | 部分溶解,有黑渣 |
1.00mL |
2.00mL | 0.50mL | 基本溶解,有少量残余 |
1.00mL |
3.00mL | 0.50mL | 完全溶解,澄清 |
1.00mL |
4.00mL | 0.50mL | 完全溶解,澄清 |
1.00mL |
2.4 溶液是否蒸干再定容试验
由于氯离子对硫酸根的测定有一定的干扰,而加入的盐酸可以通过加热的形式蒸发掉一部分,所以,进行了定容前是否蒸干的对比试验,其结果如图2所示。
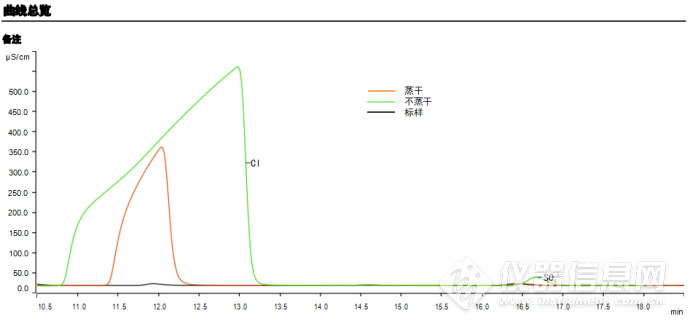
图2 样品蒸干与不蒸干的图谱
Fig. 2 Ion chromatograms of dried and non dried samples
由图2可知,未蒸干时的氯离子峰又宽又长,已经影响了硫酸根的出峰时间,而蒸干后的氯离子峰虽然仍旧较宽但已经明显小了不少,并且没有影响硫酸根离子的出峰时间。所以,蒸干有利于硫酸根的测定,因此,选择在定容前将溶液低温加热至近干。
2.5 固相萃取柱的选择
由于溶液中含有锂、钠、钾、钙、铁、铜、铬和镉等金属离子以及残留的氯离子的干扰,在溶液进样前需要过柱子净化。选取H柱去除溶液中可能存在的金属离子和Ag柱去除溶液中氯离子,其结果见图3、图4。
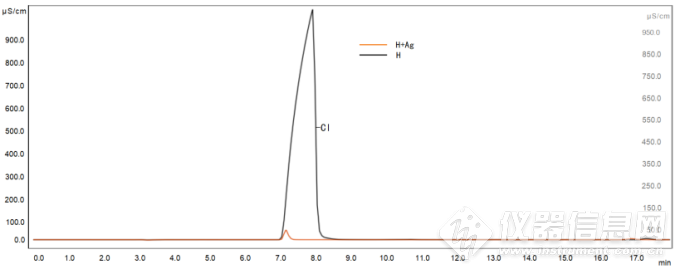
图3 过H柱和过H柱+Ag柱的试验结果
Fig. 3 Test results of passingH column and passing H column + Ag column
由图3可知,溶液只过H柱时氯离子峰特别高,严重影响了硫酸根离子的测定;而同时过H柱和Ag柱的话,氯离子峰就大大变小了,有利于硫酸根的测定。
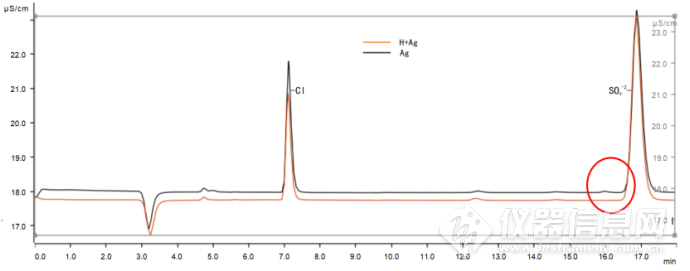
图4 过Ag柱和过H柱+Ag柱的试验结果
Fig. 4 Test results of passing Ag column and passing H column + Ag column
由图4可知,只过Ag柱时硫酸根离子附近会有干扰峰,而同时过H柱和Ag柱则没有。所以综上所述,选择过H柱+Ag柱为佳。
2.6 标准曲线、检出限及定量限
在 1.2.2仪器工作条件下,分别测定了1.2.1中系列混合标准工作溶液。以硫酸根质量浓度(x)为横坐标,色谱峰面积(y)为纵坐标绘制校准曲线。结果表明,硫酸根离子的线性范围为0~20.0μg?L-1,线性方程为y=8.54057×10-3+7.01333×10-3x,相关系数为0.9998。
依据计量规范JJG823-2014[13],选取相应的1.0μg?L-1硫酸根标准溶液进行11次平行测定并计算检出限为0.01μg?L-1,依据EPA SW-846方法规定采用4倍检出限浓度作为定量限为0.04μg?L-1。
2.7 精密度试验
选取4个不同品位的产品,按照设定的实验方法对样品中的硫酸根含量分别进行11次平行测定。得到11个测定值,计算其平均值、标准偏差及相对标准偏差,结果见表4,结果证明精密度满足分析要求。
表4方法精密度实验结果
Table 4 Precision tests of the method(n=11) /%
样品编号 Sample No. | 测定值(n=11) Found |
平均值
Average |
标准偏差SD |
相对标准偏差RSD |
1# |
0.0643 |
0.0579 |
0.0567 |
0.0539 | 0.0585 | 0.343 | 5.865 |
0.0595 |
0.0613 |
0.0618 |
0.0605 |
0.0534 |
0.0554 |
0.0585 |
|
2# |
0.112 |
0.118 |
0.118 |
0.116 | 0.115 | 0.224 | 1.953 |
0.114 |
0.114 |
0.115 |
0.113 |
0.116 |
0.111 |
0.115 |
|
3# |
0.318 |
0.303 |
0.308 |
0.317 | 0.314 | 0.777 | 2.473 |
0.323 |
0.318 |
0.313 |
0.316 |
0.309 |
0.304 |
0.328 |
|
4# |
0.652 |
0.632 |
0.655 |
0.650 | 0.638 | 1.058 | 1.658 |
0.632 |
0.623 |
0.635 |
0.643 |
0.634 |
0.626 |
0.638 |
|
2.8 加标回收试验
由于目前还没有相应的镍锰酸锂标准样品,所以采取在样品中添加不同含量的硫酸根离子进行加标回收试验,按照试验方法进行样品处理、测定,其结果见表5。该方法加标回收率在96.1~106.3%之间,能够满足测定要求。
表5 加标回收试验
Table 5 Recovery tests
样品编号 Sample No. | 样品量m1 Mass of Sample /g | 本底值SO42 Mass of SO42- /μg | SO42-加标量m2 Spiked /μg | 测定值m3 Measured value /μg | 回收率η Recovery /% |
1# | 0.2013 | 117.52 | 50 | 169.22 | 103.4 |
0.2002 | 117.02 | 100 | 213.12 | 96.1 |
2# | 0.2003 | 230.01 | 100 | 326.41 | 96.4 |
0.2005 | 231.03 | 200 | 426.62 | 97.8 |
3# | 0.2015 | 628.56 | 500 | 1160.06 | 106.3 |
0.2008 | 629.01 | 750 | 1367.76 | 98.5 |
4# | 0.2011 | 1277.05 | 500 | 1768.55 | 98.3 |
0.2006 | 1276.13 | 750 | 2041.88 | 102.1 |
2.9方法比对
目前,测定硫酸根的含量主要有两种方法,分别是离子色谱法和硫酸钡比浊法。对该两种方法分别进行了试验,结果如表6所示。由表6可知,含量高的时候两种方法的结果相差不大,但是含量低的时候,硫酸钡比浊法测定结果不理想。并且,硫酸钡比浊法对加入的硝酸钡状态和用量要求较高,测定前的静置时间也比较严格,在一定的时间内必须完成测定,同时对实验人员的操作手法要求严苛,因此,不适合批量测定。而离子色谱法前处理简单便捷,样品处理后稳定性良好,可用于大量样品的测定。
表6 测定镍锰酸锂中的硫酸根含量
Table 6 Determination of sulfate content in LiNi0.5Mn1.5O4 /%
样品编号 Sample NO. | 离子色谱法测定值 Found by ion chromatography method | 硫酸钡比浊法测定值 Found by barium sulfate turbidimetry method |
1# | 0.0585 | 未检出 |
2# | 0.115 | 0.089 |
3# | 0.314 | 0.321 |
4# | 0.638 | 0.650 |
在实验过程中,从称样量、检出限和前处理等方面对比了离子色谱法和硫酸钡比浊法,具体对比结果见表7。
表7 两种方法对比
Table 7 Comparison of two methods
序号 NO. | 项目 Content | 离子色谱法 Ion chromatography method | 硫酸钡比浊法 Barium sulfate turbidimetry method |
1 | 方法检出限 | 0.01% | 0.1% |
2 | 称样量 | 0.2g | 1.0g |
3 | 前处理样品稳定性 | 常温下15天内稳定 | 静置15-30min内完成测定 |
4 | 测定范围 | 0.01%-0.7% | 0.1%-0.7% |
由表7可知,离子色谱法不仅测定结果可靠、方法检出限低,而且前处理样品稳定性好。因此,不管是从结果准确性和测定范围还是从效率上来看,离子色谱法都更胜一筹。
3 结语
镍锰酸锂正极材料样品用盐酸和双氧水溶解,通过固相萃取柱净化后至离子色谱仪上进样测定,较传统的硫酸钡比浊法,方法操作简单便捷,样品稳定性良好,干扰少,方法检出限低,测定范围宽,精密度较高,测定结果可靠,再现性良好,适合大批量快速样品分析。
References
[1]李 旺,周 兰,刘佳丽.镍锰酸锂正极材料及其适配性电解液研究最新进展[J].无机盐工业,2019,51(6):5-10.
Li Wang , Zhou Lan , Liu Jiali.Latest development of LiNi0.5 Mn1.5 O4 cathode materials and adaptive electrolytes[J].Inorganic chemicals industry,2019,51(6):5-10
[2] 钟茂初."双碳"目标有效路径及误区的理论分析[J].中国地质大学学报(社会科学版).2022,22(1):10-21.
ZHONG Mao-chu.A Theoretical Analysis on the Effective Path and the Misunderstanding of "Dual Carbon" Goal[J].Journal of China University of Geosciences (Social Sciences Edition).2022,22(1):10-21.
[3] 王静,吴比赫,林伟庆,等.锂离子电池高电压正极材料LiNi0.5Mn1.5O4-----研究进展[J].厦门大学学报:自然科学版,2015,54(5):630—642.
Wang Jing,Wu Bihe,Lin Weiqing,eta1.Research progress in high—voltage LiNi0.5Mn1.5O4 for lithium ion batteries[J].Journal of Xia’men University:Natural Science,2015,54(5):630—642.
[4] 金彦章,王永和,刘强,等.高电压正极材料LiNi0.5Mn1.5O4制备及性能研究[J].无机盐工业, 2017, 49 ( 6 ): 45-49.
Jin YanzhangWang YongheLiu Qiang,eta1.Study on synthesis and performance of high-voltage LiNi0.5Mn1.5O4 cathode material for lithium-ion battery[J].Inorganic Chemicals Industry.2017, 49(6):45-49
[5] Rahaye I,Noviyanti A R,Rakmawaty D,etal.Preparation of Lithium Iron Phosphate-Carbon Composite as a Cathode for Lithium Ion Battery[J].Materials Science Forum,2019,966:392-397.
[6] Wen Weicheng,Yang Xiukang,Wang Xianyou,etal.Improved electrochemical performance of the spherical LiNi0.5Mn1.5O4 particles modified by nano-Y2O3 coating[J].Journal of Solid State Electrochemistry,2015,19(4):1235-1246.
[7] Nageswaran S,Keppeler M,Kim S J,etal.Morphology controlled Simodified LiNi0.5Mn1.5O4,microspheres as high performance high voltage cathode materials in lithium ion batteries[J].Journal of Power Sources,2017,346:89-96.
[8] 杨强强 , 崔雅茹,李 倩,等.共沉淀法合成镍锰酸锂正极材料前驱体[J].矿冶工程.2020,40(5):134-138
YANG Qiang-qiang,GUI Ya-ru,LI Qian,etal.Synthesis of Precursor of LNMO Cathode Material by Coprecipitation Method[J].Mining and metallurgical engineering. 2020,40(5):134-138
[9]刘春峰. 离子色谱法测定镍钴锰氢氧化物中硫酸根离子含量[J].中国无机分
析化学.2013,3(z1).
LIU Chunfeng.Determination of Principal Components in Industrial and Battery Lithium Carbonate by Automatic Potentiometric Titration Method
Determination of sulfate ion in Nickel Cobalt Manganese Hydroxide by ion chromatography[J].Chinese Jorunal of Inorganic Analytical Chemistry.2013,3(z1).
[10]张枫华,雷仲存,顾红琴.离子色谱法测定水中硫酸根离子浓度范围的探讨[J].
冶金动力.2013,161(7):56-60.
ZHANG Fenghua,LAI Zhongcun,GU Hongqin.Discussion on suitable concentration range of sulfate ion in water determined by ion chromatography[J].Metallurgical Power,2013,161(7):56-60.
[11] GB/T 11064.9-2013碳酸锂、单水氢氧化锂、氯化锂化学分析方法 第9部分 硫酸根量的测定 硫酸钡浊度法.GB/T 11064.9-GB/T 11064.9-2013 Methods for chemical analysis of lithium carbonate, lithium hydroxide monohydrate and lithium chloride - Part 9:determination of sulfate content Barium sulfate nephelometry method.
[12] 刘月菊,宋明明,邸卫利,等.电位滴定法测定钒电池电解液中硫酸根[J].冶金分析.2019,39(4):75-79.
LIU Yue-ju,SONG Ming-ming,DI Wei-li,etal.Determination of sulfate in vanadium battery electrolyte by potentiometric titration[J].Metallurgical Analysis,2019, 39(4):75-79
[13] JJG823-2014离子色谱仪检定规程.
JJG823-2014Verification Regulation of Ion Chromatographs:.
2013 Methods for chemical analysis of lithium carbonate, lithium hydroxide monohydrate and lithium chloride - Part 9:determination of sulfate content Barium sulfate nephelometry method.
[12] 刘月菊,宋明明,邸卫利,等.电位滴定法测定钒电池电解液中硫酸根[J].冶金分析.2019,39(4):75-79.
LIU Yue-ju,SONG Ming-ming,DI Wei-li,etal.Determination of sulfate in vanadium battery electrolyte by potentiometric titration[J].Metallurgical Analysis,2019, 39(4):75-79
[13] JJG823-2014离子色谱仪检定规程.
JJG823-2014Verification Regulation of Ion Chromatographs:.




