方案详情文
智能文字提取功能测试中
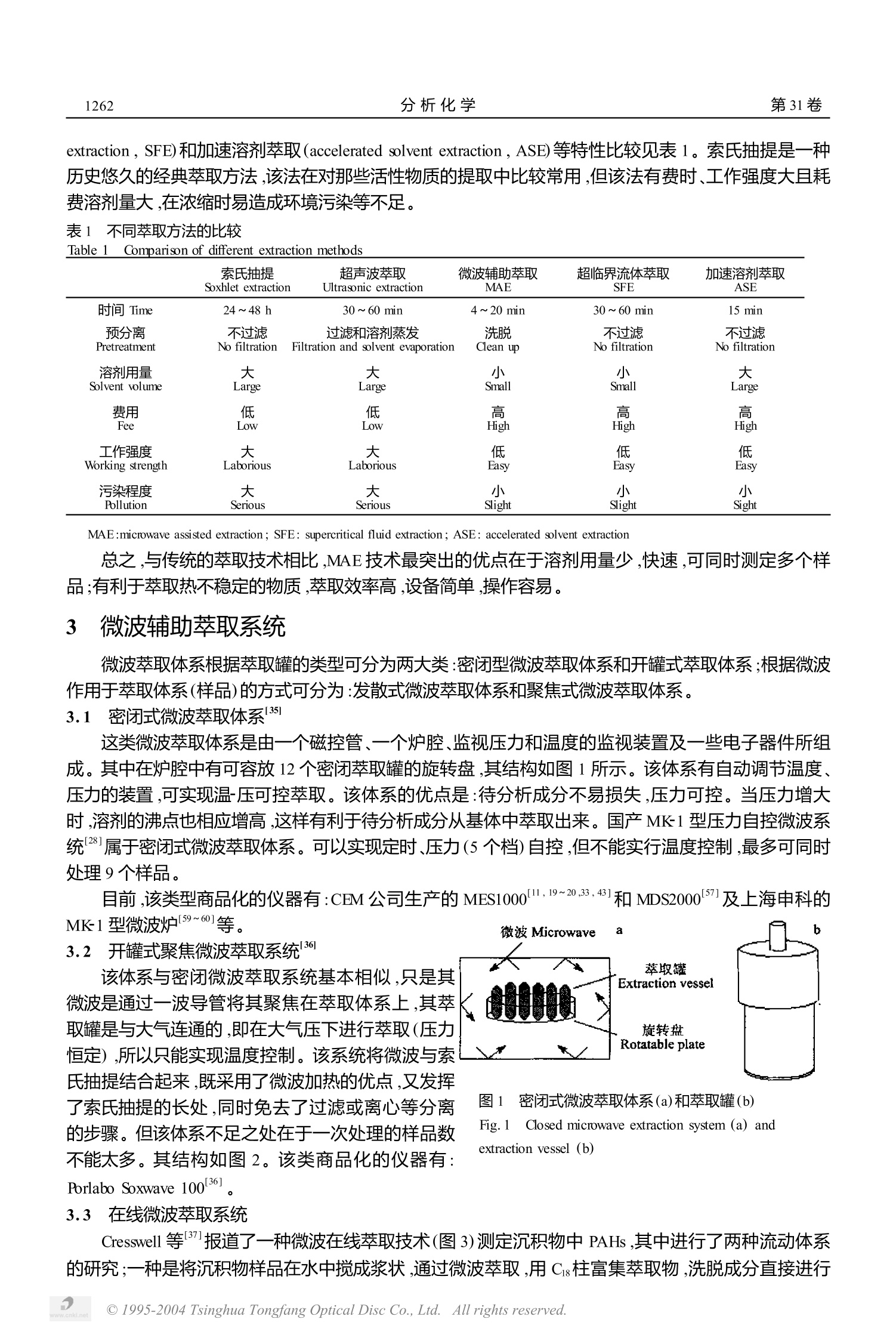
第31卷2003年10月分析化学 (FENXI HUAXUE) 评述与进展Chinese Journal of Analytical Chemistry第10期1261~1268 第31卷1262分析化学 微波辅助萃取技术的进展 李 核 李攻科 张展霞 (中山大学化学与化学工程学院,广州510275) 摘 要 介绍了微波辅助萃取技术的特点和装置,综述了近年来微波辅助萃取技术在环境分析和药物提取中的应用,并展望了微波辅助萃取技术的应用前景和发展方向。引用文献74篇。 关键词 微波辅助萃取,样品预处理,评述 引 言 样品的预处理是样品分析最为关键的步骤之一,尤其是分析复杂的样品时,样品的预处理是必不可少的。所以,发展快速、高效的样品前处理方法是分析家们一直追求的目标。传统的样品前处理的方法如索氏抽提、超声波萃取等不仅费时,而且溶剂的消耗量大。微波辅助萃取(microwave assisted extraction,MAE)具有快速、高效、省溶剂、环境友好等优点。微波技术开始主要是用于无机分析的样品预处理即微波消化,从1986年起微波能开始应用到有机分析中的样品预处理即微波辅助萃取。十几年来,MAE技术在有机分析中得到了广泛的应用。本文综述 MAE 技术在样品预处理中的应用,并展望了其发展前景。 2 微波特点 2.1 MAE特点 MAE是指利用微波能强化溶剂萃取效率,即利用微波加热来加速溶剂对固体样品中目标萃取物(主要是有机化合物)的萃取过程。微波具有波动性、高频特性以及热特性或非热特性(生物效应)等特点14] 2.1.1 快速高效 样品及溶剂中的偶极分子在高频微波能的作用下,以10/s圈的速度变换其正、负极 ,产生极极涡流、离子传导和高频率摩擦,从而在短时间内产生大量的热量。偶极分子旋转导致的弱氢键破裂、离子迁移等加速了溶剂分子对样品基体的渗透,待分析成分很快溶剂化,使微波萃取时间显著缩短。 2.1.2 加热均匀 微波加热是透入物料内部的能量被物料吸收转换成热能对物料加热,形成独特的物料受热方式,整个物料被加热,无温度梯度,即微波加热具有均匀性的优点。 2.1.3 微波加热具有选择性 微波对介电性质不同的物料呈现出选择性的加热特点,介电常数及介质损耗小的物料,对微波的入射可以说是“透明”的。溶质和溶剂的极性越大,对微波能的吸收越大,升温越快,促进了萃取速度。而对于不吸收微波的非极性溶剂,微波几乎不起加热作用。所以,在选择萃取剂时一定要考虑到溶剂的极性,以达到最佳效果。 2.1.4 生物效应(非热效应) 由于大多数生物体内含有极性水分子,在微波场的作用下引起强烈的极性震荡,从而导致细胞分子间氢键松弛,细胞膜结构电击穿破裂,加速了溶剂分子对基体的渗透和待提取成分的溶剂化。因此,利用MAE 从生物基体萃取待分析的成分时,能提高萃取效率。 2.2 MAE 技术与其它技术的比较 任何一种萃取技术都是为了从基体中快速、高效地分离出待分析成分,但是由于基体的复杂性及萃取技术的不同特点,常常在选取萃取方法的时候必须考虑到分析的目的和分析方法的费用、操作的繁简、时间的多寡等因素。其它方法如超声波萃取(ultrasonic extraction)、超临界流体萃取(supercritical fluid ( 2002-06-08收稿:2002-12-14接受 ) ( 本文系国家重点基础研究发展规划(No. G2000026302)、教育部留学回国人员科研启动基金和广东省自然科学基金博士启动基金(No. 974078)资助项目 ) extraction, SFE) 和加速溶剂萃取(accelerated solvent extraction, ASE) 等特性比较见表1。索氏抽提是一种历史悠久的经典萃取方法,该法在对那些活性物质的提取中比较常用,但该法有费时、工作强度大且耗费溶剂量大,在浓缩时易造成环境污染等不足。 表1:不同萃取方法的比较 Table 1 Comparison of different extraction methods 索氏抽提 超声波萃取 微波辅助萃取 超临界流体萃取 加速溶剂萃取 Soxhlet extraction Ultrasonic extraction MAE SFE ASE 时间 Time 24~48 h 30~60 min 4~20 min 30~60 min 15 min 预分离 不过滤 过滤和溶剂蒸发 洗脱 不过滤 不过滤 Pretreatment No filtration Filtration and solvent evaporation Clean up No filtration No filtration 溶剂用量 大 大 小 小 大 Solvent volume Large Large Small Small Large 费用 低 低 高 高 高 Fee Low Low High High High 工作强度 大 大 低 低 低 Working strength Laborious Laborious Easy Easy Easy 污染程度 大 大 小 小 小 Pollution Serious Serious Slight Slight Sight MAE:microwave assisted extraction; SFE: supercritical fluid extraction; ASE: accelerated solvent extraction 总之,与传统的萃取技术相比,MAE 技术最突出的优点在于溶剂用量少,快速,可同时测定多个样品;有利于萃取热不稳定的物质,萃取效率高,设备简单,操作容易, 3 微波辅助萃取系统 微波萃取体系根据萃取罐的类型可分为两大类:密闭型微波萃取体系和开罐式萃取体系;根据微波作用于萃取体系(样品)的方式可分为:发散式微波萃取体系和聚焦式微波萃取体系。 3.1 密闭式微波萃取体系35 这类微波萃取体系是由一个磁控管、一个炉腔、监视压力和温度的监视装置及一些电子器件所组成。其中在炉腔中有可容放12个密闭萃取罐的旋转盘,其结构如图1所示。该体系有自动调节温度、压力的装置,可实现温-压可控萃取。该体系的优点是:待分析成分不易损失,压力可控。当压力增大时,溶剂的沸点也相应增高,这样有利于待分析成分从基体中萃取出来。国产MK-1型压力自控微波系统281属于密闭式微波萃取体系。可以实现定时、压力(5个档)自控,但不能实行温度控制,最多可同时处理9个样品。 前,该类型商品化的仪器有:CEM公司生产的 MES1000[11,19~20,33,43]和MDS2000571及上海申科的MK1型微波炉I59~60]等。 3.2 开罐式聚焦微波萃取系统 该体系与密闭微波萃取系统基本相似,只是其微波是通过一波导管将非聚焦在萃取体系上,其萃取罐是与大气连通的,即在大气压下进行萃取(压力恒定),所以只能实现温度控制。该系统将微波与索氏抽提结合起来,既采用了微波加热的优点,又发挥了索氏抽提的长处,同时免去了过滤或离心等分离的步骤。但该体系不足之处在于一次处理的样品数不能太多。其结构如图2。该类商品化的仪器有:Porlabo Soxwave 10036] 图 1 密闭式微波萃取体系(a)和萃取罐(b) Fig.1 Closed microwave extraction system (a) andextraction vessel (b) 3.3 在线微波萃取系统 Cresswell等报道了一种微波在线萃取技术(图3)测定沉积物中 PAHs ,其中进行了两种流动体系的研究;一种是将沉积物样品在水中搅成浆状,通过微波萃取,用Ci8柱富集萃取物,洗脱成分直接进行 4 微波萃取的应用 4.1 多环芳烃(PAHs) PAHs 是一类广泛存在于环境中的有机污染物,由于 PAHs 具有致癌和诱变性,对人类危害较大,所以PAHs 的分析测定引起了人们的高度重视。关于 HPLC分析;第二种方法是样品在丙酮中被搅成浆状,通过微波萃取,用10 mL正己烷富集从微波炉流出液中待分析成分,然后用 GC/MS进行定性、定量分析。此外, Ericsson 等551采用了动态微波辅助萃取(dynamic microwave-assisted extraction: DMAE),该体系在萃取过程中可以不断的让新鲜的溶剂进入萃取罐,而萃取物可以通过 HPLC进行实时监测。 图3 在线微波萃取体系 Fig.3 Schematic diagram of onrline microwave system 测定 PAHs 的样品前处理技术,从经典的索氏抽提到超声波萃取萃1.,再到新近发展的超临界流体萃取、固相微萃取及 MAE 56~58,15]等均有报道。由于 MAE 具有快速、溶剂消耗量少、节省能源等优点,其发展速度尤为迅速。Vazquez 等1301对微波萃取海洋沉积物中 PAHs 的条件进行了优化,采用丙酮/正己烷(1:1)为萃取剂,在微波功率500W的条件下,萃取6 min ,PAHs的回收率为92%~106%,而传统的索氏抽提需8h以上。Pino 等通过二水平因素设计实验对海洋沉积物中PAHs 的萃取进行了优化,然后用高效液相色谱/紫外检测器进行检测,对于三环以上的 PAHs,其平均回收率为85.7%~100.73%。有关的报道还有土壤15~16,29]沉积物[17,36~38,56,57]、植物[30,58]、颗粒物及生物组织等。 萃取剂对萃取效率有很大的影响。有关萃取剂如二氯甲烷、正己烷/丙酮、丙酮、石油醚、甲苯/丙酮及水等。而以有机溶剂为萃取剂的报道较多,以水为萃取剂的报道较少,主要是由于水与许多有机物不溶,虽水对微波有较强的吸收,但使用范围有限。 Tomaniova 等501采用正己烷/丙酮(32,V/V)作为花粉、云杉针中 PAHs 的萃取剂,并且与超声波萃取进行了对照。Budzinski 等51研究了土壤和沉积物中水分含量对萃取效率影响,指出适当增加样品中水分含量可以提高萃取效率,在水分含量为20%~30%时萃取效率最高,而在这范围之外其萃取效率均有所下降。该方法不需样品干燥的步骤,可以用于现场湿样分析。对于不同基体的 PAHs的萃取研究,多数工作集中在萃取剂的选择、用量、微波功率、萃取时间优化,水分含量对萃取效率的影响研究。 Letellier 等381研究了基体颗粒的大小对萃取效率的影响,发现水分含量对每个组分萃取效率影响并不相同。水分含量对细颗粒(<40um)和含碳量高的土壤颗粒萃取效果影响不大,而对粗颗粒(40~300 um)和含碳量低的颗粒萃取效率影响较大。文献114,18,19]采用不同的方法萃取土壤中 PAHs,其中MAE的萃取效率高于索氏抽提而低于超临界萃取。 4.2 多氯联苯及农药残留 Viorica等采用MAE 和 GC/MS、酶联免疫吸收法(ELISA)联用测定土壤、沉积物中多氯联苯(PCBs) ,该方法与索氏抽提相比,所用时间和溶剂用量都大大减少。而且建立的方法适合于现场样品分析。 Pastor等采用甲苯为萃取剂研究了沉积物中19种PAHs、4种DDTs 和6种 PCBs,优化萃取条件,研究了样品重量与萃取剂的体积之比的关系对萃取效率的影响,当二者之比大于13时,萃取效率最高。其次,MAE 还被用于测定环境水样中PCBs,在样品中加入氯化钠,以增加传热的速率,从而提高萃取效率。 李攻科等1591采用微波皂化萃取气相色谱法测定生物样品中的 PCBs。为消除有机氯农药(OCPs)对测定土壤中 PCBs 的干扰,采用微波碱解法将土壤样品中的OCPs 碱解,在优化后的条件下能完全消除HCH, 滴滴涕(DDT),滴滴滴(DDD)的干扰 ,DDE, 艾氏剂(Aldrin),狄氏剂(Dieldrin)的干扰也减少,经浓硫酸处理后狄试剂的干扰完全消除1601]601。熊国华等31在应用微波萃取不同基体中 PCBs、PAHs 等方面也进行了大量的工作。 MAE 用于有机氯农药残留组分的测定研究,分析对象主要有植物土壤[11,18,42]等。使用的萃取剂主要有水[10]正己烷丙酮和甲醇等。其中用有机溶剂萃取基体中除草剂的研究最多,而以水为萃取剂的研究较少,熊国华等采用水为萃取剂萃取土壤中的中去津,回收率为73.4%。以水作为一种萃取剂,对水溶性大的化合物的萃取效果好,而对水溶性不大的化合物的萃取效率并不高。但其最大的优点是一种价廉、安全、无污染的溶剂。若能通过加入某些物质来提高萃取效果,则它将势必引起萃取方法的巨大变革。 Stout 等通过 MAE 萃取土壤中的咪唑啉杀虫剂,然后通过Cl8柱洗脱进行GC/ECNCI测定,不但使检出限达到1 ug/L 级,还大大简化了萃取后的工作量。Hoogerbrugge对土壤中三嗪的萃取条件优化,建立了多因素的萃取模型,并用实验验证。Garcia-Ayuso.等利用微波-索氏萃取联用装置萃取土壤中除草剂。该萃取体系不但发挥了微波快速加热的的优点,也发挥了索氏抽提的长处。能用于所有适合于索氏抽提的样品萃取分析。有关微波萃取环境基体中 OCPs 的应用见表2。 表2 微波辅助萃取在测定环境样品中有机氯农药残留中的应用 Table 22Application of MAE for the determination of organochlorine pesticides (OCPs) in environmental matrices 样品类型 萃取体系 萃取条件 回收率 文献 Sample type System (Model) Extraction condition Recovery (RSD,%) Ref. 5 g样品(smaple) ,30 mL 己烷/丙酮 沉积物/土壤 Soils/Sediments 密闭罐萃取体系 Closed vessel system (MES1000 ,CEM) (hexane/acetone) (1:1), 115℃,1000 >70 2 W,10 min 密闭罐萃取体系 海洋沉积物 Marine sediments Closed vessel system 己烷/二氯甲烷(hexane/dichlorometh- ane) (1:1) (2~11) 9 (MES1000 ,CEM) 密闭罐萃取体系 5g样品(sample),己烷/丙酮(hexane/ 沉积物 Sediment Closed vessel system acetone) (1 :1),100℃,50%的最大 70.6~90.6(2~8) 32 (MES1000 ,CEM) 功率(maximum power) , 10 min 沉积物 Sediments 家用微波炉 Domestic oven 2~10g样品(sample), 1 mL 水 (water), 甲苯(methyl benzene), 660 W,6 min 97~102 38 污泥 Sewage sludge 开罐式萃取体系 Open vessel system (Soxwave100, Prolabo) 30 mL 己烷/丙酮(hexane/acetone) (1: 1), 30 W, 10 min 88~105 (21~39) 39 河床沉积物River sediments 密闭罐萃取体系 Closed vessel system MLS1200(Milestone) 5g样品(sample), 30 mL 己烷/丙酮 (hexane/acetone) (1 :1) ,500 W,15 min 81~87 (2~5) 40 密闭罐萃取体系 25 mL 1 mol/L KOH 的甲醇溶液 92~98 生物样品 Biological sample Closed vessel system (MK-1) (methanol solution)+己烷 (hexane) (1 :1,V/V), 600 W, 4 min (2.3) 41 4.3 酚类化合物 苯酚及其衍生物在化学工业、纺织业、药物生产及染料生产中有广泛应用。酚类化合物在农业上也广泛应用于杀虫剂、杀真菌药等。这类化合物具有高度的亲水性,所以成了土壤、地下水的潜在污染物。 由于这类化合物具有毒性对人类健康影响极大,美国环境保护局将其中11种酚类化合物列为主要的环境污染物。 Egizabal 等33通过实验设计对微波萃取条件进行了优化,并与索氏抽提进行了对照。MAE 采用正己烷/丙酮(1:1,V/V)15 mL 在萃取罐压力为0.18 MPa,微波功率为最大功率44%的条件下萃取16.5min。而索氏抽提采用萃取剂正己烷/丙酮(73,V/V)200 mL回流8h。结果表明:MAE萃取效果普遍比索氏萃取好。但对于2-甲基苯酚的萃取效率较低,作者认为这种现象是由于烷基团与基体相互作用而造成的。Llompart过通过因子设计对微波萃取条件进行了优化,并与超声波萃取进行了对比,苯酚、邻、间、对-甲苯的回收率比超声波萃取高近1倍。此外,Llompart等201对不同基体中苯酚、邻、间、对-甲苯4种物质用SFEMAE和超声波萃取进行了对照实验。并且比较了含碳量不同的基体对萃取效率的影响,随着基体活性碳含量的增加,萃取效率有所下降。另外,MAE和超临界萃取比超声波萃取效率要高2倍以上。 Pedersen等*采用开罐式微波萃取鱼组织中的酚类物质,其检出限可达0.1 mg/L;而 Llompart 等在采用密闭罐萃取体系萃取土壤中酚类化合物,在130℃下以9mL正己烷,1mL乙酸酐/吡啶(4:1)为萃取剂,功率为1000 W的条件下萃取30 min,其萃取效率在90.5%~112.1%之间;RSD 在3.7%~7.4%之间。 4.4 有机金属化合物 目前,微波萃取环境样品中有机金属的报道有有机锡、有机汞有机砷及其形态[34,44,61]分析。文献将沉积物于密闭萃取罐中在120℃下,用6 ml/L HC处理,然后微波辐射10 min 或在开放式萃取罐(常压下)以60W功率微波辐射3 min 后,再用2 mol/L HCl 和2 mol/L HNO;处理均取得较好的结果。文献22.45对沉积物中甲基汞的萃取进行了一系列的研究。首先,对影响甲基汞萃取的条件进行了因子设计优化,其中温度和盐酸的用量是影响萃取的重要因素。在优化的条件下,方法检出限达8ng/g。此外,还对传统的萃取方法和 MAE 方法进行了对比研究4. 4.5 药物有效成分 MAE 技术应用于中草药的有效成分和植物细胞中活性物质的提取是它一个新的应用领域。目前,MAE技术在该领域的应用报道还不多,主要应用有从灵芝、云芝、猴头等高等真菌菌丝体中提取多糖以及从中药中提取白藜芦醇和从茶花粉、银杏叶、人参、喜树果等植物组织中提取药用成分621,但由于微波加热的特点所限,微波在生物细胞内有效成分的提取方面还存在着许多问题。首先,只适用于对热稳定性的产物,如寡糖,多糖、核酸、生物碱、黄酮、苷类等中药成分,而对热敏性物质,如蛋白质、多肽、酶等微波加热易导致它们变性失活;其次,要求被处理的对象具有良好的吸水性或者要求待分离的成分处于富含水的部位,否则,待分析的成分难以迅速释放出来。 范志刚等研究了 MAE 对雪莲中黄酮浸出量影响1631和麻黄中麻黄碱浸出量影响1641以及对槐花中芸香甙浸出量影响响[65]李学坚等166]对微波浸提技术和传统提取技术(回流提取法、水蒸汽蒸馏法)提取丁香油的提取效率进行了对比研究。结果表明:微波浸提技术比溶剂回流提取法选择性高,比常规的煎煮法和水蒸汽蒸馏法萃取效率高,微波浸提技术优越性是比较明显的。 韩玉芬等’首次报道采用MAE的芦荟提取物对水稻纹枯病、苹果轮纹病、小麦赤霉病、蕃茄早疫病、花生褐斑病等5种病菌有不同程度的抑菌活性,微波协助提取与常规方法比较,前者具有提取充分、省时的优点,且某些微波提取液的抑菌活性高。 总之,微波应用于环境分析已经比较成熟,但在药物的有效成分的提取应用还刚起步,许多问题还尚待进一步研究。 4.6 其它应用 文献4比较了压力流体萃取和常压微波萃取聚丙烯添加剂。李攻科等1081利用微波技术,研究了用KOH甲醇、HSO4-甲醇-甲苯、HCl-甲醇等不同体系对食用油中的脂肪酸进行衍生化,系统地比较了它们的优、劣势,以及适合的分析对象。在1 min 内完成衍生化反应,选用正庚烷代替传统方法的苯/石油醚作为脂肪酸甲酯的提取剂。 李攻科等就MAE 技术与其它样品前处理技术联用进行了一系列的研究。如微波辅助皂化-气相色谱-质谱联用(GC-MS)测定血清中胆固醇7],微波技术消解衍生化气相色谱-质谱法(GC-MS)快速测定鲨鱼软骨中脂肪酸9。在测定血清中胆固醇时以 KOH甲醇溶液为皂化液,在600W微波功率下辐射30s皂化血清样品,正庚烷为提取液。通过与水浴皂化法、酶学分光光度法比较,表明该法快速、溶剂用量少、准确、重现性好,方法的检出限为0.011 mg,特别适用于生物、食品、体液等大量样品中胆固醇的测定。在测定鲨鱼软骨中脂肪酸时,以盐酸-甲醇(体积比为14)体系作消解衍生化溶液,在600W微波功率作用下加热4 min ,将样品的消解、脂肪酸的衍生化及脂肪酸甲酯的萃取融于一体,该法适用于大批量固体样品中脂肪酸的测定。 李攻科等发展的微波碱解法159~601和微波辅助皂化法471的应用,将微波萃取技术与碱解、皂化等前处理方法相结合,既消除了基体中杂质对分析组分的干扰,又简化了对萃取物在萃取后的分离工作,直接在萃取过程中将一些不易挥发的化合物衍生化然后对其进行分析,大大缩短了萃取及萃取后的处理时间。MAE除了在上述方面的应用外,还在食品及材料添加剂等17,12,13,[72,123,13~,23~26,448~851,~705,711],70,11]方面也有很广泛的应用,随着MAE技术的发展,在有关MAE 的综述[3,52~54,72,73]和专著127]中也对MAE原理、装置、影响因素及其应用作过阐述。 5 展 望 (1)MAE与其它消除干扰的方法如皂化、碱解等相结合是很有前途的;(2)实现微波萃取与分析检测仪器的在线联用、自动化将是 MAE 技术在分析化学中的又一发展方向;(3)MAE技术应用于中草药中有效成分的提取是极有发展的前途;(4)采用水、活性表面剂作为MAE的萃取剂是很有发展前景的,它不仅价廉,而且对环境无污染,若能通过添加其它无毒、无污染的试剂改善其对有机成分的萃取效果,这将大大推动有机分析的发展。此外,由于MAE具有快速、高效节能、环境友好等特点,是很有发展前途的样品前处理技术,但对其机理的研究还不够,远不如微波消解完善,研究其机理不仅可以更好地了解 MAE ,也为进一步开发研制仪器提供理论基础,为建立如微波消解那样完善的分析方法奠定基础。因此,关于MAE的理论研究也是一个重要的发展方向。 ( References ) ( 1 Ganzler K, Salgo A, Valk o KJ. J. Chromatogr . A, 1986, 371:299~306 ) ( 2Lopez AV, Young R, Beckert W F. Anal. Chem.,19 9 4, 66(7):1097~1106 ) ( 3Jocelyn Pare R, B l a nger M R . S t afford S S. T . Trends Anal. Chem., 1994, 13(4):176~184 ) ( 4 Dean J R , Barnabas IJ, Fowlis I A . Anal. Proc., 1995,32(8) : 305~308 ) ( 5 LopezAila V, B enedicto J , Charan C, Young R, Beckert W.F. Environ. Sci . & Tech., 1995, 29(10) :2709~2712 ) ( 6 Onuska F I, Terry KA. J. H igh Resolut . Chromatogr . ,1995, 1 8(7):417~421 ) ( 7 YoungJ C. J. Agric. Food Chem.,1995, 4 3(11):2904~2910 ) ( 8 Chee K K, Wong M K,Lee H K. J. Chromatogr. A, 1996,723(2):259~271 ) ( 9 Chee K K , W ong M K , L e e H K . J . Chromatogr. A , 1996, 736(1-2): 2 11~218 ) ( 10 Stout SJ , DaCunha A R , P icard GL , Safarpour M M. J. A gric. F ood. Chem., 1 996, 44 ( 11):35 4 8~3553 ) ( 11 Stout SJ, daCunba A R, Allardice D G . Ana . Chem., 1996, 68(4):653~658 ) ( 12 Chee K K, Wong M K, Lee H K. Ch r omatographia , 1996,42(7):3 7 8~384 ) ( 13 Carro N, Garcia C M, Cela R. Analyst,1997,122(4) : 325~329 ) ( 14 Hu Guanjiu(胡冠九), Xu Minghua(徐明华). Jiangsu Environmental Sci e nce & Technology(江苏环境科技),1997,1:31~33.36 ) ( 15 Rodriguez I , Santamarina M, Bollain M . H, M e juto M . C, Ce l a R. Sp e ctroscopy-An In t ernational Journal, 19 97,13 ( 1): 5 1~59 ) ( 16 Saim N, Dean J R, Abdullah M P, Abdullah M P ,Zakaria Z J . Chromatogr. A,1997,791(1-2):361~366 ) ( 17 Pastor A, Vazquez E, Cioscar R, Guardia M. Anal. Chim. Acta , 1997, 344(3):241~249 ) ( 18 Hoogerbrugge R, Molins C, Baumann R A. Anal. Chim. Acta, 1997, 348(1-3) : 247~253 ) ( 19 Llompart M P, Lorenzo R A, Cela R, Jocelyn Pare J R . Analyst, 1997, 122(2):133~137 ) ( ◎ 1995-2004 Tsingh u a Tongfa ng Op t ical Disc Co . , Lt d . Al l rights reserved. ) ( 20 Llompart M P, Lorenzo R A, C ela R,Li K, B eanger M R , Jocelyn 0Pare R . J . C hromatogr. A , 1 997, 774(1-2):2 4 3~251 ) ( 21 Llompart M P ,Lorenzo RA, Cela R , Jocelyn P ardJ R, B anger J M R,Li K . J . Ch romatogr. A,1 9 97,757(1-2):153~164 ) ( 22 Vazquez MJ, Carm AM, L o renzo RA, C e la R. A nal. C hem., 1997,69(2):221~225 ) ( 23 Incorvia-Mattina MJ , IannucciBerger W A, Denson CL. J. Agric. Food Chem.,1997,45(12 ) :4691~4696 ) ( 24 Carro N, Garcia C M, Cela R. Spectroscopy, 1997, 13(1):61~70 ) ( 25 Frost S P, Dean J R, Evans K P, H arradine K, Cary C, Combed M H I. Analyst, 19 97,122(9):895~898 ) ( 26 Daghbouche Y, Garrigues S, Rubiol A M, Guardia M . Anal . Chim. Acta, 1997, 345(1-3):161~171 ) ( 27 Kingston HM , H a s well SJ . Mir o wave Enhanced Chemistry- Fundamentals , Sa m ple Prep a ration and Application. Was h ington DC:American Chemical S o ciety , 1997 :569~605 ) ( 28 Xiong Guohua(熊国华), Liang Jinming(梁今明), Z o u Shichun(邹世春),He Xiaoqing(何小青) , Zh a ng Zhanxia(张展霞).Chemical Journal of Chinese Universities (高等学校化学学报) ),1998,19(10):1560~1565 ) ( 29 Garcia-Ayuso L E, Sanchez M, F ern ddez de Alba A, Luque de C astro M D. Anal. Chem., 1 998,70(11):2426~2431 ) ( 30 T omaniov aM, Hajslov aJ, PavelkaJr J, Kocourek Ⅴ, HoladovaK, K movaI. J. Chromatogr. A, 1998, 827(1) :21~29 ) ( 31 Xiong G H, Liang J M, Zou S C, Zhang Z X . Anal. Chim. Acta, 1998,371:97~103 ) ( 32 Silgoner I, Krska R, Lombas E, G ans O, Rosenberg E, G r asserbaner M. F r esenius J . A nal. Chem., 1 9 98, 362(1):120 ~ 124 ) ( 33 Egizabal A, Zuloaga O , E txebarria N , Fern andez L A , Madariage J M . Analyst , 1998, 123(8) : 1 679~1684 ) ( 34 Dagnac T, Padro A, Rubio R, Raure t G. Anal . Chim . Acta, 1998, 364(1-3 ) :19~30 ) ( 35 Akiko Tannabe, Shiperu Suzuki . Anal. Chem.,1999,48(10):939~944 ) ( 36 Budzinski H, Letellier M,Garrigues , Menach L K. J. Chromatog r . A,1999,837(1-2):187~200 ) ( 37 Cresswell SL, Haswell SJ. Analyst, 1999, 124(9):1361~1366 ) ( 38 Letellier M, Budzinski H . Analyst, 1999, 124(1 ) :5~14 ) ( 39 Carro N, Sasvedra Y, Garcia I , Hompart M . J . Microcolum . Sep., 1999, 11(7 ) :544~549 ) ( 40 Dupont G , Delteil C, Camel V, B ermond A. Analyst, 1999, 124(4):453~458 ) ( 41 Cencic K Z, Marsel J . Chromatographia, 1999, 49(1-2) : 2 1~27 ) ( 42 Xiong G H, T ang B Y , Zhang Z X. Ta lanta, 1 999,4 8 (2):3 3 3~339 ) ( 43 Pedersen S N, Lindholst C . J. Chromatogr . A , 1999, 864(1 ) :17~24 ) ( 44 Ackley KL , B'Hyncer C, Sutton KL , Caruso J A. J . Anal. Atoms. Spectr., 1999,14(5):845~850 ) ( 45 Lorenzo R A, Vazquez MJ, Carro A M, Cela R. Trends Ana l. Chem . ,1999, 18(6):410~416 ) ( 46 Vandenburg H J, C l ifford A A, Bartle KD, C a rroll J , Bewton I D . A nalyst,1999, 1 2 4(3):397~400 ) ( 47 Li Gongke(李攻科), He Xiaoqing(何小青), Yang Yun(杨 云), Z hang Zhanxia(张展霞), S ong Shaoyun(宋少云), Zhang ) ( Meiyun(张美云). Journal of Instrumental Analysis (分析测试学报),1999,18(3):15~18 ) ( 48 Garcia AL E , Velasco J, Dobarganes M C, Lugue De Castro M D. J. Agric. Food Chem. , 1999, 4 7(6): 2 308~2315 ) ( 49 Youngman MJ, G reen D B. Talanta, 1999,48(5):1203~1206 ) ( 50 Eskilsson C S, Bjorklund E, Mathiasson L, Karlsson L, Torstensson A. J. Chromatogr. A , 1999,840(1):59~70 ) ( 51 Garcia-Ayuso L. E , Luque- de-Castro M. D . Anal. Chim. Acta, 1999,382(3):309~316 ) ( 52 LopezAvila V. Critical Re v . Ana l . Chem. ,1999,29(3):195~230 ) ( 53 Luque de Castro M D, Jim tez-Carmona M M, Fern indez P @ez V . Trends Ana l . Che m ., 1999, 18(11):706~ 7 16 ) ( 54 Lorenzo R Z, V aquez MJ, Carro A M , Cela R . Trends Anal. Chem., 1999,18(6):4 1 0~416 ) ( 55 Ericsson M, Colmsjo A . J. Chromatogr. A, 2 000, 877:141~151 ) ( 56 Vazquez B E , L o pez M P, L op ez Mahia P, M un i ategui-Lorenzo S, Pra d a Rodriguez D, Fer n andez Fernandez. E. Fresenius' J . Anal . Chem.,2000,366(3):283~288 ) ( 57 Pino V , Ayala J H, Afonso A M, Gonzalez V. J. C h romatogr. A , 2 000,869(1-2):515~522 ) ( 58 Pensado L , Casais C, Mejuto C, Ce l a R. J . Chromatog r .A, 2000, 869(1-2):505~513 ) ( 59 Li Gongke(李攻科), He Xiaoqing(何小青), Y ang Yun(杨 云), Zhang Zhanxia(张展霞). Chinese J. Anal. Chem. (分析 化学) : ) ,2000,28(9) :1186 ) ( 60 He Xiaoqing(何小青),Li Gongke(李攻科), Xiong Guohua(熊国华), Zhang Zhanxia(张展霞).Chinese J. A nal. C hem.(分析化学),2000,28(1):26~30 ) ( 61 GomezAriza J L, SanchezRodas D, Giraldez I, Morales E . Analyst,2000, 125(3):401~407 ) ( ◎ 1995-2004 Tsingh u a Tongfa ng Op t ical Disc Co . , Lt d . Al l rights reserved. ) ( 62 Zhang Daijia (张代佳) , Liu Chuanbin(刘传专), Xiu Zhilong(修志龙), Chang Zengyi(昌增益). Chinese Traditional an d Herbal Drugs(中草药) , 2000,31(9):附5~6 ) ( 63 Fan Zhigang(范志刚), Yang Libin(杨莉斌), Kuang L i ping(匡丽萍). Journal of Medicine & Pharmac y of Chinese Minorities (中国民族医药杂志),2000,6(1):43~44 ) ( 64 Fan Zhigang(范志刚), Zhang Yuping(张玉萍),Sun Y an(孙 燕), Kuang Liping(匡丽萍), Yang Libin(杨莉斌). ChineseTradition a l Patent Medicine(中成药 ) ,2000,22(7):520~521 ) ( 65 Fan Zhigang(范志刚),Li Yulian(李玉莲), Y ang Libin(杨莉斌), Kuang Liping(匡丽萍). Pham. J. Chin . PLA(解放军 药学学报),2000,16(1):36~38 ) ( 66 Li Xuejian(李学坚), H u a ng Haibin(黄海滨). Guang x i Journal of Traditional Chinese Medicine(广西中医药),2000,25(3) : 49~50 ) ( 67 Han Yufen(韩玉芬), Wang Yinshu(王银淑), Zhang Chunxiang(张春香),Liu Zhun(刘 准). A c ta Scientiarum N aturalium Universitatis Nankaiensis (南开大学学报<自>),2000,33(2):124~126 ) ( 68 Li Gongke(李攻科),He Xiaoqing(何小青) , Zhang Zhanxia(张展霞). Chinese Journal of Analysis Laboratory (分析试验室) , 2000, 19 (1):16~19 ) ( 69 Li Gongke(李攻科), H e Xiaoqing(何小青), Zhang Zhanxia(张展霞). Chin e se Journal of Chromatography(色谱),2000, 18(4):337~339 ) ( 70 Marcato B, Vianello M. J. Chromatog r . A,2000,869(1-2) : 285~300 ) ( 71 Simoneau C , N audin C , Hannaert P , Anklam E . F o od Research International, 2000, 33:733~741 ) ( 72 Camel V. T rends Anal . Chem., 2000, 19(4):229~248 ) ( 73 Zhang Z X, Xiong G H , Li G K, He XQ. Anal. S ci.,2000,16 ( 2):221~224 ) ( 74 Li Gongke(李攻科), H e Xiaoqing(何小青), Y ang Yun(杨 云), Z h ang Zhanxia(张展霞). Journal of Instrumental Analysis (分析测试学报),2001,20(1):1~3 ) Development of Micro wave Assisted Extraction Li He, Li Gongke, Zhang Zhanxia (School of Chemistry and Chemical Engineering, Sun Yat sen University, Guangzhou 510275) Abstract The fundamental and recent advances of microwave assisted extraction (MAE) with its applications inenvironmental analysis and pharmaceutics are reviewed. Its prospect is also described. 74 references are cited. Keywords Microwave assisted extraction, sample pretreatment, review (Received 8 June 2002 ; accepted 14 December 2002) 欢迎订阅2004年《生态环境》 《生态环境》是经国家科技部批准的正式学术期刊,向国内外公开发行。刊号:ISSN 1672-2175;CN44-1565/X。1992年创刊。入选中国核心期刊(选)数据库、中国科学引文数据库;被评为广东省优秀期刊、广东省优秀科技期刊、全国优秀农业期刊(一等奖)、中国学术期刊(光盘版)规范优秀期刊。主要刊登国内外生态学、环境科学及其相关领域具有创新性的重要研究论文,以及对热点问题和前沿问题富有启发性的高水平的综述。刊登内容广泛,是一种多学科互相渗透和互相综合的刊物。适合从事生态学、环境学、资源保护、土壤学、大气科学、水科学、地理学、地质学、地球科学、农业科学、林学、医学、社会科学、经济科学等广大领域的科技人员、学者、教师、学生各级管理者和环境爱好者阅读。 本刊全铜版纸精美印刷,季刊,大容量,大16开,正文150页/册,定价12.50元/册,全年定价50元(含邮资)。邮发代号 46-272,欢迎订阅。如错过邮局订阅期限,可直接向编辑部订阅。 邮局汇款:广州市天河区天源路808号广东省生态环境与土壤研究所《生态环境》编辑部,邮编510650。 银行汇款:开开银行:中国工商银行广州市沙河办事处,帐号:3602002709002419786,收款单位:广东省生态环境与土壤研究所。 本刊网址 :http://www. eco-environment. com;电子信箱 :editor @ecor environment. com;电话:(020)87024961 ◎Tsinghua Tongfang Optical Disc Co., Ltd. All rights reserved.
关闭-
1/8

-
2/8
还剩6页未读,是否继续阅读?
继续免费阅读全文产品配置单
上海新仪微波化学科技有限公司为您提供《微波辅助萃取技术中发展历程检测方案(微波萃取仪)》,该方案主要用于其他中发展历程检测,参考标准《暂无》,《微波辅助萃取技术中发展历程检测方案(微波萃取仪)》用到的仪器有null。
我要纠错
相关方案


 咨询
咨询