[摘 要] 目的:建立并验证了用高效液相色谱法测定饮料中三种食品添加剂的检测方法;方法:采用色谱柱(XB-C18,4.6mm×250mm,5μm),0.02mol/L乙酸铵(pH约为6.0)-甲醇为流动相(V/V=15/85),柱温30℃,流速1.0ml/min,检测波长230nm,以相对保留时间定性,色谱峰面积定量;结果:该方法平均回收率为98.59%~102.13%,相对标准偏差RSD%为0.978%~1.254%,检测限(S/N=3)为0.037~0.092mg.kg-1;结论:实验表明该方法对饮料中食品添加剂的检测快速、简便、可操作性强。
[关键词]高效液相色谱法;饮料;食品添加剂
高效液相色谱法测定饮料中的苯甲酸、糖精钠、山梨酸
[摘 要] 目的:建立并验证了用高效液相色谱法测定饮料中三种食品添加剂的检测方法;方法:采用色谱柱(XB-C18,4.6mm×250mm,5μm),0.02mol/L乙酸铵(pH约为6.0)-甲醇为流动相(V/V=15/85),柱温30℃,流速1.0ml/min,检测波长230nm,以相对保留时间定性,色谱峰面积定量;结果:该方法平均回收率为98.59%~102.13%,相对标准偏差RSD%为0.978%~1.254%,检测限(S/N=3)为0.037~0.092mg.kg-1;结论:实验表明该方法对饮料中食品添加剂的检测快速、简便、可操作性强。
[关键词]高效液相色谱法;饮料;食品添加剂
HPLC method for detection of benzoic acid, saccharin sodium and sorbicacid which in drinks
AAbstract:Objective: Established and tested three kinds of food Additives which in drinks using HPLC; Methods: Using column(XB-C18,4.6mm×250mm,5μm), The mobile phase is 0.02mol/L ammonium acetate(pH is about 6.0)- methanol(V/V=15/85), Column temperture is 30℃, Flow is 1.0ml/min, Detected wavelength is 230nm, Qualitative with relatively retention time and quantitative with peak area; Results: The average recovery rate is 88.59%~108.13%, RSD% is 0.978%~1.254%, And the detection limit (S/N=3) between 0.037~0.092mg.kg-1;Conclusion: The experiment shows that this method is high-speed、Simple and Operable for detecting the three kinds of food additives which in drinks.
Key words: hplc method; drinks; food additives
食品添加剂是食品工业的基础原料,对食品的生产工艺、产品质量、安全卫生都起着至关重要的作用,但毕竟不是食品的基本成分,尽管在用于食品之前已在试验室中进行多次安全性测试,但违禁、滥用以及超范围、超标准使用添加剂,都会给食品质量、安全卫生以及消费者的健康带来巨大的损害。食品添加剂的种类和数量越来越多,对人们健康的影响也就越来越大。随着研究的不断改进和发展,原来认为无害的添加剂,近年来发现还可能存在慢毒性、致癌作用、致畸作用及致突变作用等各种潜在的危害,因而更加不能忽视。食品添加剂的检测,目的在于监督、保证和促进正确合理地使用食品添加剂,确保人民的身体健康。苯甲酸、山梨酸、糖精钠均是常用的食品添加剂,其中防腐剂(苯甲酸、山梨酸)和糖精钠是饮料必测项目。目前关于食品中防腐剂与甜味剂的检测方法有很多,主要涉及的检测方法有薄层色谱法[1]、气相色谱法[2] [3]、液相色谱法[2] [3] [4]等。本文在液相色谱方法基础上对色谱条件进一步优化,同时检测饮料中三种食品添加剂,使其检测效果更佳、可操作性更强。
1 实验部分
1.1 实验用试剂
甲醇:色谱级
氨水、乙酸铵:分析纯
水:超纯水(符合实验室一级用水)
苯甲酸、山梨酸、糖精钠标准物质:纯度均>99.0%
1.2 仪器与设备
LC310高效液相色谱仪(江苏天瑞仪器股份有限公司),电子天平(赛多利斯科学仪器(北京)有限公司),超声波清洗器(张家港市神科超声电子有限公司),精密酸度计(上海精密科学仪器有限公司),超纯水机(南京易普易达科学发展有限公司)等。
1.3 分析条件
色谱柱:XB- C18色谱柱(250mm×4.6mm,5μm),月旭材料科技(上海)有限公司;
流动相: 0.02mol/L乙酸铵/甲醇(V/V=15/85);
流速:1.0 mL/min;
柱温:30℃;
检测波长:230nm;
进样量:10μl。
1.4 标准溶液的配置
用超纯水分别将3种标准物质配置成约1mg/ml的标准储备溶液(定容时可加入1-2滴无水乙醇消泡),使用时用超纯水稀释成适宜浓度的混合标准溶液,谱图如图1所示。
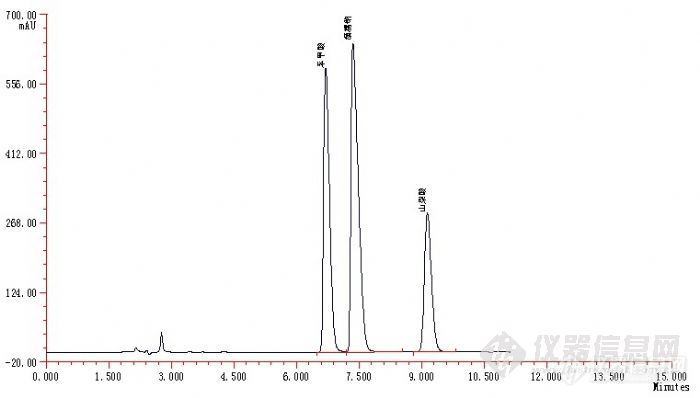
图1 三种食品添加剂液相色谱图
Fig.1 Liquid chromatogram of three food additives
1.5 样品前处理
1.5.1 汽水类:准确称取5.00 g-10.00 g试样,精确至0.0001g,放入小烧杯中,微温搅拌除去其中溶解的二氧化碳气体,用氨水(1+1)溶液调pH约为7,用玻璃棒小心将样品转移至25ml容量瓶中,并用少量水清洗烧杯内壁,清洗液一并转移至容量瓶中,并加水定容至刻度,摇匀,经0.45μm水系滤膜过滤,待测。
1.5.2 饮料类:准确称取5.00 g -10.00g 试样,精确至0.0001g,用氨水(1+1)调pH约7,用玻璃棒小心将样品转移至25ml容量瓶中,并用少量水清洗烧杯内壁,清洗液一并转移至容量瓶中,并加水定容至刻度,摇匀,经0.45μm水系滤膜过滤,待测。
2 结果与讨论
2.1 色谱条件优化选择
考察了不同规格的C18反相色谱柱对三种食品添加剂分离的影响:150mm的色谱柱,虽然总体出峰时间短,但分离效果欠佳,而选用250mm的色谱柱,各峰能达到有效分离(分离度均大于1.5),因此选用250mm的C18反相色谱柱;粒径选择参考了5μm、3μm、10um三种不同粒径的填料对分离的影响,同样长度的色谱柱,3μm粒径的填料分离的色谱峰峰形尖锐,但柱压较高,且价格较贵,10um粒径的填料分离的色谱峰形对称性较差,而5um粒径的填料综合了前两种粒径的优点,因此采用5μm粒径的填料;采用甲醇-草酸铵(1.25g/L)[4]、甲醇-乙酸铵溶液(0.02mol/L)等作为流动相时,用甲醇-乙酸铵溶液(0.02mol/L)分离效果较好,且考察了甲醇-乙酸铵溶液(0.02mol/L)不同比例下的分离情况各种物质的分离情况,在甲醇-乙酸铵体积比为85:15时效果最佳,各物质之间能很好的分离,基线比较平稳。考察了不同柱温(25℃、30℃、35℃、40℃)下各峰分离的情况,在30℃条件下,各峰的分离效果最佳,故选择30℃为柱温。对三种食品添加剂的混标进行紫外全波段扫描,在230nm处各物质对紫外光的吸收都比较好,同时也参考相关文献[1].[2].[3],故选择230nm为检测波长。
2.2 峰位确定
将各标准储备溶液稀释至适宜浓度的标准溶液,按本方法确定的色谱条件,取各单标和混标10μl分别进样测定,按各保留时间确定出峰顺序,出峰顺序为:苯甲酸、糖精钠、山梨酸。
2.3 阴性和系统适用性试验
不加入样品,加入试剂,按样品处理方法进行测定,在各组分相应保留时间处均没有吸收。
取混标10μl进样测定,三个峰相互之间的分离度均>1.5,符合相关规定。理论板数按糖精钠计,均大于8000。
2.4 精密度和重现性实验
准确吸取三种食品添加剂的混标溶液10μl,连续进样6针,进行测定,考察各组分峰面积的相对标准偏差,分析结果如表1所示。
表1 精密度实验数据
Table . 1 Precision of experimental data
组分名称 | 峰面积A | A平均值 | Rt相对标准偏差RSD/% |
苯甲酸 | 8931603 | 8908252.67 | 0.87 |
8792655 |
8919949 |
8980461 |
8986352 |
8838496 |
糖精钠 | 8446111 | 8415672.17 | 0.74 |
8308033 |
8403722 |
8455194 |
8484635 |
8396338 |
山梨酸 | 5140247 | 5129523.33 | 0.62 |
5075328 |
5114234 |
5141873 |
5169418 |
5136040 |
2.5 线性关系和检测限
在本方法确定的实验条件下,苯甲酸、糖精钠、山梨酸在如下表2的进样量范围之间,线性关系良好。各化合物的相关系数见表2。在 S/N =3的条件下,确定各组分的检测限也列入表2中。
表2 线性关系和检出限实验数据
Table . 2 Linearity and detection limit data
组分 | 线性范围 | 线性方程 | 相关系数r | 检测限/(mg.kg-1) |
苯甲酸 | 0.02ng-2.49ng | y = 35923x - 1250.4 | 0.9999 | 0.049 |
糖精钠 | 0.04ng-3.42ng | y = 107334x - 18732 | 0.9997 | 0.092 |
山梨酸 | 0.01ng-0.78ng | y = 15117x + 15278 | 0.9998 | 0.037 |
2.6 回收率试验
采用在实际样品中加入不同添加水平的混标的方式进行回收率实验,按 1.5中的方法处理后分析,采用外标法定量,每个添加水平单独测3次,实验结果表明,其平均回收率为为98.59%~102.13%,RSD为0.978%~1.254%。
2.7 实际样品的测试
采用本实验方法测试部分饮料,实验结果如表3所示。
表3 样品检测结果
Table .3 Sample test results
样品名称 | 食品添加剂的含量/(mg.kg-1) |
苯甲酸 | 糖精钠 | 山梨酸 |
汽水饮料1 | 49.85 | 0.33 | 0.49 |
汽水饮料2 | 0.13 | 0.06 | 未检出 |
茶饮料1 | 46.78 | 0.11 | 0.4 |
茶饮料2 | 0.2 | 未检出 | 0.31 |
果汁饮料1 | 未检出 | 未检出 | 0.28 |
果汁饮料2 | 0.32 | 0.10 | 未检出 |
3 结论
综上所述,通过对部分汽水类、茶类、果汁类饮料进行测试,本方法前处理简单、方便快捷、灵敏度高、回收率好、精密度好,且试剂用量少,避免了大量化学试剂的使用,减少了环境污染,用于快速测定食品中添加剂苯甲酸、山梨酸、糖精钠的含量简单可行。
参考文献
[1] 杨祖英.薄层色谱法测定山梨酸和苯甲酸[J].中国酿造,1983,2(3):32.
[2] GB/T 5009.28-2003食品中糖精钠的测定[S]. 北京: 中国标准出版社, 2004: 223-230.
[3] GB/T 5009.29 -2003 食品中山梨酸、苯甲酸的测定[S]. 北京: 中国标准出版社, 2004: 231-239.
[4] 余炳生,梁广华,刘子阳,等.饮料及果品中糖精钠、苯甲酸、山梨酸和咖啡因的反相HPLC同时快速测定[J]. 食品科学,2001,22(2):67-70.


