摘要:目的通过对固相微萃取(SPME)条件进行优化,建立蔬菜、水果中有机氯农药残留量的快速检测方法。方法使用顶空-固相微萃取技术作为前处理手段,采用气相色谱-质谱联用方法检测蔬菜中15种农药组分。结果在0.05~1.0μg/mL范围内线性回归好,相关系数r大于0.99,样品加标回收率为71%~89%,相对标准偏差为1.1%~9.8%。结论与传统提取方法相比,该方法具有快速、无溶剂萃取、简便、准确、重现新较好的特点,可作为蔬菜、水果中农药残留检测的分析方法。
关键词:固相微萃取;有机氯农药;残留量;气质联用;蔬菜;水果
本文通过优化固相微萃取的试验条件,对蔬菜、水果中添加的有机氯类农药进行萃取,采用气相色谱-质谱联用仪在选择离子(SIM)条件下检测农药残留量,建立了13种有机氯农药及2种拟除虫菊酯类农药的多残留检测方法。
1 实验部分
1.1 仪器、试剂与材料
气相色谱—质谱联用仪(Perkin Elmer珀金埃尔默,Clarus500);分析天平(Mettle-Toledo 梅特勒-托利多);匀浆机(IKA仪科);固相微萃取装置、聚二甲基硅氧烷萃取头PDMS100μm(美国SUPELCO公司)
15种有机氯及拟除虫菊酯农药标准品:六六六、五氯硝基苯、百菌清、乙烯菌核利、七氯、三唑酮、艾氏剂、三氯杀螨醇、稻丰散、腐霉利、异菌脲、硫丹、滴滴涕、狄氏剂、甲氰菊酯、联苯菊酯(1000 最/mL,农业部环境质量监督检验测试中心)
试验材料:蔬菜购自本地市场。
1.2 标准溶液配制
准确移取15种有机氯农药标准品用正己烷定容,全部配成20 mg/L的标准储备液,吸取以上标准储备液适量,混合后稀释至质量浓度为0.05、0.1、0.2、0.5、1.0 mg/L系列标准溶液。
1.3 实验方法
1.3.1蔬菜样品前处理
将蔬菜和水果(西红柿、黄瓜、苹果、哈密瓜)各2kg先切成块后等份取出代表部分,在食物破碎机搅碎至浆状。
根据试验要求准确称取每种样品,加入已知量的混合农药标准,均匀混合后备用。
1.3.2 SPME萃取和GC进样
准确称取5g样品置于加盖容器瓶(10mL)中,将容器瓶放在温控装置上,将SPME装置插入容器瓶中,按要求将萃取头推出且置于匀浆液面上方,准确控温在一定时间后按要求取出萃取头。迅速插入气相色谱仪的进样口并推出萃取头,热解析一定时间后启动色谱仪进样程序。取出萃取头按上述方法进行再次萃取分析。
1.4 仪器条件
色谱柱:HP-5MS(30 m×0.25 mm×0.5 μm);载气:氦气(99.999%);流速:1.0 mL/min;初始状态不分流;进样口温度:270 ℃;程序升温:100 ℃保持1min,以20 ℃/min升温至280 ℃,保持10 min;离子化方式:电子轰击(EI);离子化能量:70 eV;离子源温度:230 ℃;传输线温度270 ℃;溶剂延迟:3 min;扫描范围:50~400 amu;检测方式:SCAN/SIM;定量方式:外标法。
2 结果与讨论
2.1 萃取条件的优化
2.1.1萃取头的选择
固相微萃取头因其涂层类型和膜厚度不同,具有不同适用极性和挥发性等,适用范围也不同,固相微萃取的萃取效率决定于被分析物在萃取头的吸附涂层相与样品相之间的分配系数(K)。吸附涂层材料的选择及设计可根据被分析物的极性和挥发性并按照“相似相溶”原理进行。有机氯类、拟除虫菊醋类挥发性强、极性弱,故本次试验选择100μm PDMS。
2.1.2萃取方式的选择:
目前固相微萃取可分为直接法(DI-SPME)和顶空法(HS-SPME),直接固相微萃取是将萃取头直接插入液体样品或暴露于气体样品中,被分析物从样品中直接转移到萃取头涂层上,适用于洁净样品及气态样品分析。顶空固相微萃取则是将萃取头放在样品上方的蒸发相中,可避免萃取头涂层受到样品基质中不挥发物质或高分子量物质的干扰,适用于易挥发和半挥发物质的分析。考虑本次试验蔬菜、水果样品基质复杂,故选择顶空固相微萃取进行测试。
2.1.3萃取温度:
本次试验选用50℃、60℃、70℃、80℃四个水平来研究萃取温度对萃取效果的影响,15种农药的响应都随着萃取温度的增加而呈正比增加。在70~80℃之间变化趋缓,考虑70℃±1较易控制,监测的农药在该温度下不会分解,故最佳萃取温度选择70℃,温度对萃取效果影响见图1。
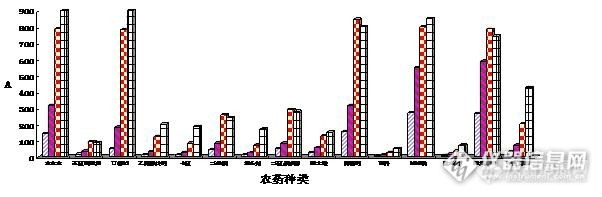
图1 不同萃取温度对15种农药的萃取效果(左~右:50~80℃)
2.1.4萃取时间:
固相微萃取头达到平衡的时间取决于目标物的浓度和萃取头对其的灵敏度,大部分农药都需要很长时间达到平衡,需要综合目标物的响应和时间效率,来选择最佳的萃取时间。本次试验选用10min、20min、30min、45min和60min五个时间水平来研究萃取时间对萃取效果的影响,15种农药都随着萃取时间的增加,响应呈正比增加,出于对实验效率的考虑,萃取时间既可以达到较好的萃取效果又可以实现连续的检测,所以萃取时间选择30min。时间对萃取效果影响见图2。
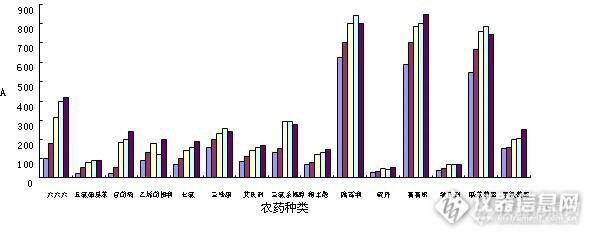
图2 不同萃取时间对15种农药的萃取效果(左~右:10~60min)
2.1.5盐离子浓度:
在顶空法模式下,通常会用饱和或近饱和的无机盐浓度,因其可以降低弱极性有机化合物的溶解度,提高分配系数,从而提高萃取头对目标物的吸附。本实验选择在离子浓度30%(近饱和)NaCl溶液对15种有机氯农药进行萃取。
2.2 质谱条件的选择
采用每种农药的保留时间和特定的定性离子之间丰度比来定性,对于特征离子都大于 m/z 200的农药,至少要选择2个特征离子;对于特征离子只大于m/z 100的农药,至少要选择 3个特征离子。选择定量离子时要考虑选择特征性高或质量数高的离子选择与柱流失碎片离子不同的离子(如不宜选择73、147、156、191、207、253、281等HP-5MS柱流失),选择对称性高且重现性好的离子,定性依据:目标化合物的保留时间与标准样品相比,变化在0.05 min以内,所选择特征离子的相对丰度比例与标样相比在10%之内。采用外标法定量,利用最大丰度的特征选择离子进行定量分析[5]。15种有机氯农药标准品的保留时间、定性、定量离子见表1,农药标准品图谱见图3。
表1 SPME-GC-MS检测15种农药的名称、保留时间及特征离子
Table.1 Retention time, quantitative ions, qualitative ions of 15 pesticide residues by SPME-GC-MS
序号 | 农药组分 | 保留时间/min | 定量离子(m/z) | 定性离子(m/z) |
1 | α-六六六 | 6.58, | 219 | 183,221,254 |
2 | 林丹 | 6.84 | 183 | 219,254,221 |
3 | 五氯硝基苯 | 6.89 | 295 | 237,249 |
4 | β-六六六 | 6.94 | 219 | 217,181,254 |
5 | 百菌清 | 7.10 | 266 | 264,270 |
6 | d-六六六 | 7.23 | 219 | 217,181,254 |
7 | 乙烯菌核利 | 7.49 | 285 | 212,198 |
8 | 七氯 | 7.71 | 272 | 237,337 |
9 | 三唑酮 | 8.05 | 208 | 210,181 |
10 | 艾氏剂 | 8.10 | 263 | 265,293,329 |
11 | 三氯杀螨醇 | 8.16 | 139 | 141,250,251 |
12 | 稻丰散 | 8.42 | 274 | 246,320 |
13 | 腐霉利 | 8.50 | 283 | 285,255 |
14 | 硫丹 | 8.86 | 241 | 265,339 |
15 | p′p-滴滴伊 | 8.98 | 318 | 316,246,248 |
16 | p′p-滴滴滴 | 9.09 | 235 | 237,199,165 |
17 | o′p-滴滴涕 | 9.14 | 235 | 237,165,199 |
18 | 狄氏剂 | 9.13 | 263 | 277,380,345 |
19 | p′p-滴滴涕 | 9.42 | 235 | 237,246,165 |
20 | 联苯菊酯 | 10.27 | 181 | 165,166 |
21 | 甲氰菊酯 | 10.47 | 265 | 181,349 |

图3 15种农药标准品SPME-GC-MS色谱图(0.5mg/kg)
2.3 标准曲线
在优化的最佳萃取条件下,测定5种不同浓度的混合农药标准溶液(0.05、0.1、0.2、0.5、1.0mg/L),每种浓度进样3次。在此线性范围内以浓度与平均峰面积作标准曲线,变异系数RSD(%)值在1.34~8.99之间,相关系数r均大于0.99,线性方程及参数见表2。
表2 SPME-GC-MS检测15种农药标准的标准曲线
Table.2 The linear equations and correlation coefficients of pesticides by SPME-GC-MS
序号 | 农药组分 | 回归方程 | RSD/% | 相关系数(r) |
1 | 六六六 | y = 2749x -144.14 | 5.98 | 0.9962 |
2 | 五氯硝基苯 | y = 187.28x - 0.6942 | 3.25 | 0.9999 |
3 | 百菌清 | y = 2017.3x - 150.62 | 4.36 | 0.9952 |
4 | 乙烯菌核利 | y = 318.3x - 21.371 | 2.99 | 0.9912 |
5 | 七氯 | y = 191.73x - 6.3406 | 5.49 | 0.9957 |
6 | 三唑酮 | y = 492.06x - 2.4604 | 1.34 | 0.9974 |
7 | 艾氏剂 | y = 170.52x - 5.8916 | 5.47 | 0.9927 |
8 | 三氯杀螨醇 | y = 599.01x - 14.035 | 6.08 | 0.9973 |
9 | 稻丰散 | y = 301.38x - 4.5089 | 7.77 | 0.9940 |
10 | 腐霉利 | y = 1604.9x + 4.3859 | 5.48 | 0.9988 |
11 | 硫丹 | y = 47.913x + 2.6723 | 2.98 | 0.9913 |
12 | 滴滴涕 | y = 4116.7x - 142.56 | 8,99 | 0.9973 |
13 | 狄氏剂 | y = 65.744x + 3.8746 | 6.72 | 0.9949 |
14 | 联苯菊酯 | y = 3590x - 73.894 | 5.63 | 0.9988 |
15 | 甲氰菊酯 | y = 436.04x - 11.533 | 6.08 | 0.9991 |
2.4方法回收率及精密度
根据国家无公害蔬菜的农药最大残留量标准[6],分别对西红柿、哈密瓜添加3组不同浓度的混合标准,分别为0.5、0.2、0.05mg/kg,按样品分析步骤操作,高浓度0.5、0.2 mg/kg添加回收重复测定3次,低浓度0.05mg/kg添加回收重复测定5次。另取同批次样品作空白实验,取3次空白测定结果的平均值作为本底,扣除本底(实测样品农药残留量均为未检出)后分别计算加标回收率及相对标准偏差(RSD)(见表3)。
表3 SPME-GC-MS检测15种有机氯农药平均回收率及RSD值(n=3、n=5)
Table.3 Recoveries and RSDs of 15 pesticide residues in different samples by SPME-GC-MS (n=3、n=5)
农药组分 | 添加量 /(mg·kg-1) | 西红柿 | 哈密瓜 |
回收率/% | RSD /% | 回收率/% | RSD /% |
六六六 | 0.5,0.2,0.05 | 87,96,81 | 3.4,5.7,2.4 | 82,92,88 | 1.2,5.9,6.0 |
五氯硝基苯 | 0.5,0.2,0.05 | 82,84,79 | 4.7,1.1,3.0 | 79,86,77 | 7.5,2.2,1.8 |
百菌清 | 0.5,0.2,0.05 | 76,82,75 | 4.2,4.8,6.3 | 87,90,75 | 2.7,1.7,5.4 |
乙烯菌核利 | 0.5,0.2,0.05 | 83,81,86 | 5.2,7.9,6.9 | 79,86,74 | 1.1,1.5,3.4 |
七氯 | 0.5,0.2,0.05 | 86,75,78 | 2.7,2.7,2.4 | 77,80,82 | 5.6,1.3,2.0 |
三唑酮 | 0.5,0.2,0.05 | 71,86,87 | 1.1,7.8,1.3 | 83,74,85 | 1.7,2.1,3.3 |
艾氏剂 | 0.5,0.2,0.05 | 80,80,88 | 5.6,1.7,21 | 85,72,88 | 1.9,4.1,2.6 |
三氯杀螨醇 | 0.5,0.2,0.05 | 82,74,88 | 4.1,3.9,1.8 | 72,84,86 | 5.2,7.8,4.7 |
稻丰散 | 0.5,0.2,0.05 | 75,72,78 | 2.8,4.5,4.1 | 82,82,73 | 4.7,2.4,3.6 |
腐霉利 | 0.5,0.2,0.05 | 87,84,89 | 1.6,8.4,6.9 | 86,89,87 | 4.2,6.3,3.5 |
硫丹 | 0.5,0.2,0.05 | 79,74,82 | 2.8,1.0,3.4 | 87,79,84 | 2.9,2.6,4.3 |
滴滴涕 | 0.5,0.2,0.05 | 78,72,84 | 3.7,8.6,4.2 | 77,74,78 | 8.4,1.9,5.9 |
狄氏剂 | 0.5,0.2,0.05 | 79,86,71 | 6.2,1.0,2.9 | 82,78,84 | 4.1,1.1,5.3 |
联苯菊酯 | 0.5,0.2,0.05 | 77,71,74 | 1.3,1.6,1.9 | 87,84,78 | 9.8,5.5,0.5 |
甲氰菊酯 | 0.5,0.2,0.05 | 73,74,75 | 8.1,1.1,3.3 | 86,82,85 | 7.5,6.5,1.1 |
3 结论
本研究建立了快速、灵敏、准确的固相微萃取-气相色谱-质谱联用技术检测蔬菜、水果中有机氯农药残留的方法。该方法与传统方法比较,具有简便、快速、省溶剂的特点,方法的回收率和精密度较好,能满足农药残留检测工作的需要。
参考文献:
[1] Pawliszyn J. New directions in sample preparation for analysis of organic compounds [J].Trends Anal. Chem. 1995, 14(3):113-122
[2] TOMKINSA BA, BARNARD AR. Detmmination 0f organochlorine pesticides in ground water using solid-phase microextraction followed by dual-column gas chromatography with electron-capture detection.[J]. J Chromatogr A, 2002, 964:21-33.
[3] NATALIA CAMPILLO, ROSA PENALVER, NEREA AGUINAGA, etal. Solid-phase microextraction and gas chromatography with atomic emission detection for multiresidue determination of pesticides in honey[J]. Anal chim. Acta, 2006,562:9-15.
[4] 夏阳, 刘俊亭. 固相微萃取法(SPME)在农药残留分析中的应用[J]. 农药, 2002,41(3):15-16.




