

特别说明:本论文表面上是讨论离子色谱的一种特殊类型-离子转换色谱。但本质上是对传统抑制器理念的全新认识,如何认识膜抑制和柱抑制的各自优缺点。
也许这是本论文的最大价值所在。------恐龙注。
离子转换色谱是一种特殊类型的离子色谱,虽然离子转换色谱早在1983年,Downey和Hieftje和等首次提出离子转换色谱(Replacement-IonChromatography, RIC)概念——基于传统离子色谱基础上的一种色谱分离方式。其基本原理是在传统的双柱型离子色谱(分离柱+抑制柱)中引入第三根“转换柱”(ReplacementColumn),目的是将从抑制器中洗脱出来的被分析离子在其中实现定量替换,成为以目标离子形式存在的洗脱产物,然后进入检测器实现检测。但这方面国内外罕有人研究,国外有关文献仅仅只有十来篇,国内类似文献仅仅有一篇。
据相关文献报道,目前离子转换色谱的分离模式主要有:阴离子-阳离子-原子发射光谱检测;阳离子-阴离子-紫外-可见分光光度检测;阴离子-阳离子-大气阴极辉光放电光度检测器,阳(阴)离子-阳(阴)离子-电化学选择性电极检测。
上述研究大多仅仅只有一篇文章,这种探讨理论的可能性研究,实验的结果差强人意,跟传统方法没有任何优势,充其量只实现了一个idea。而且大多研究在上个世纪进行。
我们实验室对离子转换色谱的原理进行重新研究分析,发现大多数研究中,其替换是采用抑制器的方式,而dionex膜抑制器是公认的最佳抑制模式。但是采用膜抑制器的最大问题,离子渗漏造成背景高,灵敏度低,操作稳定性差,因此研究取得的进展缓慢,在实验室遇到难以克服的一些困难。
采用膜抑制器转换的方式,其实存在众多弊端,如果从其原理上看,柱抑制器同样可行,虽然柱抑制器的抑制容量有限无法长期使用。但是在实际分析过程中,经过第一个抑制器抑制后,再通过抑制柱的转换,其实其所含离子已经大大减少,与淋洗液有着本质的区别,连续使用数天是没问题的。抑制柱的最大优点是解决了膜抑制器的渗漏问题,在柱形式中是不存在的。因此,一般柱抑制器的抑制容量足够连续分析数天。其带来的无渗漏、可梯度洗脱,无需额外的部件,使用简单的有点是膜转换器无法替代的。为什么长期以来,所有的科研工作者一直采用膜转换器而不用柱转换器,其本质在于对柱抑制器和膜抑制器的错误认识。在通常的抑制分析中,膜抑制器有其独特的优势。但是在离子转换这个特殊的离子色谱模式中,老式的柱抑制器模式,更具有优势。只有对离子色谱抑制原理的充分认识,柱膜抑制器各有特点和优势,才能充分发挥各自的优势。
因此,当我们将抑制柱的模式应用到研究中,克服了原有模式的众多弊端,同时在通常的一根抑制柱的模式上,首次提出了“二次转换”的新概念,也就是被测离子通过二次转换,变成了自己同类的离子。首次实现了紫外检测器间接测定无紫外吸收的阴离子。
下面举例来说明:
1 仪器与试剂
ICS3000离子色谱仪(Dionex,美国),包括泵(SP/DP)模块、检测器/色谱(DC)模块、淋洗液自动发生器(EG)模块,AS-AP自动进样器。色谱工作站(变色龙6.8 SR7),超纯水机(MilliPore A10)。
2 色谱条件
色谱柱:DionexIonPacTM AS11-HC(4 mmx 50mm Guard +4 mm x 250mmAnalytical)。
Li+转换柱(3cm x 3 mm i.d.);IO3- 转换柱(3cm x 3 mm i.d.),均为自制柱。
淋洗条件:KOH(淋洗液自动发生器),梯度程序:0~12min, 0.8 mmol/L;12~50 min,0.8~14.10 mmol/L;50~70 min 14.10~34.10 mmol/L;70~75.00min 34.10 mol/L;75.01~85.00 min 0.8 mmol/L 抑制器:ASRS300(4mm);抑制电流:95mA;检测器:电导检测器、紫外检测器(检测波长210 nm);进样量25μl;柱温:30 ℃
3结果与讨论
3.1 实验装置构建
“一次离子转换”的UV-RIC系统检测阴离子时,被测阴离子从抑制柱中洗脱出来进入转换柱前,是以其各自共轭酸的形式(HA) 的形式存在的,由于阴离子转换膜上残留的OH- 交换位点,被测阴离子以其共轭酸的形式(HA) 经过这些残余的OH-离子交换位点时H++ OH- =H2O 的中和反应就会被促发,为了维持电荷平衡,被测阴离子便会被部分吸附在阴离子交换膜上。依据道南原则,H+ 在阳离子中体积最小,电荷最低,因而阴离子交换膜对于 H+ 的道南排斥作用最低,从而导致HA 的透膜扩散变得相对容易,发生严重的透膜损失。由于受到以上两个因素的限制,“一次离子转换”的UV-RIC系统无法实现阴离子的紫外检测。
本文采用二次离子转换色谱,即在传统的抑制型离子色谱的基础上,在抑制器之后与紫外检测器之前,依次串联两根自制型的离子转换柱:第一根为锂型阳离子转换柱,第二根为IO3-型阴离子转换柱。实验过程中,无机阴离子与有机酸经过AS11-HC分离柱分离,并经阴离子抑制器分别以各自的无机、有机酸形式洗脱出来后进入第一根锂型阳离子转换柱时,被测离子共轭酸中的H+便会与阳离子转换柱中大量存在的Li+ 交换位点发生离子转换,从而几乎全部被定量地转换为锂离子盐的形式;随后,当被测阴离子以其各自锂盐的形式再进入到第二根阴离子转换柱中时,各个被测阴离子又会与阴离子交换柱中大量存在的紫外离子交换位点(IO3-)发生离子转换,从而全部被定量地转换为LiIO3,最后进入紫外检测器,在210nm的波长处实现紫外检测。
经过以上所述的“二次离子转换”的过程后,所有被测阴离子均可以被顺利地,定量地转变为有紫外响应的碘酸根离子。由于阴离子经过第二根紫外转换柱时是以其各自锂离子盐的形式存在,而不是以共轭酸的形式存在的,即使第二根阴离子转换柱中仍然会残存少量OH-的交换位点,这些 OH- 的交换位点也不会对结果产生明显的影响,确保了离子转换的顺利进行。图1为该实验的流程示意图。
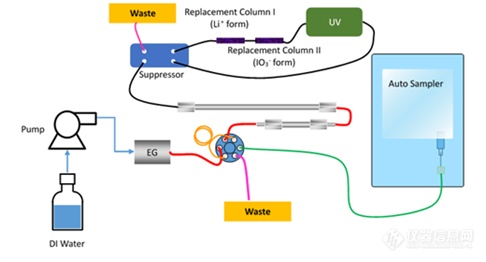
图1 二次离子转换与紫外检测器联用实验装置示意图
3.2 标准系列溶液的线性、精密度、定量限与检出限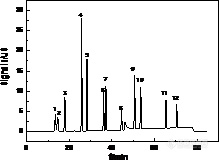
图2 标准溶液中十二种待测离子的色谱分离谱图(紫外模式+电导模式)
1. lactate; 2. acetate; 3. formate; 4. chloride; 5. nitrite; 6. bromide; 7.nitrate; 8.succinate; 9. sulfate; 10. oxaiate; 11.phosphate; 12.citrate.
图2可知,在2节色谱条件下,十二种阴离子和有机酸的混合标样在UV-RIC系统中基本可以实现基线分离效果。其中,Cl-、NO2-、Br-、NO3-线性拟合曲线几乎重合,说明强电离一价无机阴离子可以等摩尔置换出Li+ 和IO3-,从而使离子转换效率几乎达到100%,实现定量转换。由于SO42-电荷数为二,故其线性拟合曲线的斜率高于一价离子,且近乎为一价离子的两倍。由于有机酸的弱电离性(乳酸、乙酸、甲酸),其转换效率低于100%,故其信号强度与拟合曲线斜率相对强电离的阴离子偏低,但二价(琥珀酸、草酸)、三价(柠檬酸)弱电离的有机酸,其线性拟合曲线的斜率近乎分别为一价强电离无机阴离子斜率的两倍、3倍。对于总体而言,各个待测离子的线性相关系数均可达到0.9994~0.9999之间,线性关系良好。比较紫外和电导的谱图出峰位置相似但峰高有区别。
4.实际样品检测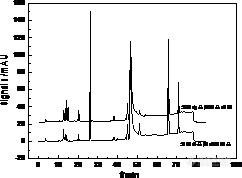
图3 两份啤酒样品的分离谱图(紫外模式和电导模式)
表1 IC-CD系统与UV-RIC系统对于两份啤酒样品检测结果的对比
| Sample | Compound | Detection results of IC-CD system (mg/L) | Detection results of UV-RIC system(mg/L) | RSD (%) (n=6) |
|
f beer sample1 | Lactate | 14.92 | 15.60 | 3.2 |
| Acetate | 9.212 | 8.973 | 1.9 | |
| Formate | 1.099 | 1.184 | 5.3 | |
| Chloride | 16.67 | 16.21 | 2.0 | |
| Succinate | 8.135 | 7.975 | 1.4 | |
| Sulfate | 1.823 | 1.762 | 2.4 | |
| Oxaiate | 1.203 | 1.147 | 3.4 | |
| Phosphate | 33.58 | 33.72 | 0.29 | |
| Citrate | 11.50 | 10.99 | 3.2 | |
|
|
|
|
|
|
|
beer sample2 | Lactate | 4.436 | 4.248 | 3.1 |
| Acetate | 1.365 | 1.465 | 5.0 | |
| Formate | 0.9600 | 1.009 | 3.5 | |
| Chloride | 18.35 | 17.88 | 1.8 | |
| Succinate | 7.164 | 7.349 | 1.8 | |
| Sulfate | 3.920 | 4.185 | 4.6 | |
| Oxaiate | 1.335 | 1.257 | 4.3 | |
| Phosphate | 29.51 | 29.26 | 0.60 | |
| Citrate | 12.09 | 11.46 | 3.8 |