

电喷雾离子源原理研究进展
罗杰鸿1*
(1.广东安纳检测技术有限公司)
Research progress in the principle of electrosprayion source
Luo jiehong1*
(1.1.Guangdong ANAtesting technology Co., Ltd, Guangzhou 510000, China)
Keywords Ion source theory, ion evaporation model, charged residue model, chainejection theory, Zhu Xinyi's experiment and theory, ion migrate and transport
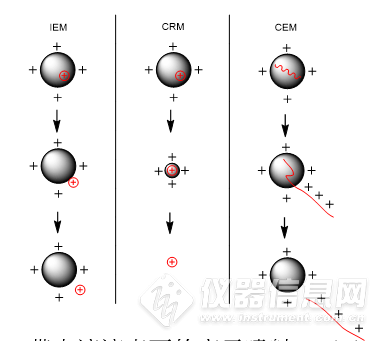
图1 ESI的三种机制。(a) IEM:带电液滴表面的离子喷射;(b) CRM:蛋白质释放到气相;(c) CEM:未折叠蛋白喷射[18]
2.离子蒸发模型
离子蒸发模型认为,在高电场梯度和脱溶剂气体的作用下,溶液在电喷雾针出口形成微小的带电液滴,液滴表面的电荷密度随着液滴中溶剂的蒸发而增加。当电荷密度增加到瑞利稳定极限时,液滴被静电排斥并分裂成更小的液滴。重复该过程,直到发生场诱导离子蒸发。当离子之间的静电斥力达到一定程度时,挥发性高的离子优先从液滴表面喷射并进入气相,而其平衡离子保留在液滴中并最终成为固体残留物,这是离子蒸发模型[8,19]。Iribarne[8,19]等人提出,离子蒸发过程可以用过渡态理论来表示:
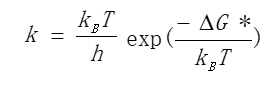
式中:-G*是自由活化能,kB是玻耳兹曼常数,h是普朗克常数,T是温度。
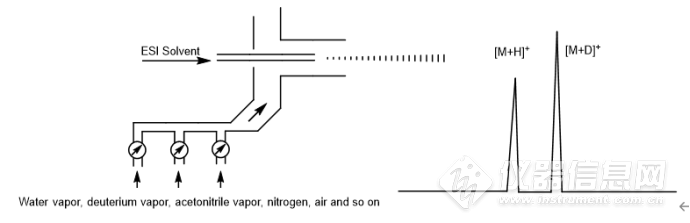
Fig.2 principle of new CEESI ion source
然后,以咖啡因为样品,以水蒸气和氘水蒸气为辅助气体调节电离室中的气氛。当辅助气体为水蒸气时,无论是溶解在水中的咖啡因还是溶解在氘水中的咖啡因,质谱检测到的主峰为[M+H+]=195.2。当辅助气体为氘水蒸汽时,无论咖啡因溶于水还是溶于氘水,质谱主峰均为[M+D+]=196.2。朱一心和合作者认为咖啡因没有OH键,所以不能产生氢氘交换。从实验结果可以推断出咖啡因在两种不同条件下的不同质谱,即质子(H+或D+)来自电离室大气。
朱的结果表明,在气相电离过程中使分子带电的质子实际上来自于水分子在电场中电离产生的质子。极性分子在高电场中极化,极化的分子和质子产生静电引力,形成多电荷分子离子。结合实验,朱一心及其合作者提出并证明了电喷雾电离中的质子来自泰勒锥外的大气。电离室的气氛是影响电喷雾电离过程的重要因素。通过有效控制电离室气氛,可以提高分析物分子的电离效率,其新发现为质谱分析带来了更多的新应用。
朱一心及其同事认为,当电喷雾发射针处于正电压时,针尖表面会形成一个稳定的泰勒锥,因为泰勒锥的曲率半径很小(纳米量级),针尖表面的电场很强,只能离开泰勒锥。同时,针尖上的水分子场蒸发形成氢离子,氢离子被条形极性分子的负端吸附,形成多电荷离子。同时可以看出,当两个极性分子出现在泰勒锥附近时,氢离子被极性较大的分子吸附,从而出现离子抑制现象。
6. 离子迁移搬运机理
朱一心及其同事的实验首次证明,电喷雾离子源中的质子来自泰勒锥外的大气。然而,朱的原理并不能解释一种常见的实验现象,即离子加合现象[27,28]。离子加合现象,如铵离子加成,铵离子来源于流动相中添加的醋酸铵。显然,质子和其他加合离子来自流动相。基于实验和作者的相关研究内容[28-30],作者等[14]提出了“离子迁移和搬运”的机制。“离子迁移和搬运”的机理可以归纳为三点。
首先,在离子源中,在雾化室温度和脱溶剂气体的条件下,脱溶剂在毛细管针尖周围的空间中迅速形成大量的H+、NH4+(添加NH4Ac)、Ac-(添加NH4Ac)、Cl-(添加CHCl3和其他氯源)、NO2-(添加含NO2-)和Na+等离子体,这称为流动相-氮气辅助气氛围。流动相-氮气辅助气氛围,为H+、NH4+等加合离子的电泳提供了条件。
同时,流动相中的分析物通过毛细管电压、雾化室温度和溶剂气体去除的作用形成裸露小分子(这些裸露小分子可能进一步裂解成离子,迁移到质谱仪检测器,然后进行测定,如Folpet[31,32])。
最后,这些带电离子通过某种力(氢键、范德华力、离子键相互作用等)与无电荷的裸露小分子结合,产生迁移并被测定。在这里,大量的H+、NH4+、Ac-、Cl-、NO2-和Na+离子充当“搬运工”。真正迁移的是这些离子(包括热分解产生的离子)。当它们迁移时,一些分析物形成的无电荷裸露分子被“搬运”到质谱仪检测器并被检测。可能的途径称为“离子迁移搬运”机制,示意图如图3所示。
离子迁移搬运机理可以简述为:假设当毛细管为正,而质谱检测器为负时,由流动相、脱溶剂气或者空气等提供电泳条件。此时,H+、NH4+等离子发生迁移,当它们迁移的时候,通过作用力,把裸露的小分子或者蛋白质搬运到质谱检测器。搬运的对象可以是裸露的小分子或者蛋白质,也可以是团簇小溶剂,也可以是空气中的小分子物质。

Fig. 3 Schematic diagram of "ion migrate and transport"mechanism
Conclusions
本文从离子源原理出发,介绍了离子蒸发机理、带电残体机理、链喷射理论、朱一心的实验与理论、离子迁移搬运机理等理论,综述了该领域的最新研究进展。离子源原理的研究对离子源的设计和开发具有重要意义。理论的发展可以为解决一些问题提供一些帮助,例如定量问题。离子源理论发展缓慢,在一定程度上影响了离子源的设计和开发[33-35]。因此,发展离子源理论具有重要意义,将是一个重要的研究方向。
Notes and references
1 X. Zhao, F. Bu, L.M. Zhou, B.Li, ValueEngineering, 2012, 31, 326.
2 Lee J Y , Min H K , Moon M H ..Analytical and Bioanalytical Chemistry, 2011, 400(9):2953-2961.
3 M. Dole, L.L. Mack, R.L. Hines, R.C. Mobley,M.B. Alice, J. Chem. Phys., 1968, 49, 2240.
4 M. Yamashita, J.B. Fenn, J. Phys. Chem., 1984, 88, 4451.
5 C.M. Whitehouse, R.N. Dreyer, M. Yamashita,J.B.Fenn., Anal. Chem.,1985, 57, 675.
6 A.P. Bruins, T. R. Covey, J.D. Henion, Anal. Chem., 1987, 59, 2642.
7 N. B. Cech, C.G. Enke, Mass spectrometry reviews,2001, 20, 362.
8 J.V. Iribarne, B.A. Thomson, TheJournal of Chemical Physics, 1976, 64, 2287.
9 Dole, Journal of ChemicalPhysics, 1968, 49, 2240.
10 A.T.Iavarone, E.R. Williams, Journalof the American Chemical Society, 2003, 125, 2319.
11 E. Ahadi,L. Konermann, J. Phys. Chem. B., 2011, 116, 104.
12 L. Konermann, A.D. Rodriguez,J. Liu, Anal. Chem., 2012, 84, 6798.
13 J.Y. Pei, Z.H. Hou, Journalof Instrumental Analysis, 2018, 37, 1508.
14 J.H. Luo. Guangdong Chemical Industry,2020, 47, 78.
15 F.Y. Gao, W.B. Zhang,Y.F. Guan,Y.K. Zhang, ScientiaSinica(Chimica), 2014, 44, 1181.
16 K. Q. Tang, A. Gomez . Physics of Fluids, 1994, 6, 404.
17 P. Nemes , I.Marginean, A.Vertes. Analytical Chemistry, 2007, 79, 3105.
18 L. Konermann, E. Ahadi, A.D.Rodriguez, S. Vahidi, Anal.Chem.,2013, 85, 2.
19 W.B. Zhang, F.Y. Gao, Y.F.Guan,Y.K. Zhang, Chinese Journal of Chromatography, 2014, 32, 395.
20 Aliyari, Elnaz, Konermann, etal. Analytical Chemistry 2020, 92, 15,10807-10814.
21 Znamenskiy V , Marginean I ,Vertes A . Solvated Ion Evaporation from Charged Water Nanodroplets[J]. Journalof Physical Chemistry A, 2015, 107(38):7406-7412.
22 J.F.de la Mora, Anal ChimActa., 2000, 406, 93.
23 Lars, Konermann, Robert, et al. TheJournal of Physical Chemistry, 2014, 118(41):12025-12033.
24 Haidy M , Quentin D , Lars K .Analytical Chemistry, 2018, 90.
25 Pimlott D , Konermann L .International Journal of Mass Spectrometry, 2021, 469.
26 Y.X. Zhu, G. Dolios, R. Wong, Y.K.Zhang, National mass spectrometry Symposium of Chinese Chemical Society ,2015,175.
27 R.B. Cole, J.H. Zhu., RapidCommunications in Mass Spectrometry, 1999, 13, 607.
28 J.W. Li, J.H. Luo, GuangdongChemical Industry, 2019, 46, 134.
29 G.Y. Liu, J.H.Luo, J.B. Huang.,Guangzhou Chemistry, 2020, 45,60.
30 Y.Q. Nong, J.H. Luo,Guangdong Chemical Industry, 2020, 47, 151.
31 Z.H. Tang, X.H. Liang, L.H. Wang,Z. Dang. X.H. Liang, Chinese Journal of Tropical Agriculture, 2018, 38,99.
32 Aurélie Berthet, MichèleBouchard, Patrick Schüpfer, et al. Analytical and Bioanalytical Chemistry, 2011, 399(6):2243-2255..
33 B.Q. Li, Z.Y. Zhang, J.L. Kong,L. Zhang, C.H. Guo, C.P. Li, Journal of Chinese Mass Spectrometry Society,2020, 41, 221.
34 J.M. He, T.G. Li, J.J. He, Z.G.Luo, ABLIZ Zeper, Journal of Instrumental Analysis, 2012, 31,1151.
35 X.L. Ding,Y.X. Duan, ScientiaSinica(Chimica), 2014, 44, 672.