

老化验工
第4楼2010/09/24
铬酸钡的溶解度与温度、溶剂、PH值有关。在温度和溶剂不变情况下,PH值显著影响铬酸钡的溶解度,在PH4以下,几乎就不会沉淀。原因可通过下面几个六价铬的沉淀平衡、酸碱平衡和聚合平衡来解释: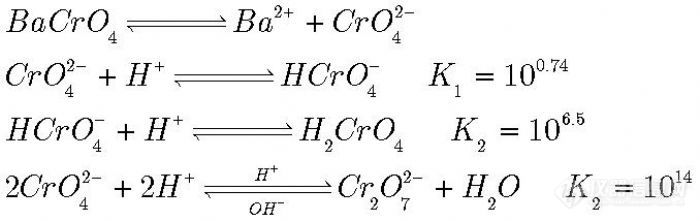
不考虑任何影响时,铬酸钡在纯水中的溶解度约为0.00001mol/L.
由于铬酸为二元弱酸(一级酸式离解较强),因而当PH值降低时,铬酸钡的溶解度会随之增大,可以从平衡移动原理得到解释。酸性条件下沉淀溶解的主要原因还在于生成的铬酸和铬酸氢根在酸性条件下能转化成重铬酸根,而重铬酸钡是不沉淀的,计算知:当PH=3时,若溶液中含1mol/L重铬酸根时,铬酸根浓度已经只有0.0001mol/L了,PH值越纸,转化率越高。这是影响铬酸钡沉淀溶解度的主要原因。都可以用平衡移动原因来解释的。
当PH值在10以上时,铬酸根沉淀完全的程度取决于温度和加入的氯化钡的过量程度,酸度的影响可以忽略。
但有一个现象要注意:如果你沉淀的PH值太高,如达到PH14,则加入过量的氯化钡时,也会有少量氢氧化钡沉出,因为氢氧化钡的溶解度不是很大,当溶液中有大量氢氧根存在时,便会析出少量氢氧化钡,后者在用水洗涤时会因溶解而消失,而铬酸钡的溶解损失则不大。
当然,对于较低浓度的铬酸根,加氯化钡沉淀时,如果溶液中含浓度较高的强电解质(所有存在的阴阳离子),都会导致沉淀的溶解度明显增大,这种现象称为盐效应。