液液萃取LLE和固相萃取SPE两种方式处理茶饮料香气成分的粗略比较
前 言
茶饮料是夏日最常见最受大家欢迎的饮品,清爽解渴,消暑清凉。但茶饮料的香气成分很复杂,香气化合物的极性相差较大,沸点范围很宽,所涵盖的化合物这类很多。也无法直接进样,需要进行适当的提取后供gc-MS分析。有多种样品处理方式,例如顶空,液液萃取,固相微萃取,固相萃取,同时蒸馏萃取,吸附搅拌子等。鉴于篇幅所限,以及考虑处理的效果和设备的限制,本文仅简单讨论液液萃取LLE和固相萃取SPE两种方式对处理茶饮料香气成分差异。
1试验部分
1.1 仪器与装置
美国安捷伦6890N/5975C气相色谱-质谱联用仪,带有德国Gerstel的MPS2多功能自动
进样系统,整合FID检测器,同时带德国Gerstel毛细管柱分流装置。
全自动液液萃取仪 (Ludwig)
固相萃取仪SPE (J.T.Baker)
默克密理博超纯水机
1.2样品和标样、试剂
茶饮料样品,市场样,来自某超市。
所有香气化合物标准品均来自Sigma-Aldrich等主要试剂公司,少数为实验室内部精制标样。C6-C30正构烷混合标准物来自安谱公司。
SPE小柱:BondElut PPL(苯乙烯-聚乙烯基苯聚合物,从安谱公司购买),3ml/200mg
甲醇,特丁基甲醚(色谱纯,安谱公司),氯化钠(分析纯)
超纯水(本实验室默克密理博超纯水机制备)
1.3 gc/MS条件
1.3.1 色谱条件:
色谱柱:安捷伦HP-Innowax(60m×0. 25 mm ( i.d.)×0.25μm)毛细管柱;
升温程序: 60℃,以5 ℃/min升至250℃,保持18 min;
载气(He,纯度99.999%以上)流速1.8 mL/min;
进样口温度250℃,分流进样,分流比10:1; 进样量:1μl。
检测器:FID, 氢气:30ml/min, 空气:350ml/min, 尾吹:N2,30ml/min, 温度:270℃。
1.3.2质谱条件:
电子轰击(EI)离子源;电子能量70eV;传输线温度280℃;离子源温度230℃;四级
杆温度150℃。SCAN扫描范围:29-400。
1.4样品处理及分析方法
液液萃取法(LLE):准确称取约300g冰红茶饮料样品,加入适当量内标物,加入30g固体氯化钠,用乙醚戊烷(1:1)120ml,用全自动液液萃取仪提取,无水Na2SO4干燥后用微柱浓缩器浓缩到1ml。进样1微升进行gc-MS/FID分析。也可以使用分液漏斗来进行液液萃取,设备就比较简单,但需要人工操作来震摇和分离收集。
固相萃取法(SPE):准确称取约300g茶饮料样品,加入适当量内标物。
活化SPE小柱:用3ml甲醇,3ml水洗;加入上述样品,流速1ml/min; 用3ml水冲洗小柱;干燥后,用特丁基甲醚1ml洗脱。进样1微升洗脱液,进行gc-MS/FID分析。
在分析样品前,和样品分析完全相同的条件下,用0.05%的C6-C30的正构烷标样注射到gcMS,获得正构烷的保留时间,用于计算保留指数。分析样品后,用软件计算样品各个组分的保留指数,并和标样的保留指数对比来,结合质谱来定性。
事先也用同样方法测定标样的保留指数备用。
2 结果与讨论
2.1 茶饮料液液萃取和固相萃取总离子色谱图(TIC)轮廓图比较
茶饮料液液萃取LLE总离子色谱图(TIC)如下:
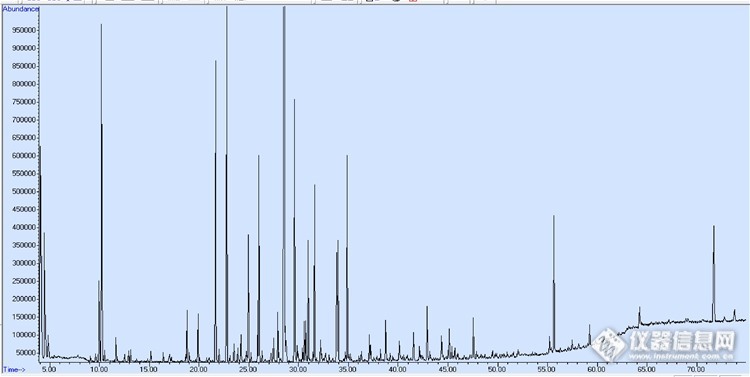
图1 茶饮料液液萃取LLE总离子色谱图(TIC)
***************************************************************************************************************
茶饮料固相萃取SPE总离子色谱图(TIC)如下:
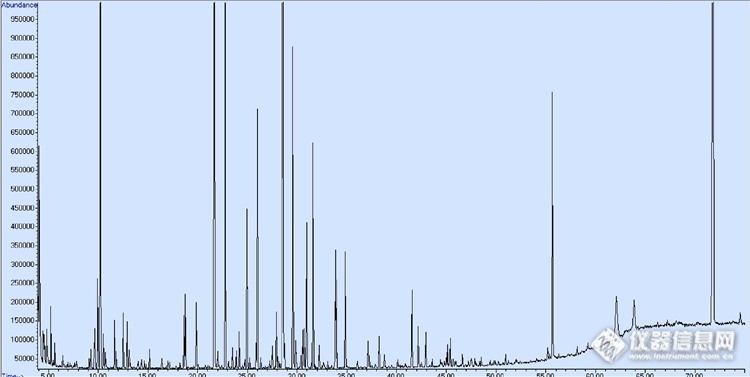
图2 茶饮料固相萃取SPE总离子色谱图(TIC)
*************************************************************************************************************
把两者的总离子色谱图放在一起进行比较。
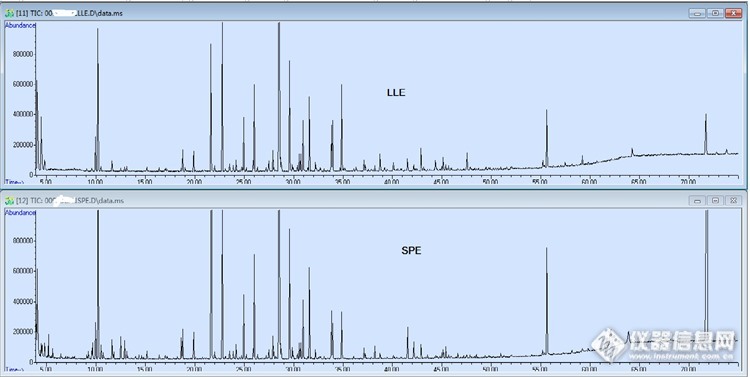
图3 茶饮料固相萃取和液液萃取总离子色谱图(TIC)对比
************************************************************************************************************
从上面的对比图看出来,两者的轮廓图(profile)比较接近,有些香气化合物的响应有所不同,种类不完全一样,有差别。
在FID积分后,液液萃取有223个峰,固相萃取有239个峰(未计算amdis拆分的峰),绝对峰个数固相萃取要多一些。或者讲固相萃取的提取的组分要多一些。
总面积比较:液液萃为270728545,固相萃取342057304,后者略多一些。这可能和样品的最后的浓缩也有关系。
由于两种提取方式有所不同,有些化合物的提取回收率有差异。
2.2数据处理:
先用Amdis质谱数据解卷积处理质谱数据,减少本底干扰,对共流出峰拆分,提取出大峰下面的峰或隐藏在里面的色谱峰。同时用Amdis的MSL质谱数据库和工作站的PBM(L)质谱数据库检索,并结合保留指数来鉴定峰。所有保留指数均由标准样品测定。极少数没有保留指数的化合物,参照其它资料和以往的经验,在保证良好匹配度的情况下确认。由于FID的动态线性范围很宽,香气样品的含量范围较宽,一般用气相色谱FID来定量,而不用质谱总离子(TIC)来定量。用FID检测器的结果计算茶饮料样品组分的含量。
共鉴定测定了茶饮料中180个香气香味组分。其中液液萃取143个组分,固相萃取148个组分。
固相萃取的检出灵敏度相对高一些,一些含量小的成分在液液萃取上面未捡到,但在固相萃取就检出了。例如methyl butyrate,methyl 2-methylbutyrate,alpha-fenchene,camphene, hexanal, limetol, citroxide, coamene, diethyl malonate,camphene hydrate, ocimenol, linalool oxide, piperitone, 一些酸,酚,indole等。
而在液液萃取上面检出了nonanal,tetrahydrolinalool, propionic acid, cis-ocemenol, hexenal, phenylethyl alcohol,carveol, hexenoic acid, nerolidol, jasminlactone等,而在固相萃取上面看不到。
液液萃取也检出可能由于溶剂不存或付反应带来一些化合物,例如ethyl acetate, ethanol, acetoin, acetic acid。
含量对比(部分举例差异大的):Vanillin在LLE上是1.647%, 而在SPE上面是2.425%,caffeine在LLE上面是1.209%,而在SPE上面是9.291%,相差很大。Triacetin在LLE上面0.282%,而在SPE上面0.527%,Maltol在LLE上面0.061%,而在SPE上面0.024%,ethylMaltol在LLE上面是0.087%,而在SPE上面0.052%,benzyl alcohol在LLE上面3.441%,而在SPE上面1.476%。两者对于不同化合物的回收率不同,选择性不一样。
2.3 茶饮料成分(鉴于知识产权问题,只公布部分数据,请谅解)
表 茶饮料成分表 (部分)
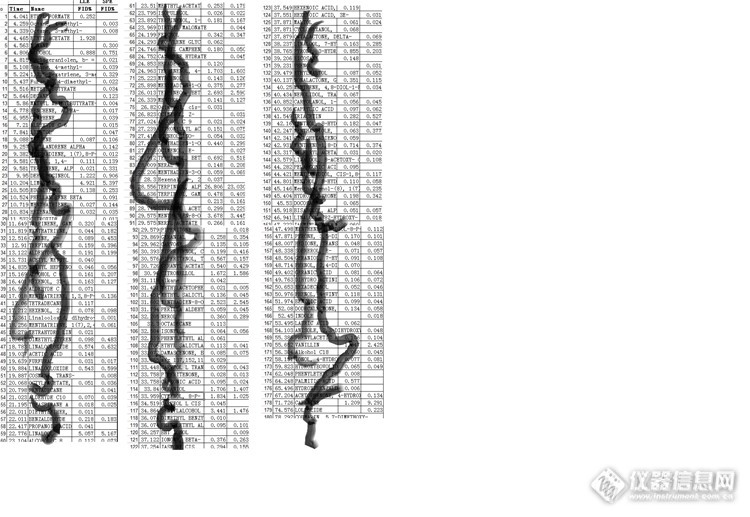
3 结论
茶饮料的香气成分非常复杂,香气化合物的极性相差较大,沸点范围很宽,所涵盖的化合物这类很多。选择更为合适有效的前处理尤为重要。用液液萃取法来提取茶饮料香气成分,容易操作,如果采用分液漏斗设备就不贵,效应少,可以较高的浓缩倍数。但需要使用大量溶剂,并需要浓缩,手续繁琐,费时间,极性化合物回收率低,容易乳化,浓缩时候低沸点组分损失大,也会有少量副产物生成。固相萃取法操作简单方便,使用极少量的有机溶剂,避免产生乳化现象,提取浓缩净化一体。但不同填料对有不同化合物的选择性不一样。不同性质的化合物回收率有差异。相对比较,固相萃取更有优势。但如果两者结合,互补就更好了。





