
Insm_188a0345
第9楼2021/02/28
以下是我整个实验过程,为什么我实际滴定的结果和理论计算的结果不同啊
1 测定原理
利用氨性醋酸锌和脱硫液中硫氢根离子作用生成硫化锌沉淀,经过滤将沉淀分离,加入碘标准溶液及盐酸溶液,过量的碘用硫代硫酸钠标准溶液返滴。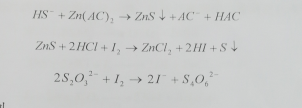
2试剂及其配制
0.01mol/L碘标准溶液
0.01mol/L硫代硫酸钠标准溶液
10g/L淀粉溶液
2%醋酸锌溶液:称取2g醋酸锌溶于100mL水中,加冰醋酸0.6mL。
3测定步骤
准确吸取10mL脱硫液放入盛有5mL 的2%醋酸锌溶液的250mL烧杯中,在沸水浴上加热至沉淀物凝聚,过滤,用水洗至无硫代硫酸根。滤纸同沉淀移入250mL碘量瓶中。加入约80mL水、20mL 的0.0ImoLlL碘溶液和5mL的1:2盐酸。然后搅碎滤纸,立即用0.01molL硫代硫酸钠标准溶液滴至获黄色再加入 3mL10g/L.淀粉溶液,继续滴定至蓝色消
空白实验:在80mL水中加入20ml碘溶液,5mL1:2盐酸,3mL10g/L淀粉溶液,用0.01mol/L硫代硫酸钠标准溶液滴至蓝色消失。
4计算
我用的是0.228g/L的硫化钠 v1用18.8ml v2用15.8ml 根据公式得出硫氢根离子浓度是0.201g/L
但是根据大家告诉硫化钠和硫氢根离子他们的比例关系,算出的是0.228g硫化钠溶液1L水后能生产0.0965g/L的硫氢离子。
为什么我实际滴定后计算出的结果与直接用化学方程式计算的结果不一样啊? 结果相差了2倍