

柯灿艺
目录
第1章 碳酸镁的制备
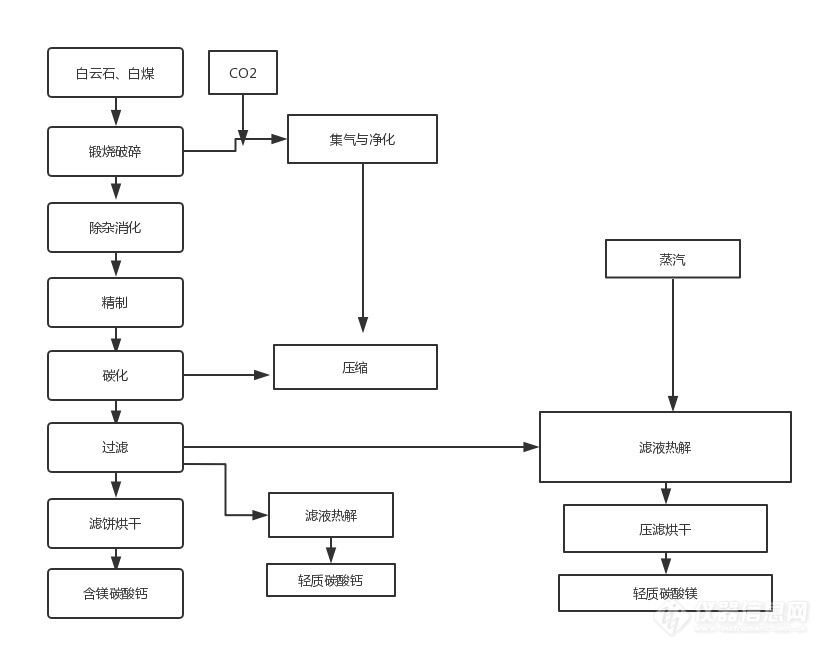

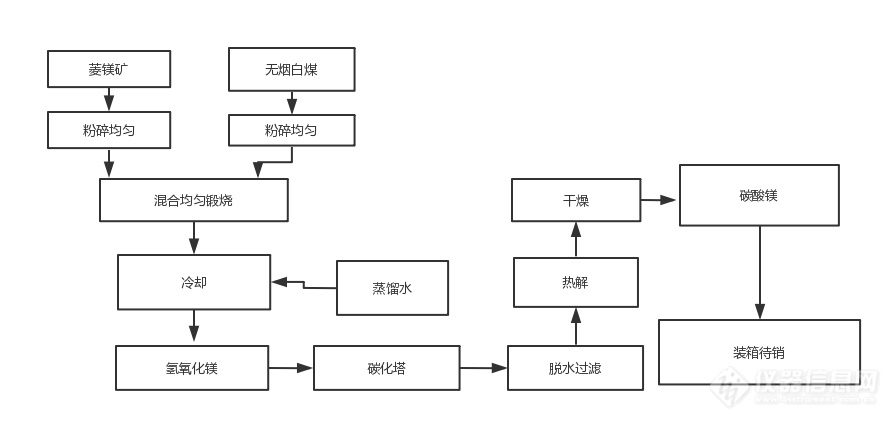
第2章 碳酸镁的应用
项目 | 指标 |
氧化镁(MgO), ω/% | 40.0~44.0 |
酸不溶物, ω/% | 0.05 |
氧化钙(CaO), ω/% | 0.60 |
可溶性盐, ω/% | 1.0 |
砷(As)/(mg/kg) | 3 |
重金属(以Pb计)/(mg/kg) | 10 |
参考文献
项目 | 指标 |
氧化镁(MgO), ω/% | 40.0~44.0 |
酸不溶物, ω/% | 0.05 |
氧化钙(CaO), ω/% | 0.60 |
可溶性盐, ω/% | 1.0 |
砷(As)/(mg/kg) | 3 |
重金属(以Pb计)/(mg/kg) | 10 |