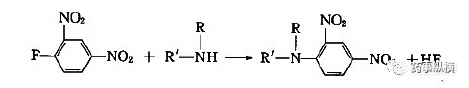该篇按照酸类化合物,碱类化合物,共轭双键化合物,需衍生的化合物的类别,进行方法开发的分享。
酸类化合物:
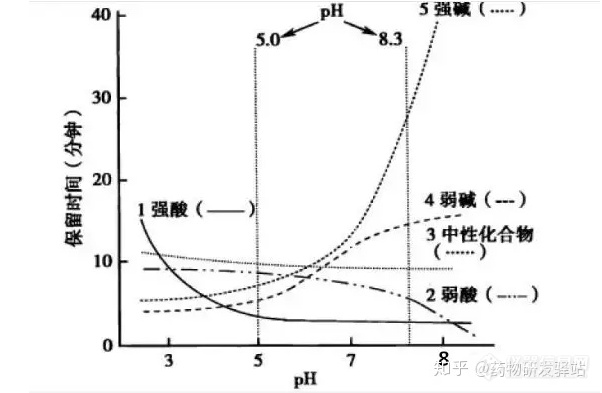
酸类化合物:
流动相pH要低于待测物pKa,待测物在反相中才以中性化合物存在
增加保留措施:(序号就是优先级顺序)
1.运行纯水相,需要能耐100%纯水,耐pH2以下的色谱柱,比如T3
2.HILIC模式:反反相。
水相为洗脱相,有机相为保留相。有机相的占比不能少于40%。
离子形态才能在该模式下实现保留。
3.离子对试剂:使用四丁基氢氧化铵等
案例1:
开发检测原料的方法
原料结构如下

色谱柱 | Waters Atlantis T3 (4.6*150mm,3um) |
流速 | 1.0ml/min | 波长 | 228nm |
柱温 | 40℃ | 进样量 | 1ul |
流动相A | 0.1%磷酸水溶液 | 流动相B | 乙腈 |
梯度洗脱 | Time(min) | A% | B% |
1 | 0 | 95 | 5 |
2 | 3 | 95 | 5 |
3 | 8 | 20 | 80 |
4 | 10 | 20 | 80 |
5 | 10.1 | 95 | 5 |
6 | 15 | 95 | 5 |
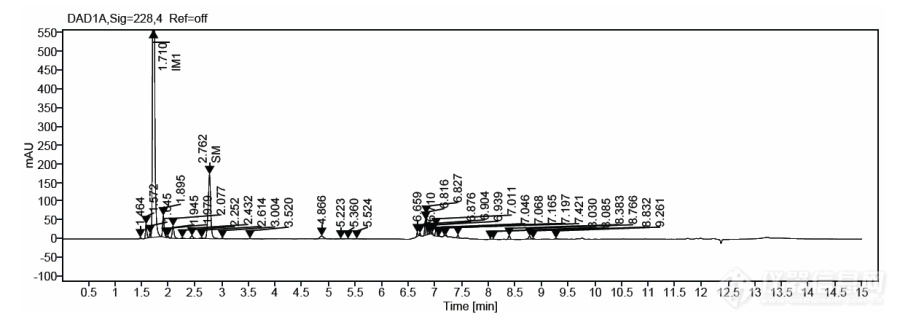
原料RT2.76min,分离,保留及峰形都符合要求。
案例二:
开发吡啶酸的方法

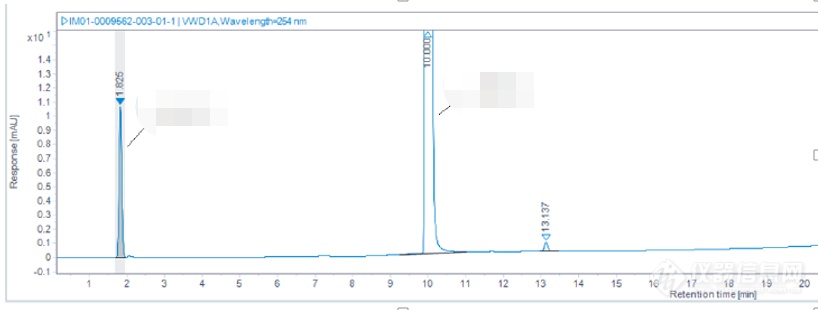
吡啶酸pKa小于2,换纯水相也很难提升保留。
使用HILIC方法去开发:
使用Amide色谱柱
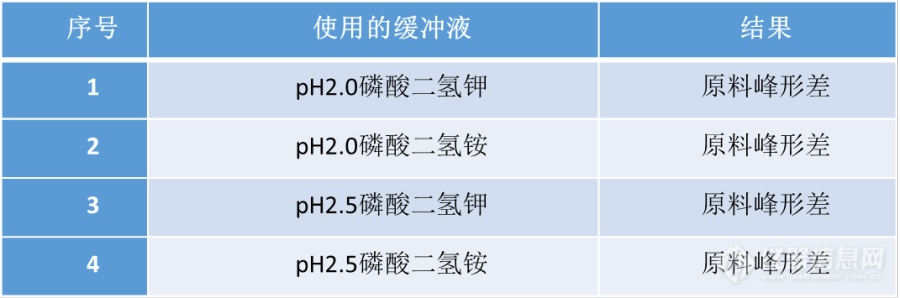
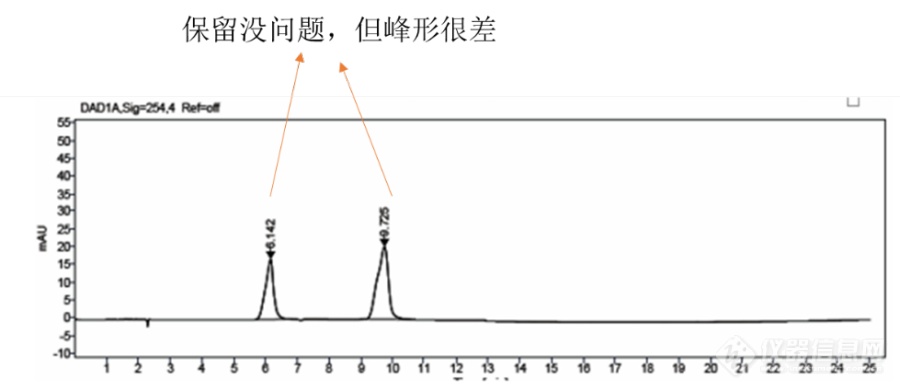
使用离子对试剂:

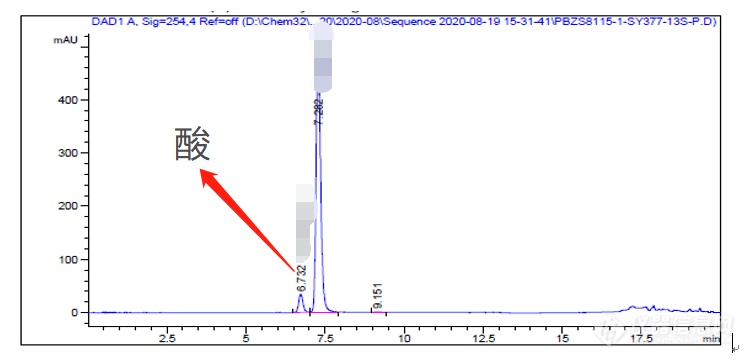
已完全分离,保留较好,峰形较好。
碱性化合物:
流动相pH要高于待测物pKa,待测物在反相中才以中性化合物存在。
增加保留措施:(序号就是优先级顺序,若能用高氯酸代替氨水,则2优先级最大)
1.使用高pH缓冲液,比如氨水
2.使用高氯酸或高氯酸盐作为缓冲液添加剂。
3.HILIC模式:反反相。
水相为洗脱相,有机相为保留相。有机相的占比不能少于40%。
离子形态才能在该模式下实现保留。
4.使用TEA抑制峰拖尾(已慢慢淘汰)
5.离子对试剂:使用己烷磺酸钠等,最好别用
案例:
开发该化合物IM4的纯度方法。
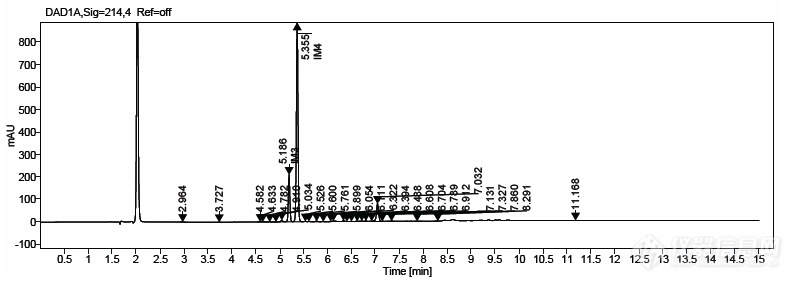
使用氨水体系去开发:
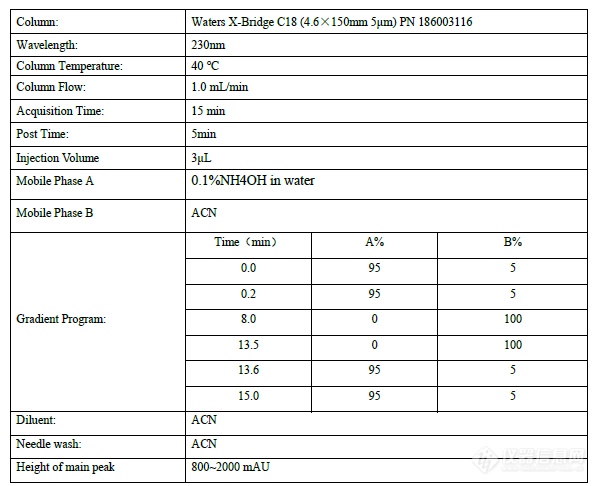
开启全波段,214nm为最佳吸收波长
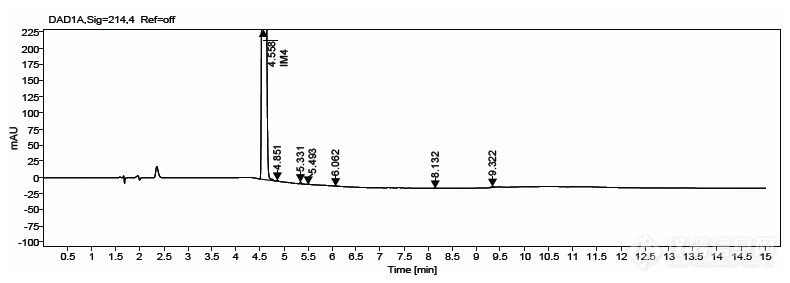
用氨水体系,峰形及保留都可以。
一周时间后,IM4保留2.8-4.6min之间漂移,方法需要调整。
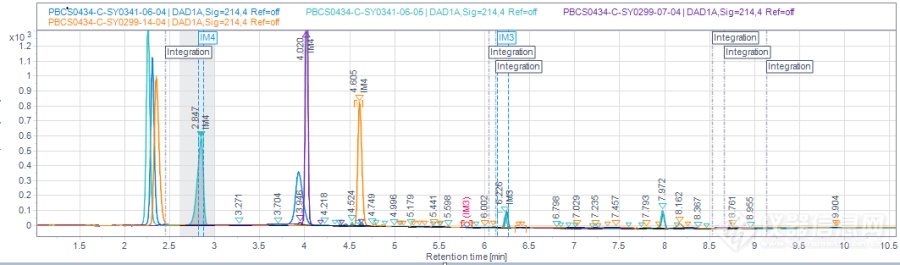
改用HClO4
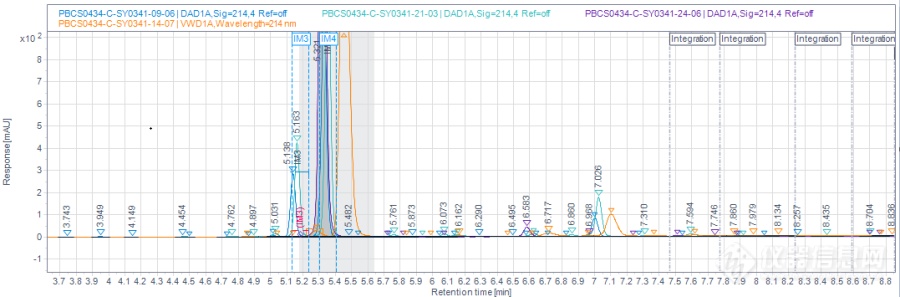
15天之内的叠加图,在5.3-5.5min之间,保持稳定。
ClO4-有非常强的扰乱水分子间的氢键、增加其混乱度的能力。能够增强在反相色谱系统中低pH条件下碱性化合物的保留。其中的作用机制是ClO4-和质子化的碱性分析物产生强的离子对作用而对它们之间的水分子产生排斥,从而形成一个中性复合物。这种复合物在疏水的固定相上有更好的保留。
也有人认为分析物保留的增强与ClO4-在反相固定相上的吸附有关。
ClO4- 对比NH4OH的优势:
色谱柱更耐用(绝大部分色谱柱耐酸不耐碱)
截止波长更低,基线干扰小
一定程度上能修饰峰形
劣势:
无法与MS联用。
共轭双键化合物:
共轭双键化合物的分离案例:
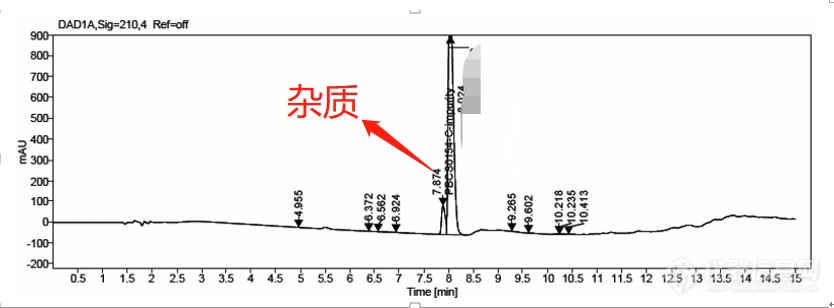
前者为杂质,后者为主物质。

使用通用方法后发现杂质和主物质无法完全分离
使用苯基柱,将色谱柱换成Waters X-Bridge® Phenyl , 4.6*150mm,3.5um
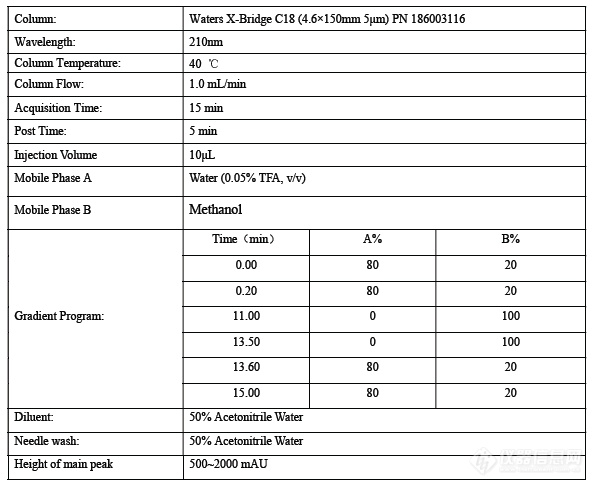
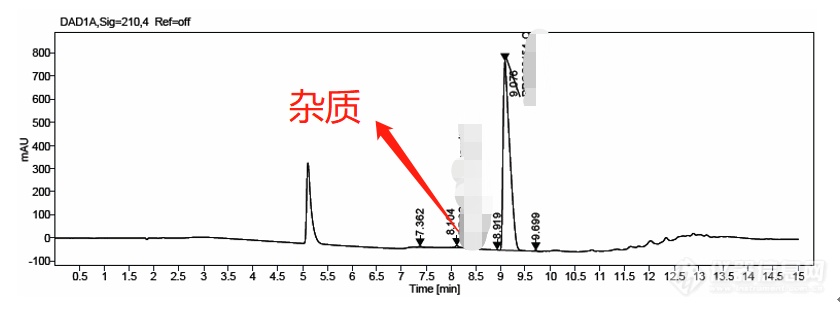
分离情况很好,方法优化完成。
苯基柱对于共轭双键,苯环有独特的选择性
衍生案例:
案例1
需开发检测中间态中原料的分析方法
路线:
中间态:
初始方法:

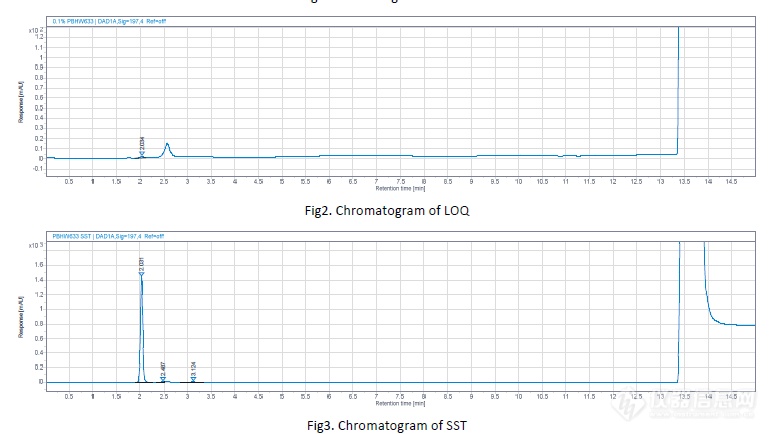
结果:IPC中没有中间态,全是原料
分析:中间态遇水反应回原料,无法监控原料残留。
反应如下:
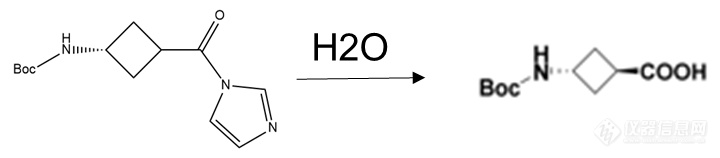
如何监控?
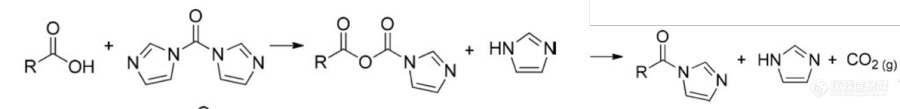
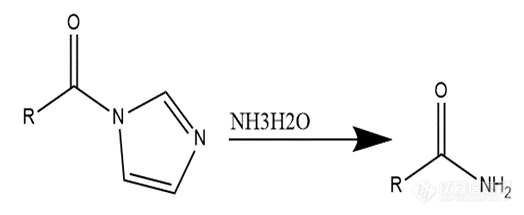
衍生点:CDI化合物遇氨水形成酰胺,反应迅速。
样品配制:
transfer 100μL reaction solution into a centrifuge tube. Add 1.0 mL of NH3·H2O,shake about 1min, volume to 3mL with DMF,shake about 1 min。
巧妙之处:将中间态衍生成了IM1,IM1中间体和反应液中控方法,可以用同一个色谱条件。
方法思考:有必要用HILIC体系去监控样品么?
尝试使用高氯酸体系
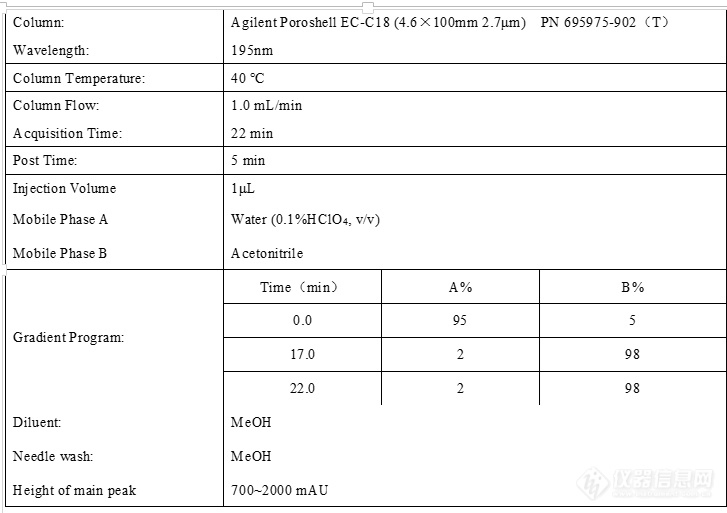
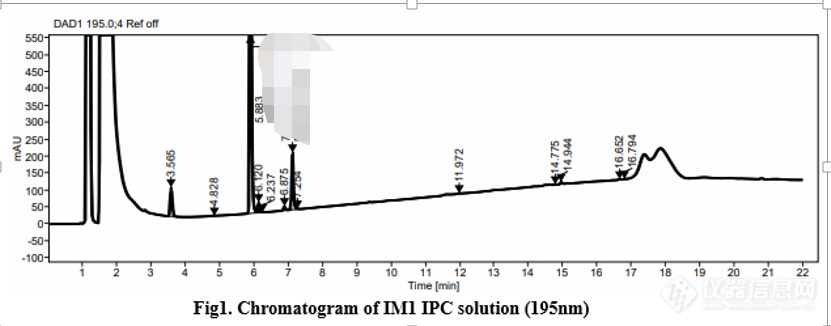
高氯酸对比hilic优点:
流动相配制简单;IM1和原料保留增强;基线无干扰;运行时间缩短了10分钟。
案例2:
 该化合物的手性方法开发
该化合物的手性方法开发

方法开发尝试二
尝试气相手性柱去实现分离
用了仅有的两根气相手性柱,达不到完全分离。手性化合物性质接近,通过调节升温程序,也无济于事、
方法开发尝试三
尝试反相系统,正相色谱柱去实现分离,结果:和正相结果一致,峰分裂成几个。

衍生点:醛酮化合物可通过肼类化合物衍生成棕
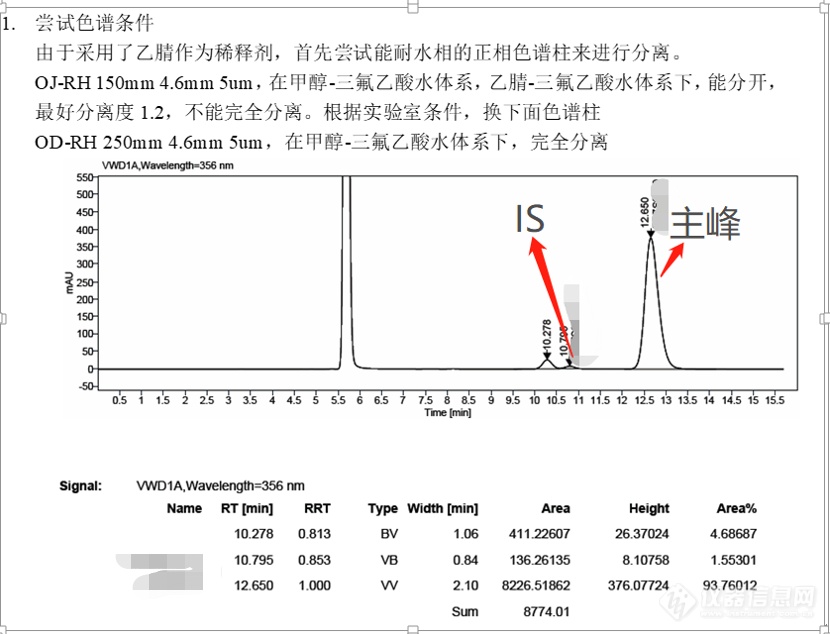
能用反相进行手性分离的化合物都有明显的特征:具有较强的氢键官能团。
再介绍几种衍生的反应:
酰氯的衍生:
酰氯和醇类反应,形成酯类化合物。
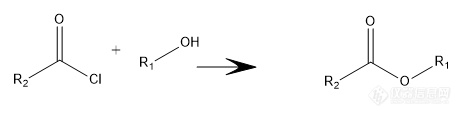
酰氯和水反应,形成羧酸类化合物。
与仲胺,伯胺反应,形成酰胺
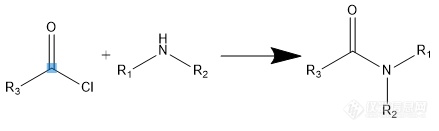
胺类的衍生:
卤代烃衍生化试剂,该反应还适用于仲胺的鉴别
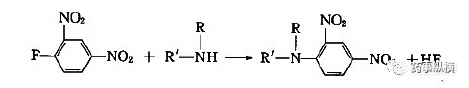
与酰氯反应,形成酰胺。
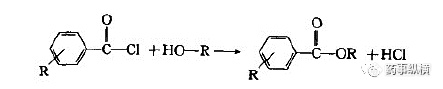
羟基的衍生:
与酰氯反应,生成酯类化合物
羰基的衍生:
与肼类反应,生成棕
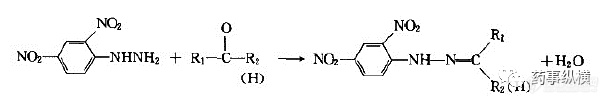
衍生目的:提高响应,增加保留,淬灭等等。要灵活使用。


































 该化合物的手性方法开发
该化合物的手性方法开发