推荐厂家
暂无
暂无
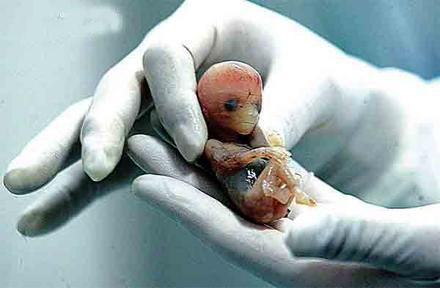





著名中药材“熊胆”近来被推上风口浪尖:活熊取胆,将传统中医药推入伦理争议中。自古至今,传统中药材大多取自大自然,这些集“天地之灵气”的药材,对多种疑难杂症的诊疗具有奇效。步入现代社会,不少中医中药却遭遇伦理尴尬。面对声声质疑,传统中药能否跨过现代医学“伦理关”? 中医药取材濒临匮乏 中药向来以取材天然、选择大胆而著称。从动物、植物到矿物,皆可“入药”。但大自然并非取之不尽、用之不竭,随着自然资源的不断减少,天然中药材濒临匮乏。上海中医大附属龙华普外科主任张静教授举例,“以往读书时,老师常会提及经典药方"犀骨地黄汤",此方清热解毒功效甚好。犀牛列入保护动物清单之后,犀骨无从获取。我从医至今,正宗的"犀骨地黄汤"几乎不见踪影,取而代之的是水牛骨。”类似的例子不胜枚举,植物药材亦然。“李时珍所著《本草纲目》里许多野生草药,如今已绝种。那些曾在历史上盛传的药方,就此成为"传说"。”专家不无惋惜 天然中药材为何日渐匮乏?专家分析原因:首先,随着人口增长,患者人数大幅增加,资源消耗“水涨船高”,数量有限的天然中药材供不应求;其次,现代工业破坏了生态平衡,致使一些物种濒临绝境,中药无从取材;再者,现代伦理意识大大增强,以往看来理所应当的取材方式被质疑、甚至被摒弃,中药取材受到严格限制。中药材的匮乏,一定程度上对事业发展带来阻碍 伦理先要划清“边界” 像活熊取胆这样沿袭成百上千年的取材方法,而今因伦理问题遭遇尴尬。一边是“以人为本”的医疗理念:一边却是“保护大自然”的环保呼声:人类不能为了一己私利,不顾其他物种的繁衍发展。传统取材方式与现代伦理之间,该怎样实现平衡才有利于持续发展?上海大学社会学者胡申生认为,分清伦理的边界,或可有助于提高社会认知。他形象地说,“活熊取胆”与吃鱼翅之类的做法,根本属性并不一样。其一,熊胆的用途是急救人命,吃鱼翅纯粹出于养生考虑;其二,取熊胆并非就此夺取熊的性命,吃鱼翅则可能导致鲨鱼彻底灭绝。就目前而言,暂且不论获取方式如何,活熊取胆尚不到伦理无法容忍的境界。 专家同时补充,社会看待伦理的态度应更加辩证、科学。人与动物的生命价值并非此高彼低,或彼高此低。人类不应为自身利益,无视动物生命;相反,亦不应因一味保护动物,无视人类生命。作为“万物之灵长”,人类无疑是自然界最为重要的物种。在必须时,人类获取包括动物在内的自然资源来延续生命,无可厚非。不过活熊取胆之类的事宜,能否通过“伦理关”,攸关中医能否与时俱进的大计。 运用伦理手段找出路 中医如何在传统取材与现代伦理中找到出路?张静喆认为,以动物取材为例,界定动物种类与范围是关键。针对犀牛、老虎等濒危保护动物,为繁衍物种,中药取材只能找寻其替代品;但针对一些可通过人工饲养、繁殖的动物,为确保疗效,中药取材不应设定过于严苛的限制。在界定选择范围的基础上,尽可能用科学手段减少动物的痛苦。实验室的小白鼠曾经也引起伦理讨论。如今,科学家们用无痛、麻醉等伦理手段,减轻小白鼠的痛苦;有的甚至给为科学而“牺牲”的小白鼠造墓、立碑,这便体现了伦理意识。在中药取材时,类似的伦理手段可被借鉴。这样,针对天然中药材的伦理质疑声也会有所减少。 胡申生还表示,传统中医中药跨入现代社会势必会“水土不服”。接轨现代医学,“伦理关”无法轻松逾越;但中医药更不可因遭受伦理质疑而裹足不前。应对传统中医药的伦理问题,不妨医学、伦理、社会学家携起手来,集纳各方意见为中医药发展提出宝贵建议,让中医药更加适应现代医学体系。
关于印发药物临床试验伦理审查工作指导原则的通知 国食药监注436号 2010年11月02日 发布 各省、自治区、直辖市食品药品监督管理局(药品监督管理局),总后卫生部药品监督管理局: 为加强药物临床试验的质量管理和受试者的保护,规范和指导伦理委员会的药物临床试验伦理审查工作,提高药物临床试验伦理审查工作质量,根据《药品注册管理办法》和《药物临床试验质量管理规范》的有关规定,国家局组织制定了《药物临床试验伦理审查工作指导原则》,现予印发。请你局指导本辖区内药物临床试验机构学习,参照执行。 附件:药物临床试验伦理审查工作指导原则起草说明 国家食品药品监督管理局 二○一○年十一月二日
[size=4] [font=黑体] 根据十一届全国人大常委会第二次委员长会议的决定,全国人大常委会办公厅近日向社会全文公布了食品安全法草案,并广泛征求各方面意见和建议,以更好地修改、完善这部法律草案。 食品安全法是我国继产品质量法、消费者保护法和食品卫生法之后又一部专门保障食品安全的法律。怎样才能最大限度地提高立法质量?怎样才能让这部法律在防止、控制和消除食品污染与危害,保证食品安全,保障人民群众生命安全和身体健康等方面发挥更大的作用?本期评论版专门组织了一组文章,分别从不同角度进行了评析。 以人的生命为本,在食品安全领域首先需要确立伦理底线,超越人类底线的行为必须严厉打击 [/font][/size]

 400-659-9826
400-659-9826
 留言咨询
留言咨询

 留言咨询
留言咨询
 留言咨询
留言咨询


