


工农兵
第2楼2009/11/05
日本 石灰消化法
生石灰 (CaO 100%) 0.840
专业法定编号
制备方法
国际储运号
主要化学方程式有:
氢氧化钙溶液和饱和碳酸钠溶液反应能够生成氢氧化钠:
Ca(OH)2 + Na2CO3=2NaOH+CaCO3↓,这个反应可以用来制取小量烧碱。
氢氧化钙和二氧化碳的反应
Ca(OH)2+CO2=CaCO3↓+H2O(这是石灰浆涂到墙上后氢氧化钙与二氧化碳发生的反应,墙会“冒汗”就是因为生成了水H2O,墙变得坚固是因为生成了碳酸钙CaCO3,在乡下有时为了使墙更快变硬,就在刚刷好的屋里烧炭生成二氧化碳CO2(C+O2=(点燃)CO2)。这个反应也是检验CO2的方程式,气体通入石灰水变混浊的是CO2)。
不同量的氢氧化钙和碳酸氢钠的反应
2NaHCO3+Ca(OH)2(少量)=CaCO3↓+2H2O+Na2CO3
NaHCO3+Ca(OH)2(过量)=CaCO3↓+H2O+NaOH
工业上煅烧石灰石CaCO3==(高温)CaO+CO2↑(此反应也是工业上制取大量CO2的方法,一式二用)
工地上经常冒白烟是在制石灰浆Ca(OH)2:CaO+H2O=Ca(OH)2(因为熟石灰的溶解度随温度升高而降低,所以工人更愿意在夏天制石灰浆,这样温度高时溶进水的熟石灰少,可制得更多石灰浆,此反应放出大量热量)
石灰浆被抹在墙上,与CO2反应后变硬Ca(OH)2+CO2=CaCO3↓+H2O
氟化氢氨与氢氧化钙的化学方程式:NH4HF2 + Ca(OH)2 = CaF2 + 2H2O +NH3
氯化镁和氢氧化钙反映的化学方程式:MgCl2+Ca(OH)2=CaCl2+Mg(OH)2↓
硝酸氨与氢氧化钙反应的化学方程式:
2NH4NO3+Ca(OH)2=NH3↑+H2O+Ca(NO3)2
(NH4)2SO4+Ca(OH)2=NH3↑+H2O+CaSO4
CaCO3+SiO2=CaSiO3+CO2 条件是高温
氢氧化钙具有碱的通性。它的碱性或腐蚀性都比氢氧化钠弱,可以说是一种中强性碱,这些性质决定了氢氧化钙有广泛的应用。农业上用它降低土壤酸性,改良土壤结构,很明显在这种场合用氢氧化钠是不可能的。农药波尔多液是用石灰乳和硫酸铜水溶液按一定比例配制的。因1885年首先用于法国波尔多城而得名。这种用于果树和蔬菜的天蓝色粘稠的悬浊液农药,是通过其中的铜元素来消灭病虫害的。其中不仅利用了氢氧化钙能与硫酸铜反应的性质,也利用了氢氧化钙微溶于水的特点使药液成粘稠性,有利于药液在植物枝叶上附着。另外氢氧化钙与空气中的二氧化碳反应生成难溶于水的碳酸钙,也有利于药液附着于植物表面一段时间不被雨水冲掉。
工农兵
第3楼2009/11/05
氢氧化钙和二氧化碳的反应不论在化学实验室还是在工农业生产中,或者在自然界都经常发生。经常被利用着。石灰沙浆砌砖抹墙的事实熟为人知。鲜为人知的是制糖工业中也发生这个反应:在制糖过程中要用氢氧化钙来中和糖浆里的酸,然后再通入二氧化碳使剩余的氢氧化钙变成沉淀过滤出去,这样才能减少糖的酸味。
氢氧化钙溶液和饱和碳酸钠溶液反应能够生成氢氧化钠:
Ca(OH)2 + Na2CO3=2NaOH+CaCO3↓,这个反应可以用来制取小量烧碱。
Ca(OH)2+CO2=CaCO3↓+H2O ,这个反应可用来鉴定氢氧化钙溶液。
如果在氢氧化钙溶液中继续通入二氧化碳,会发下溶液先浑浊后澄清,这是因为二氧化碳会和碳酸钙[Ca(CO3)]继续反应
CaCO3+CO2+H2O=Ca(HCO3)2, 而碳酸氢钙[Ca(HCO3)2]是易溶的,所以溶液会再次澄清。加热溶液又变浑浊,因为碳酸氢钙受热分解
Ca(HCO3)2==CaCO3↓+CO2↑+H2O
氢氧化钙不能盛放在带玻璃塞的试剂瓶中,因为虽然二氧化硅化学性质稳定,但是会与强碱反应,如NaOH,KOH,RbOH,Ba(OH)2,Ca(OH)2。如果把氢氧化钙
放在带玻璃塞的试剂瓶中,会发生如下反应:
Ca(OH)2+SiO2===CaSiO3↓+H2O
而硅酸钙会沉淀在瓶塞上,导致瓶子打不开,所以不能成在带玻璃塞的试剂瓶中。
制取氢氧化钙:H2O+CaO=Ca(OH)2(这里切记!没有沉淀符号的)
初中需掌握的并不多:
Ca(OH)2+CO2=CaCO3↓+H2O
Ca(OH)2 + Na2CO3=2NaOH+CaCO3↓即可
Ca(OH)2+2HCl=CaCl2+H2O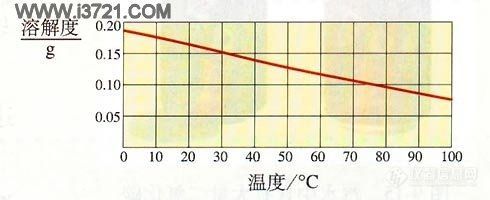
工农兵
第4楼2009/11/05

澄清石灰水
即为Ca(OH)2的澄清溶液
CaO(也就是生石灰)溶于水后生成的Ca(OH)2溶解度非常小,所以我们常看到的石灰水都是混的,澄清是过滤后的结果,而且由于澄清的石灰水作用主要就是检验反应产物,如果本身不澄清,即使生成沉淀也不能看到,所以书中提到石灰水一般都要加澄清。
并且澄清石灰水是混合物
用途
主要用于检验产物,一般用于检验二氧化碳。另外二氧化硫也能使澄清石灰水变混浊。
检验二氧化碳的原理
二氧化碳通入澄清石灰水变混浊,是因为二氧化碳和石灰水反应生成碳酸钙沉淀:
CO2+Ca(OH)2=CaCO3↓+H2O
如果继续通入二氧化碳,混浊的石灰水又会变得清澈,这是因为通入的过量的二氧化碳与碳酸钙和水反应生成了可溶的碳酸氢钙:
CaCO3+CO2+H2O=Ca(HCO3)2