瞬稳静态注射化学发光法测定水果中的总铬
摘要利用Cr3+对鲁米诺一过氧化氢化学发光反应的催化作用,瞬稳静态注射化学发光法的优点,建立测定Cr3+的新方法,并通过硼氢化钾的还原作用,使Cr6+还原为Cr3+,从而实现对总铬的测定。确定此方法的最佳条件:放大倍数64×;铬(III)试液的pH为4.5;EDTA浓度为0.1mol/L。线性范围为1.0×10-5mg/mL一1.0×10-3mg/mL,该法测定苹果,红枣样品的回收率均在80%-120%范围内,符合要求。
关键词化学发光法水果总铬
引言随着我国对外开放的不断扩大和人民生活水平的提高,农产品的质量安全问题日益引起人们的重视。除了较明显影响人体健康的农药残留问题外,对人体有累积性影响的微量元素限量闯题也开始引起人们的关注。铅、铬、砷等公认有毒重金属对人体健康危害不仅受到医学界的重视,也成为食品检验、卫生标准和环境检测的重要分析项目。而锰、铜、锌等人体必须的元素,超过一定的限量范围也会对人体有害。为此,各国都对食品中的微量元素作出了限量规定。我国还发布了砷、铅、铜、锌、镉、汞、氟、硒、稀土、铬等10种(类)元素在水果中的限量卫生国家标准及相应的测定方法国家标准,这些标准的发布和实施,为我国衡量和测定水果中有害元素含量提供了科学依据[1]。
三价铬是人体必须的微量元素之一,对维持正常血糖,胆固醇和脂肪酸代谢有影响。而六价铬则是明确的有害元素,能使人体血液中某些蛋白质沉淀,引起贫血、肾炎、神经炎等疾病,长期与六价铬接触还会引起呼吸道炎症并诱发肺癌或者引起侵入性皮肤损害,严重的六价铬中毒还会致人死亡。所以寻求一种快速的具有高灵敏度的测量水果中重金属含量分析方法对其安全营养性的探讨具有指导作用[2][3]。
在我国的食品检验标准中,微量元素的测定大多采用传统的化学法和原子吸收法。化学法由于分析步骤烦琐,检测周期长,显然满足不了目前日益提高的检测需求。原子吸收法是目前普遍采用的一种方法,也是国家标准方法。而相对于原子吸收法,化学发光法作为一种有用的痕量分析技术具有灵敏度高,线性范围宽(常常在3-4个数量级,原子吸收法只有2-3个数量级),价格便宜(一般一台发光仪1-2万左右)等优点,在食品分析领域得到迅速发展,是目前测定食品中重金属含量前景非常大的一种方法。据此本文建立瞬稳静态注射化学发光测定水果中痕量铬的新方法,结果令人满意。
1材料和方法
1.1实验原理
水果中的有机物可以被浓硝酸与高氯酸的混酸氧化,生成二氧化碳、水、氮气等氧化产物。有机物中常见非金属元素原子(C、H、O、N、P、S)氧化后大部分以气体形式逸出,金属元素原子则以高价离子形式存在于溶液中,水果中各种价态的铬可被硼氢化钾还原为三价铬,三价铬可以催化双氧水与鲁米诺的反应,在低浓度条件下,反应速度与催化剂浓度有关。
1.2实验材料
1.2.1实验仪器
YN-FG1型瞬稳静态注射化学发光分析仪(河南农业大学迅捷测试技术有限公司),YN-2000微电脑多功能养分速测仪(河南农大机电技术开发中心),消化仪,电炉,移液管,烧杯,三角瓶,反应瓶,玻璃棒,50 ml比色管,500ml、100ml、50ml容量瓶。
1.2.2实验试剂
1.2.2.1消化用混酸
500ml容量瓶中加入300.0ml浓硝酸,50.0浓高氯酸,按先后顺序,振荡摇匀。
1.2.2.2 3%NaOH
称取1.20g分析纯NaOH置于40ml小烧杯中,加水至标线,搅拌均匀,冷却后用移液管转移到滴瓶中。
1.2.2.3 30%NaOH
称取12.00g分析纯NaOH置于40ml小烧杯中,加水至标线,搅拌均匀,冷却后用移液管转移到滴瓶中。
1.2.2.4 0.5mol/LHCl
用吸量管取33.33ml分析纯浓盐酸置于100ml容量瓶中,加水至标线摇匀,此时浓度为4mol/L,取12.50ml置于100ml容量瓶中,加水至标线摇匀,此时浓度为0.5mol/L。
1.2.2.5 硼氢化钾溶液
称取分析纯硼氢化钾0.10g,溶于事先加入3%NaOH5滴的约10ml水中,定容到100ml,摇匀,此时浓度约为0.1%,取10.00ml置于100ml容量瓶中,定容到100ml,摇匀,此时浓度约为0.01%,用移液管转移到滴定瓶中。
1.2.2.6 EDTA溶液
称取3.72g分析纯EDTA,溶于约50ml 水中,转移到100ml容量瓶中,定容摇匀,此时所得EDTA浓度为0.1mol/L。
1.2.2.7 H2O2工作液
量取10ml 0.1mol/LEDTA,加入事先加入60.00ml去离子水的100ml容量瓶中,加入1.00ml分析纯H2O2(30%),定容摇匀。
1.2.2.8 鲁米诺工作液
500ml容量瓶中加入200ml左右的去离子水,加入50.00ml鲁米诺储备液(2.5*103mol/L),加入1.8g分析纯NaOH,定容,摇匀。
1.2.3 实验样品
红富士苹果,新郑大枣,均买自丹尼斯超市。
1.3 实验方法
1.3.1 Cr6+系列浓度标准溶液制备
称取分析纯重铬酸钾0.02834g置于100ml容量瓶中,加入少量去离子水,振荡溶解,加入浓HCl 3滴,定容,此时Cr6+的浓度为100mg/L。然后100mg/L的Cr6+依次稀释到1.5 mg/L、1.0 mg/L、0.5 mg/L、0.1 mg/L、0.05 mg/L、0.01 mg/L这几个浓度。
1.3.2消化水果样品的制备
称取5.00g水果样品置于事先洗干净的500ml磨砂口的三角瓶中,待测样品加入2ml去离子水,加入35.0ml混酸,2.0ml浓硫酸,投入5粒左右玻璃珠,连接到消化装置上,在电炉上小火加热至液面泛起大气泡,停止加热,当酸液中固形物基本消失时继续加热,当溶液开始显黑色时取下三角瓶,稍冷后加入5.0ml浓硝酸,继续加热,如果加热过程中个别样品又显黑色,则所有样品中添加同样量的浓硝酸。当三角瓶口烟雾上下翻腾而不从瓶口逸出,停止加热,稍冷,用约20ml去离子水冲洗瓶壁,继续加热至三角瓶中溶液约剩2.00ml,并且颜色变为无色时,准确稀释到50ml。空白与标准溶液的制备方法与此相同。
1.3.3 待测溶液的制备
取待测液10.00ml置于比色管中,同时做空白与标准,加入20滴30%NaOH,摇匀,加入一滴酚酞,用30%NaOH调整至恰显红色。用0.5mol/LHCl调整pH值至红色恰好消失,充分摇匀后用0.3%NaOH调整至刚显红色,加入1.00ml0.5mol/LHCl溶液,摇匀,加入4滴0.01%硼氢化钾溶液,摇匀,静置5分钟,加入1.00ml0.1mol/LEDTA溶液,加入2.00mlH2O2工作液,摇匀定容。
1.3.4 上机测定
1.3.4.1 仪器本底的测定
打开主机电源,预热20min,同时打开进液阀和放液阀,对仪器储夜池用蒸馏水进行冲洗,少量多次,调节仪器测定参数,测试类型选择本底测量,合上仪器盖子,关闭进液阀和放液阀,按下开始测量,待进样灯亮的同时打开进样阀,反应停止后记录实验数据。
1.3.4.2空白样品的测定
打开进液阀和放液阀,对仪器储夜池用蒸馏水进行冲洗,少量多次,调节仪器测定参数(同测定仪器本底时相同),测试类型选择空白测量,关闭进液阀和放液阀,在漏斗1中加入2.00ml鲁米诺发光试剂,漏斗2中加入2.00ml空白试剂,合上仪器盖子,按下开始测量,待进样灯亮的同时打开进样阀,反应停止后记录实验数据。
1.3.4.3标准数据的测定
打开进液阀和放液阀,对仪器储夜池用蒸馏水进行冲洗,少量多次,调节仪器测定参数(同测定仪器本底时相同),测试类型选择标准测量,在漏斗1中加入2.00ml鲁米诺发光试剂,漏斗2中加入2.00ml标准试剂,合上仪器盖子,关闭进液阀和放液阀,按下开始测量,待进样灯亮的同时打开进样阀,反应停止后记录实验数据。
1.3.4.4待测样品的测定
打开进液阀和放液阀,对仪器储夜池用蒸馏水进行冲洗,少量多次,调节仪器测定参数(同测定仪器本底时相同),测试类型选择空白测量,关闭进液阀和放液阀,在漏斗1中加入2.00ml鲁米诺发光试剂,漏斗2中加入2.00ml待测样品,合上仪器盖子,按下开始测量,待进样灯亮的同时打开进样阀,反应停止后记录实验数据。
2结果与分析
2.1 化学发光仪测定参数的选择
为了增加测定的准确性,本实验对化学发光仪测定参数进行了一系列的选择,测定结果如表1:
表1
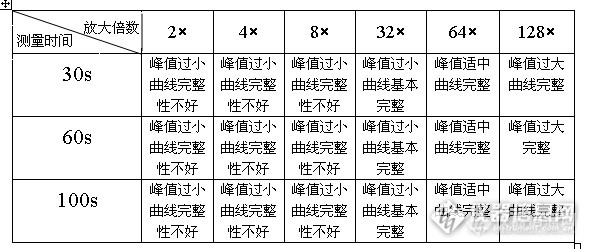
根据测量结果,最后确定的最适宜的测量参数为:测量时间:100s ,放大倍数:64×,浓度单位:mg/kg, 测试模式:发光强度。
2.2 反应溶液PH的选择
本实验选择了硼氢化钾作为氧化剂,而硼氢化钾在酸性条件条件下才表现出强的氧化性。实验选取了1.5, 2.0, 2.5, 3.0, 3.5, 4.0, 4.5, 5.0, 6.0, 7.0十个PH,分别测定浓度为1.0mg/L的Cr6+标准液在各个PH 的发光强度(以发光曲线的积分面积表示),测定结果如表2:
表2
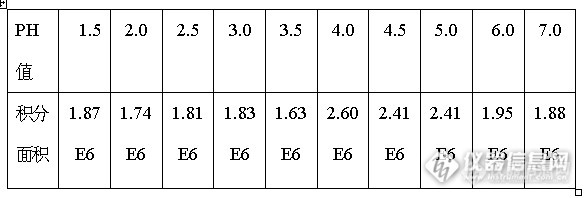
以PH值为X轴,积分面积为Y轴作曲线图如下:
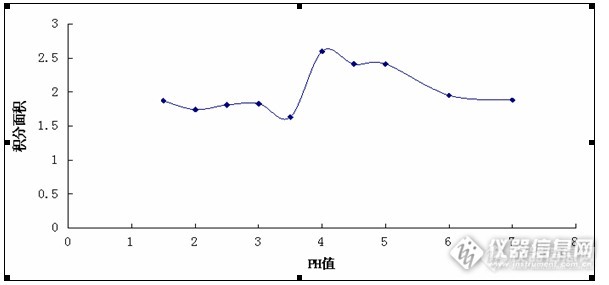
根据曲线图可以看出,开始发光强度随着PH值的增加而增加,达到一定程度,又随着PH值的增加而减小。在反应溶液的PH值为4.0的时候,发光强度达到最大,但稳定性不好,而在PH在4.5-5.0的时候发光强度较大,并且比较稳定,因此本实验反应溶液的PH选4.5。
2.3 试液中的EDTA浓度
EDTA可与大多数金属离子迅速形成稳定的络台物,但与铬(Ⅲ)离子成络合物很慢。所以,向试液中加入EDTA,在其未与铬(Ⅲ)离子成络合物时就进行发光测定,则可排除多数离子的干扰。但是,如果EDTA浓度太高,它就会与铬(Ⅲ)离子以明显的速度络合,反而干扰测定。
实验表明,试液中的EDTA的浓度低于2 x 10-3M时,反应的发光强度保持不变,高于此数值时,发光强度明显减小。本文选用l x 10-3M为试液中EDTA的浓度。
2.4校准曲线和相对标准偏差
在最佳实验条件下,铬(Ⅲ)试液在1.00×10-5一1.00 x lO-3mg/mL浓度范围内,化学发光强度与其浓度呈较好的线性关系,本实验分别测定了浓度为1.5×103mg/mL,1.O×103mg/mL,0.5×103mg/mL,0.1×103mg/mL,0.05×103mg/mL,0.01×103mg/mL的六价铬标准液进行了测定,结果见表3,标准曲线为y= 4.9913x+2.9113,R^2=0.9956(不含空白),y=5.0097x+2.7907,R^2=0.9928(含空白)。对浓度为1.00×103mg/mL六价铬的标准溶液进行10次平行测定,其相对标准偏差为0.6%。
表3
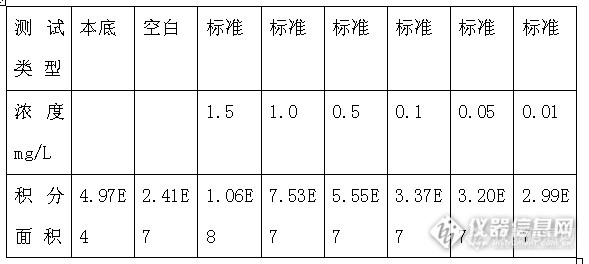
不加空白的标准曲线:
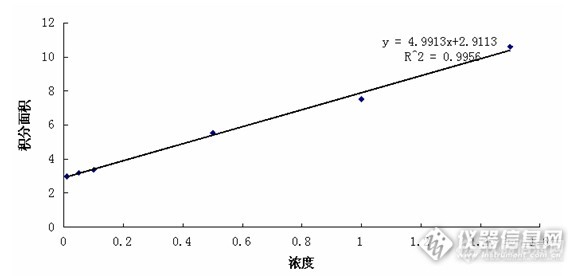
加空白的标准曲线:
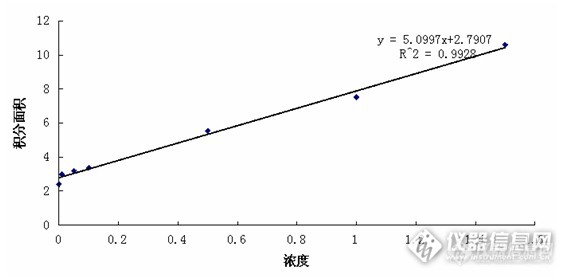
2.5 样品的测定
2.51 样品回收率的测定
在最佳实验条件下对苹果和红枣两种样品进行了测定,消化过直接定容到50ml并经过一系列处理的待测液发光强度过大,因此对其进行了一系列的稀释,并进行测定,发现稀释5倍时发光强度适中。同时对取样量和加标量进行了实验,当取样量为2ml,加标量为10ml(1.00mg/L)时,样品,样品加标准,标准的发光强度均在标准曲线范围内,符合要求。实验结果如表4。
表4
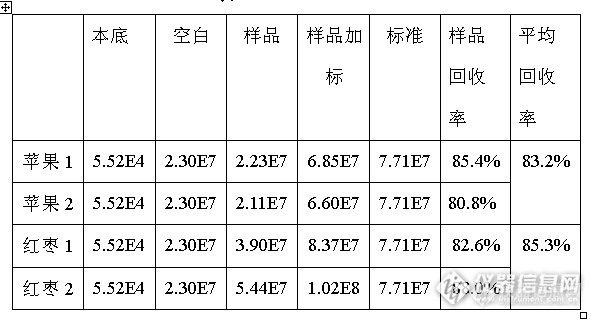
3 结论与讨论
对水果中微量元素含量进行分析研究,尤其是严格控制水果中重金属元素含量,制定统一方便有效的分析测定标准和方法,保证食品质量安全迫在眉睫。其中检测方法的选择性与灵敏度是非常关键的因素。利用该方法实现对苹果和红枣中总铬的定量分析,结果令人满意。实验表明,测量时间为100s,放大倍数为64,EDTA浓度为0.1mol/L,铬(Ⅲ)试液的pH为4.5的条件下,化学发光强度最强。该方法操作简单、快速、检测限低、结果准确可靠,从而拓宽瞬稳静态注射发光法的应用范围,对水果中其他微量金属的研究,以及其他水果中微量金属的研究提供新思路。但该法最大的不足是共存元素的干扰大,但加入掩蔽剂或与现代分离技术联用可克服这一问题。瞬稳静态注射化学发光分析方法用于水果分析还需进一步研究和完善。








