

ICP-MS测定XX中药注射液中重金属及有害元素的基质干扰试验研究
一、实验目的
样品的分解与溶解是分析中的一个重要部分,采用仪器法对中药中的痕量有害元素进行残留分析时,一般均需经过将样品中的有机物消解破坏,完全转溶于水或者稀酸的过程,其作用有三:首先,将样品转变成溶液形式,以满足一般仪器分析的进样要求;其次,待测金属元素在样品中经常以不同的形态、价态方式存在,在对其总量的测定过程中,需将不同的有机态、络合态、不同价态的形式转化为同一种无机态,以保证测定结果的准确;再次,中药有机体成分复杂,对测定可能形成较强的基质干扰,需预先加以破坏、排除。中药注射液多为澄明液体,采用上述三种方法测定时,理论上均可以不经消解有机破坏处理,直接或适当稀释后进样。实验首先考虑样品基质的干扰,对样品稀释后直接进样,通过回收率反映是否有基质干扰。如无基质干扰,则可以将样品稀释后直接进样,简化操作,节省人力物力;如有基质干扰,则应设计合理的样品消解条件,对样品消解后再进样分析。
二、试剂与仪器
1.1 仪器:电子天平(型号 XS 105DU,型号 FX-200),电感耦合等离子体质谱仪ICP-MS(型号为安捷伦 7700),Milli-Q 超纯水处理系统,微波消解仪(CEM MARS5)。
1.2 试剂:水为高纯水,硝酸为色谱级(Fisher scientific),调谐溶液为 Li、Mg、Y、Ce、Tl、Co 的混合标准溶液(Agilent 公司,质量浓度为 1 μg·L-1,);内标溶液为 100 μg·mL-1 的 Li、Sc、Ge、Rh、In、Tb、Lu、Bi 的混合内标溶液稀释 100 倍使用(Agilent 公司,批号 5188-6525),高纯氩气(北京诚维信科技发展公司)。
三、标准溶液的配制
3.1、储备液及标准曲线的制备
混合标准溶液的制备(临用现配): 精密量取砷标准溶液 1ml 置 10ml 量瓶中,5%硝酸溶液定容至刻度,配成砷标准储备溶液;另精密量取镉标准溶液 1ml、汞标准溶液 1ml 置 100ml 量瓶中,5%硝酸溶液定容至刻度,配成镉、汞混合标准储备溶液。分别取镉汞储备溶液 1ml、砷储备液 1ml、铅标准溶液 2ml、铜标液 1ml 置 100ml 量瓶中,用 5%硝酸溶液定容至刻度,摇匀,制成每 1ml 含铜(Cu)10μg,铅(Pb)2μg,砷(As)1μg,镉(Cd)0.1μg,汞(Hg)0.1μg 的混合标准溶液。
3.2、标准曲线的制备:分别精密量取混合标准溶液 10.0、5.0、2.0、1.0ml,各置100ml 量瓶中,加 5%硝酸溶液稀释至刻度,得标准曲线第 7 点、第 6 点、第 5点第 4 点混合标准溶液;再分别精密量取标准曲线第 7 点混合标准溶液 5.0、2.0、1.0ml,各置 100ml 量瓶中,加 5%硝酸溶液稀释至刻度,得标准曲线第 3点、第 2 点、第 1 点,绘制标准曲线。
3.3、工作曲线标准溶液中不同元素浓度见下表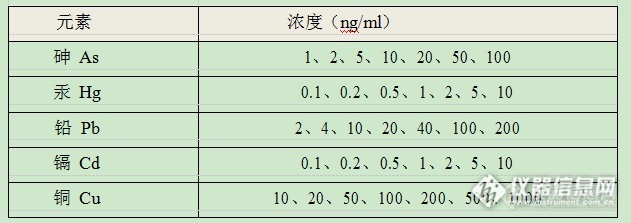
四、测定条件
4.1 、质谱条件
反馈功率为 5W,射频功率为 1550W,载气(高纯氩气)流速为 1.05 L•min-1,等离子气体流速为 15.0L•min-1,蠕动泵转速 0.3rps,采样深度 8mm,检测质量数m/z=75(As),采样周期为 0.1s。
4.2、 同位素和内标选择
测定时选取的同位素为 63Cu、75As、114Cd、202Hg 和 208Pb,按照内标同位素质量数与待测元素质量数相近的原则,63Cu、75A s 以 72Ge 作为内标,114C d 115 I n 作为内标,202Hg、208P b 以 209B i 作为内标,并根据仪器的要求选用适宜校正方程对测定的元素进行校正。
4.3、内标溶液的制备:(0~5℃密封贮存)精密量取含 72Ge、115In、209Bi 的混合内标液适量,置量瓶中,用 5%硝酸溶液稀释至刻度(含72Ge、115In、209Bi 1ug/ml)
(图片来自网络如有冒犯请多多谅解)
五、样品制备及测定结果
5.1、XX注射液每日最大用量为 40ml,按照《中国药典》2015 版注射液限度规定,按各品种项下每日最大使用量计算,铅不得超过 12ug,镉不得超过 3ug,砷不得超过 6ug,汞不得超过 2ug,铜不得超过 150ug,计算后限度为:铅不得过 0.3ug/ml,镉不得超过 0.075ug/ml,砷不得超过 0.15ug/ml,汞不得超过 0.05ug/ml,铜不得超过 3.75ug/ml。
5.2、供试品溶液制备:XX注射液(批号 20161035)精密量取 3ml,置 50ml量瓶中,用 5%硝酸稀释至刻度摇匀即得,平行制备两份样品。
5.3、加标回收样品制备:复方苦参注射液(批号 20161035)精密量取 3ml,置50ml 量瓶中,再精密量取标准储备液 1ml,加入量瓶中,用 5%硝酸稀释至刻度摇匀即得,平行制备两份。
5.4、结果如下表 所示: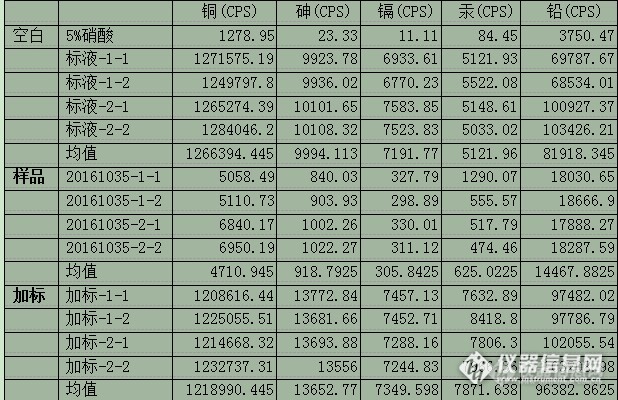


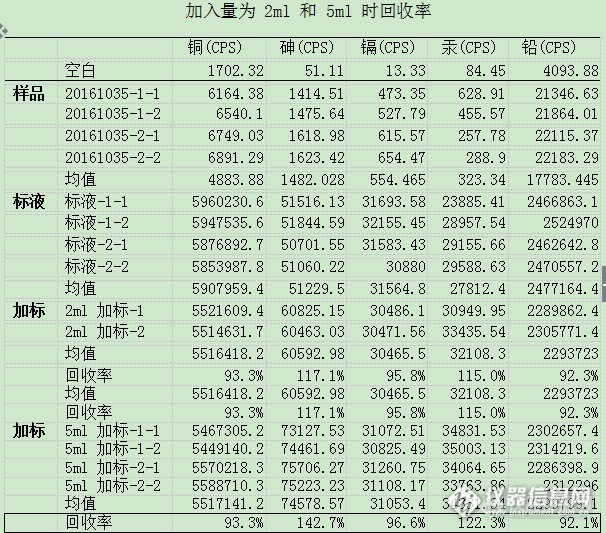
从检测结果来看,其基质对砷和汞测定均有干扰,在取样为 2ml 时,基质干扰明显减弱,回收趋于正常水平。但是在此稀释倍数下,取样较少时,其样品限
度落在标曲线性范围以外,检测灵敏度难以满足风险评估要求,所以需要进一步考察消解条件。
六、微波消解条件考察
6.1、条件 1:
精密量取待测样品(批号 20161035)3ml,分别置微波消解罐中,加硝酸 8.0ml,置加热板 120℃加热 2h,取出消解罐,放冷,将消解液转入 50ml 量瓶中,用少
量水洗涤消解罐 3 次,洗液合并量瓶中,用水定容至刻度,摇匀。同时制备空白试剂。
6.2、 条件 2:
精密量取待测样品(批号 20161035)3ml,分别置微波消解罐中,加硝酸 8.0ml,按操作规程安装好装置,消解(3 分钟升温至 120℃保持 3 分钟,2 分钟升温至
150℃保持 3 分钟,2 分钟升温至 190℃保持 10 分钟),消解结束后,冷却至 60℃以下,取出消解罐,放冷,将消解液转入 50ml 量瓶中,用少量水洗涤消解罐 3
次,洗液合并量瓶中,用水定容至刻度,摇匀。同时制备空白试剂。
6.3、两个条件结果对比: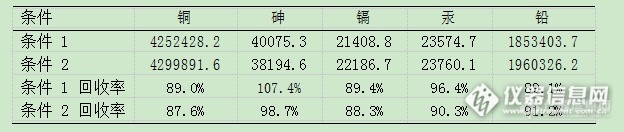
实验发现,消解条件下,砷和汞的回收率均在正常水平范围内,明显排除了基质干扰,其他元素回收率在正常水平内;对比两种消解条件,其结果差异并
不大,而条件 1 为直接加热,操作简单,条件 2 为微波消解,消解后需进行赶酸,操作相对复杂,综合考虑,选择条件1为样品前处理条件。
6.4、加热时间的考察
精密量取待测样品(批号 20161035)3ml,分别置微波消解罐中,加硝酸 8.0ml,置加热板 120℃加热,分别加热 1、2、3、4、5h,结果如下表所示: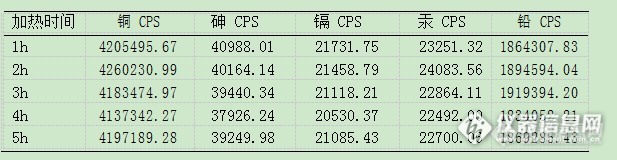
由测定结果可知,加热 1h 以上均可,考虑到样品基质复杂, 排除不确定因素干扰,所以选择加热 2h,使其充分消化,更彻底去除基质干扰。
总结: 通过对以上数据分析,确定本检验方法的样品前处理方法为:精密量取本品 3ml,加硝酸 8ml,置加热板 120℃加热2h,放冷,将消解液转入 50ml量瓶中,用少量水洗涤容器 3 次,洗液合并量瓶中,用水定容至刻度,摇匀。同法制备试剂空白溶液。