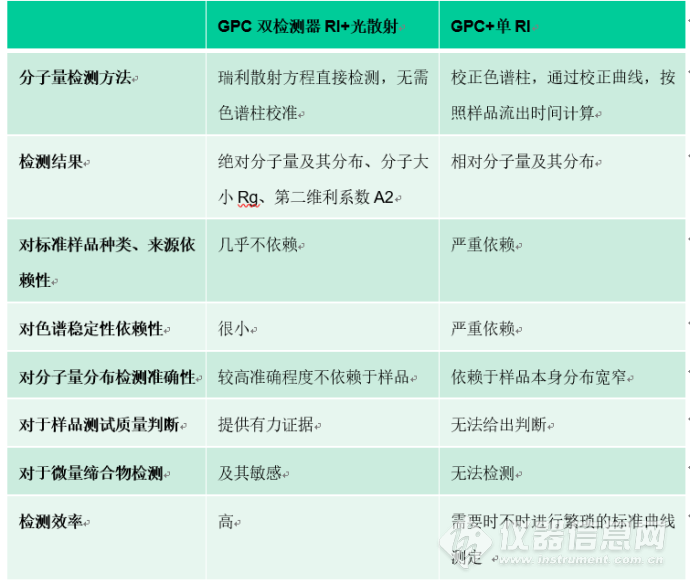
介绍过传统校正对于相对分子量的检测方法,以及光散射技术对于绝对分子量的检测原理,下面我们通过检测概念、标准样品影响、保留时间影响、对于分布检测的准确性、测试质量判断、对于团聚物的检测以及检测效率几个方面来了解一下GPC技术需要和光散射技术联合使用。
检测概念
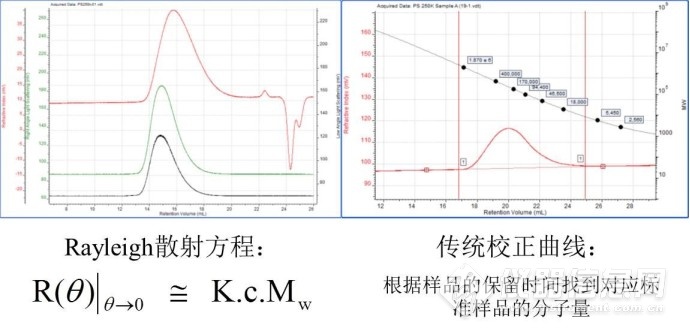
光散射法和传统法色谱信号区别
通过RI和光散射检测器连用,凝胶渗透色谱GPC/SEC在一个测试过程中同时收集RI和光散射信号,得到绝对分子量Mw、Mn、Mz,分子量分布,均方旋转半径和第二维利系数。而通过传统校正在一个测试过程中收集RI信号,得到相对分子量Mw、Mn、Mz,分子量分布。
相对分子量的检测的准确性依赖于很多条件,但最关键的一点是溶解在溶剂中的高分子线团的流体力学体积,因为流体力学体积的大小和分布决定了样品的流出时间也就决定了所得到的相对分子量的数值和重复性。
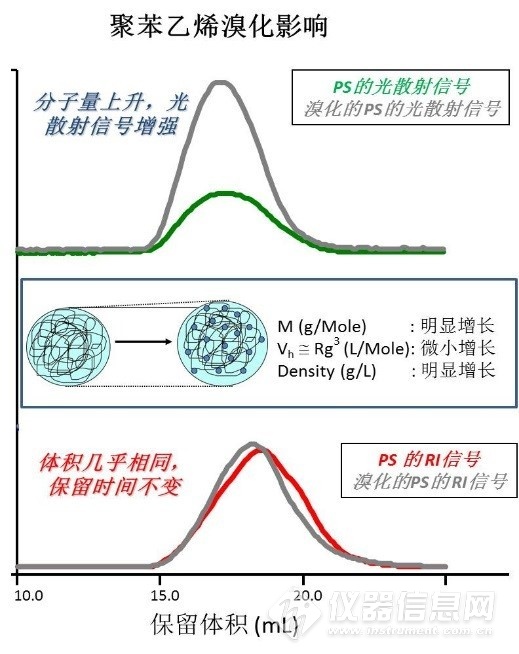
光散射信号和RI信号对于聚苯乙烯及其溴化聚苯乙烯的响应
上面的一个例子中,通过两种不同的检测方法检测了两个样品。一个是聚苯乙烯,另外一个是溴化聚苯乙烯。溴元素是质量很大但是体积很小的元素,溴化的聚苯乙烯和没有溴化的聚苯乙烯相比分子量有明显的升高,但是分子体积基本不变。通过测试我们发现,传统校正下,对于聚苯乙烯和溴化聚苯乙烯的RI信号几乎没有区别,因此传统校正得到的结论是相对分子量没有改变,而通过光散射检测器我们可以看到,溴化之后的散射光强明显加强,说明分子量增大。光散射得到的绝对分子量告诉我们,溴化后的聚苯乙烯分子量是62万,而没有溴化的聚苯乙烯的分子量是25万!
我们再来看一个蛋白质测试的例子。蛋白质样品本身是多肽的四级堆积结构,分子密度较高,而不同聚集态的蛋白团聚物之间的分子密度差别很大,这就导致了相对分子量和其真实分子量之间差别很大。
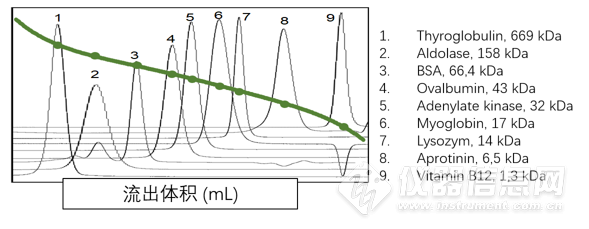
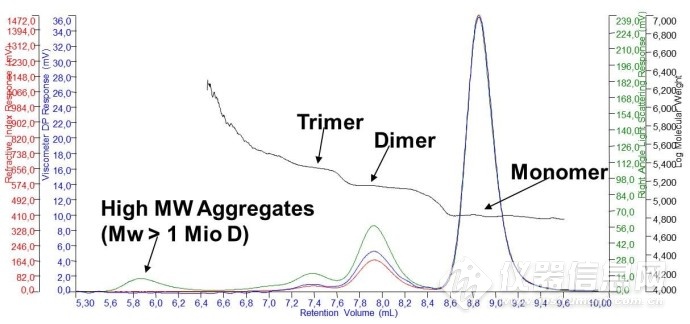
这个例子中我们首先使用一系列蛋白进行了传统校正曲线的绘制,如上图
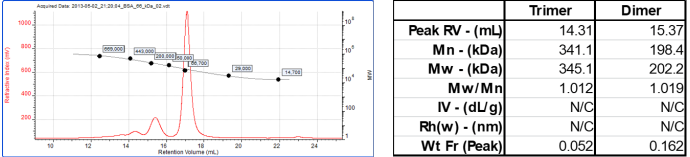
利用传统校正曲线检测BSA牛血清白蛋白样品(单体分子量66.4KDa),如上图我们可以看到,其二聚体和三聚体Mw分别得到202KDa和345 Da,这些寡聚体的分子量与其真实值有着明显的偏差。
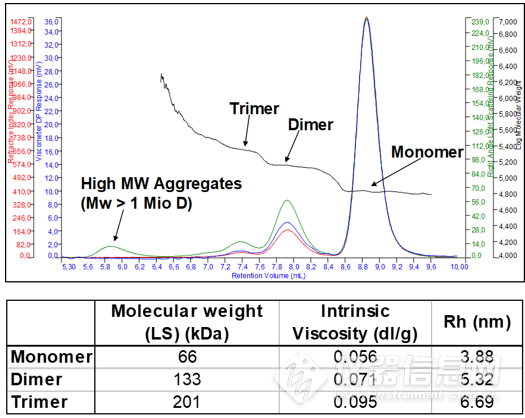
而通过光散射检测器得到的结果单体66 K Da,二聚体133 K Da,三聚体201 K Da,这与其真实值具有高度的一致性!
标准样品影响

LS = KLS• (dn/dc)^2•M•C
RI = KRI•(dn/dc)•C
通过光散射检测器检测绝对分子量只需要仪器常数KLS和KRI,而仪器常数只取决于流动相的种类、检测温度,不取决于任何标准样品以及标准样品的种类。
而对于传统校正而言,其计算结果严重依赖于标准样品的种类和来源!相对分子量的计算取决于校正曲线,所有影响校正曲线的因素将对于计算结果造成影响,而标准样品是影响校正曲线的重要因素之一。使用不同高分子标准样品由于分子密度的差异,得到不同的标准曲线。即使使用同一种标准样品,相同供应商的不同批次,校正曲线也会有所差异,导致分子量结果不同
保留时间影响
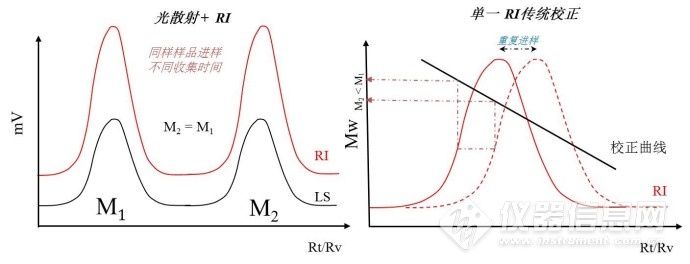
保留时间对于光散射检测和传统检测的意义
通过光散射检测器检测绝对分子量不依赖于样品信号保留时间!分子量结果和重复性只与RI和光散射信号强度相关,与保留时间无关,因而可以得到极高的准确性和重复性。
传统校正严重依赖于样品信号保留时间!由于色谱柱老化,色谱泵不稳定,测试温度波动造成的样品RI信号保留时间的改变会造成分子量结果的明显差异。
对分子量分布的检测准确性
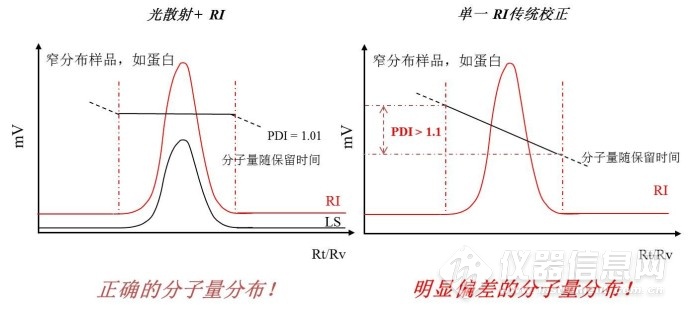
高分子分布信息的准确性取决于分子量检测的准确性。对于窄分布样品如蛋白质,光散射得到的绝对分子量能够正确地表征样品的分布信息。而传统校正由于其分子量是通过校正曲线得到,其分子量在不同的流出时间在校正曲线上有所差别,所以得到的分子量分布与样品的真实结果会有明显偏大。这将影响到检测者得到正确的结论。
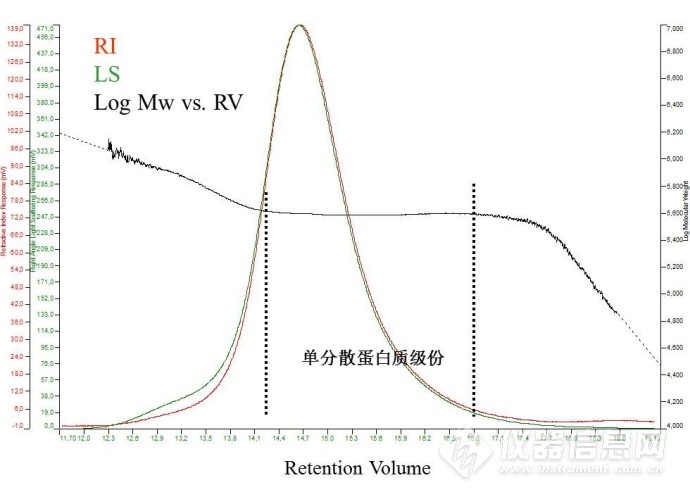
典型的蛋白质色谱流出曲线
判断测试质量
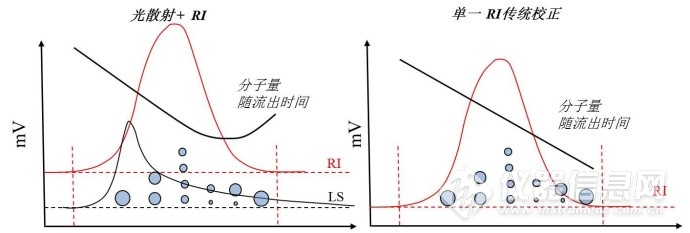
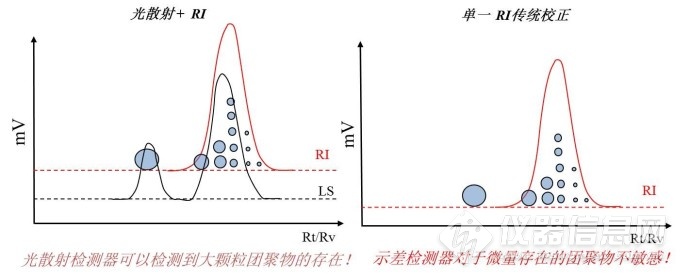
绝对分子量分布和相对分子量分布对于信号质量的判断
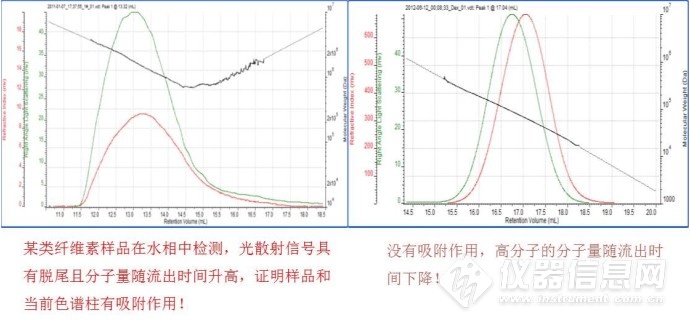
通过光散射和RI检测器的结合使用,还可以有效判断GPC的测试质量。在GPC检测过程中如果在错误的制备条件下检测样品,(意味着流动相、色谱柱种类错误),都可能造成高分子样品在色谱柱上的吸附。而高分子在色谱柱上的吸附将会造成GPC在分离过程中高分子材料不按照从大到小的顺序流出,这将导致错误的分子量和分子量分布结果。通过光散射检测器和RI检测结合,可以得知样品在色谱柱上有无吸附,判断依据如下:
[list=disc]