CNS_20.002_明胶
方佳华
二〇二一 年 七 月
摘 要
明胶作为应用广泛高分子物质,具有良好的成膜性、凝胶性、生物可降解性、生物相容性。本文简要介绍作为食品添加剂——明胶的相关理化性质、分子量分布的测定方法,改性方法及其在感光工业、食品、医药、化妆品、纺织、造纸、防腐抗蚀、化工等行业应用情况,和国家标准对其的规范。
关键词:食品添加剂;明胶;检测;应用
引言
食品添加剂是为改善食品品质、色、香、味,以及为防腐和加工工艺的需要而加入食品中的化学合成或者天然物质。其对于防止食品腐败变质,保证食品供应,满足人们对食品营养、质量以及色、香、味的追求,起到了重要作用。
长期以来,有人混淆了食品添加剂和非食用物质的界限,将从事违法犯罪活动。“牛肉膏”、“甲醛泡海参”、“水煮明胶似肉冻”、“橡皮杨是皮鞋做的”等食品添加剂滥用现象、非法原料生产现象等层出不穷,其加深了公众对食品添加剂的误解。让消费者正确认识食品添加剂,没必要谈“剂”色变,是至关重要。


图1[2] 明胶在食品中的应用(左) 禁止的明胶生产原料(右)
明胶是常用的食品添加剂之一,其是以牛、猪等动物骨、皮为工业原料,经一系列预处理、净化,提取出其中的胶原,使其适度降解,再通过热变性等工序而制得。明胶作为一种天然生物高分子材料,其具有生物可降解性、良好的生物相容性和凝胶性、低成本等优点,使其成为最早的商品化蛋白质。在感光材料、食品、医药、化妆品、造纸、防腐抗蚀、选矿、建材、化工等行业和许多产品中获得广泛应用,并产生了很高的经济效益。本文以食品中几乎处处可见的明胶为切入点,简要介绍明胶的相关理化性质、分子量分布的测定方法、改性方法、应用以及国家的规范标准。
1 明胶
按照 A.G.Ward 的定义,明胶( gelatine 或 gelatin )是胶原经温和而不可逆的断裂后的主要产物[1]。胶原通常是由3条多肽链相互缠绕所成的螺旋体,历经变性分解可形成单条多肽链(α-链)的α-组分、由两条α链组成的β-组分和由三条α链组成的γ-组分,以及介于其间和小于α-组分或大于γ-组分的分子链碎片(图1)。
明胶含有18种氨基酸,不同于蛋白质构成的20种,其缺少色氨酸,而半胱氨酸(及胱氨酸)是从明胶生产原料通过加工过程作为微量杂质而混入的。明胶的多肽长链中,甘氨酸占三分之一,即甘氨酸在明胶分子链中出现的周期性为3;其它氨基酸的周期性:脯氨酸为6,羟脯氨酸和丙氨酸为9,精氨酸为18,赖氨酸为24等。
明胶与胶原具有同源性。胶原具有棒状三股螺旋结构(图1 b),当其部分水解制备明胶的过程中,胶原的这种三螺旋结构发生部分分离和断裂。二者的氨基酸组成相似,但因预处理的差异,组成成分也可能不同。
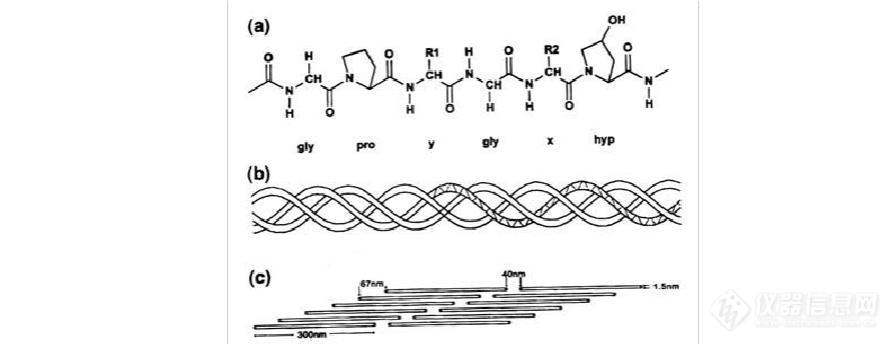
图2[2] (a):胶原分子式;(b)3条多肽链螺旋体; (c):明胶
1.1 明胶分子量分布MWD
明胶是一个具有一定分子量分布的多分散体系,其分子量分布于几千到几十万不等,且因工艺条件不同而有所差别。一般而言,碱法胶MWD比较集中,α、β的相对含量较高,小分子量所占百分比小;而酸法胶相对具有比较宽的MWD,且小分子部分含量大[3]。明胶的重要理化性质,例黏度、胶冻强度、冻点、溶解性都与分子量分面有密切关系。
1.1.1 早期MWD测定方法
在早期的明胶MWD研究中,主要采用的方法包括粘度法、渗透压法、超速离心法、光散射法等。
粘度法是通过测定明胶的粘度并进而求算明胶分子量的一种方法,明胶的特性粘度[η]与分子量Mn存在[η]=K[Mn]的经验关系;基于实验研究作lg[Mn]-lg[η]图,可得到[η]的分布曲线来表示明胶的分子量分布。渗透压法也是间接的测量方法。J. Pouradier等人用渗透压法对分子量为65000的碱法明胶以醇凝絮法进行了分级,粗略得到M=31000050000[3]。光散射法是利用明胶的胶体特性,通过散射角度与分子大小的关系来确定分子量的方法。
超速离心法是把高聚物溶液(1%)放入离心场中,以每分钟50000转左右的超离心速度进行沉降,离心机所装备的Schlieven光学系统能显示折射率梯度(反映溶液及溶剂的界面移动)随与转子中心的距离而变化的图像[4]。在固定浓度、转速、温度、时间等条件下,观测并用摄影法记录下不同胶样在离心时的迁移距离x值,根据x-t的线性图,按式1可得沉降常数S值(其中为角速度),并判断不同胶样在分子量上的定性差别。
(式1)
高奇香、彭必先等[5]用高速离心沉降平衡法对一系列国内外的明胶的沉降常数进行了测定,可发现不同类型、同工艺制得的明胶的沉降常数K差别较大。
上述几种方法,由于准确性和重复性不很高,只能定性地或半定量地比较不同明胶的分子量分布,无法对明胶中各个不同组份,如α、β、γ进行单独的测定和表征,更谈不上对不同构象组份的分离。它们仅能粗略给出MWD的数据,难以得到更大的发展[4]。
1.1.2 聚丙烯酰胺凝胶电泳(SDS-PAGE)法
聚丙烯酰胺凝胶电泳可根据不同蛋白质分子所带电荷的差异及分子大小的不同所产生的不同迁移率将蛋白质分离成若干条区带。SDS作为阴离子表面活性剂能打断蛋白质的氢键和疏水键,并按一定的比例和蛋白质分子结合成复合物,使蛋白质带负电荷的量远远超过其本身原有的电荷,掩盖了各种蛋白分子间天然的电荷差异[4]。基于此,各种蛋白质-SDS复合物在电泳时的迁移率,不再受原有电荷和分子形状的影响,而只是棒长的函数。
已有研究,如Ebihara等用SDS-PAGE法来表征胃蛋白酶降解明胶的分子量分布,结果表明在15kDa、17kDa、36kDa和60kDa处有特征谱带[6]。
明胶作为棒状蛋白,在进入凝胶板内所要求的分子筛的孔径比普通球形蛋白要大,特别是两根棒状蛋白交叉排列在一起更甚。实践证明,高分子量的明胶中不同构象组份难以进行完全的分离。所以SDS-PAGE测定明胶分子量分布时若采用球蛋白作marker,只能表征明胶的大概分子量范围,并不能得到准确值,精确分子量需要进行修正[4]。
1.1.3 高效液相色谱法
随着蛋白分离技术的进步、高分辨率、高稳定性固定相的应用,以及检测器
的改进和计算机的应用,越来越多的人运用高压液相色谱来进行明胶组份的分离和表征。具有体积排阻效应的凝胶过滤色谱柱在大分子蛋白测定的HPLC应用较广。如T. ohno等[7]用Asahipak (GS2G7B+GS620x2)为色谱柱,0.2M 磷酸缓冲液为洗脱液测定了不同喷射方式、喷射压力下得到的明胶的分子量分布。美国杜邦公司研究所的J. Beutel用HPLC测定了部分IAG明胶的分子量分布,解析了计算机得到的色谱图,并求算出α、β、γ组份的百分比[4]。D. Lorry等[5]利用已知校正蓝线和电子计算机处理分离效果低的色谱图,给出一系列IAG明胶的色谱分离分析结果。
1.2 明胶的理化性质
1.2.1 等电点
徐文达[8]指出,等电点是指胶体大分子溶解于一定组成的缓冲溶液中不发生电泳时此缓冲溶液的pH值,表明等电点与缓冲溶液的离子强度有关,且用等电聚焦法测得的结果即为等电点。酸法猪皮明胶的等电点一般在pH 7.5-9的范围
内,而碱法明胶的等电点在pH 4.8-5.0范围内。这两种不同工艺制得的明胶相混合使用时会出现不相容的现象,如乳剂分层 、透明度降低、凝聚等[9]。故在混胶时要注意胶的等电点及使用时的pH。
1.2.2 表面活性
由氨基酸构成的多肽链存在着亲水区和疏水区,因而明胶和一些表面活性剂一样具有适当的表面活性。研究表明,明胶溶液的表面张力与其浓度、温度、pH值等因素有关。在明胶溶液浓度为1%或1%以下、温度为10-45℃,在溶液形成少于1小时的界面上进行测定,发现pH 2-3间其表面张力最大,而最小表面张力则出现在等电点处[1]。此外,表面张力在30℃以下同温度呈负线性相关,30-40℃间更为剧烈,在40℃以上时随着温度断增高进一步下降,其下降速率比纯水的要大[1]。
1.2.3 凝胶强度
明胶凝胶是具备弹性并保持一定形状类似于固体的物质,其在受热后能可逆地又转变为溶液状态。凝胶强度数值为明胶重要表征值,是明胶溶液在低温下冷却至发生凝胶化并在一定的低温下老化一定时间所测得。明胶的凝胶强度与明胶的分子量及其分布、氨基酸组成及工艺过程有关,不同用途的明胶所要求的凝胶强度也不同[1]。
明胶溶液的凝冻及其随后的凝胶网络的变化是由于溶液中无序明胶分子部分地回复到胶原结构而引起的[1]。彭必先、陈丽娟[10]测定明胶各个组分发现,α、β组分含量的增加将有利于凝胶强度值的提高。
1.2.4 粘度
黏度反映了微小的纤维状肽链分子溶解并分散在水中时因相对运动而产生的内摩擦力。对于稀溶液来说,由于体系中分子数极少,内摩擦力几乎为零,其所表现出的黏度反映了多肽链体系平均分子量的大小。基于此,在固定温度、pH等的条件下,稀溶液的黏度测定主要用于测定明胶体系的平均分子量。而在浓溶液的情况下,其黏度主要是由明胶分子之间的流体力学的相互作用所引起的。在明胶浓溶液的浓度范围内,影响黏度的主要变量是温度、pH值和所加的盐类[1];此外,明胶的平均分子量和分子量分布也影响到明胶的黏度。
1.3 明胶的分类
明胶按照生产方式分为B型明胶、A型明胶、酶法明胶。三种明胶最大的不同点即为前处理过程采用方法不同。B型明胶以2-5年牛皮及牛骨等为原料,经预处理,后中性介质提取可得等电点在5.4-5.3[11]间的明胶。A型明胶一般以6-9个9月猪皮及骨头或牛小骨为原料,在酸性介质中预处理并提取得到等电点在6.8-8.5(骨胶)及7.5-9.5(皮胶)间的明胶[11]。酶法明胶是指原料经酶预处理,在适度pH值的介质中提取的明胶。
明胶按照用途可以分为食用明胶、药用明胶、照相明胶、工业明胶[12]。
明胶按照品质不同可以分为高档明胶、低档明胶、骨胶,其中高档明胶简称明胶,国外称为Gelatin,低档明胶和骨胶则称为Glue[12]。
1.4 明胶的改性
对胶原多肽链上的功能基团进行修饰可获得改性明胶,其改性方法分为物理改性、化学改性、共混改性。
1.4.1 物理改性
物理改性是通过改变明胶自身结构而改善其原有的某些性能,该过程不需任何添加剂,通过γ射线、紫外线照射的光化学交联和热交联等方法实现[14]。
紫外线照射可使明胶结构中的芳香族氨基酸残基(如酪氨酸、苯丙氨酸)产生自由基,历经自由基引发,发生交联。虽光化学交联明胶能改善其凝胶强度等性质,但辐照后明胶的结构易被破坏,也不能有效改善明胶的热稳定性[14]。
1.4.2 化学改性
化学改性是明胶链中的功能基团与小分子化合反应或对其侧基修饰,或利用自由基、离子与其发生加成或开环聚合反应,对明胶进行接枝制得改性明胶[14]。
在化学改性中交联改性是通过化学试剂与明胶链上(明胶链端部和侧链)的活性基团反应生成新的化学键而实现的明胶改性[14]。以共价键与明胶链中赖氨酸的 ε-氨基反应形成 Schiff 碱结构的醛类是常用的交联剂。但从医药、食品安全方面考虑则更倾向于应用天然生物交联剂,如京尼平、天然酚类、天然多糖等。所含有羧基、羟基,可直接或经氧化后与明胶链中的活性基团反应而实现明胶的改性[14]。
侧链修饰是基于明胶侧链所含有的多种活性基团,如氨基、羧基、巯基、羟
基、胍基等,同小分子试剂反应。如己酰基(Hx)氯化物通过与碱性明胶(AlGltn)侧链上的游离氨基反应,得到利于创伤修复的己酰基改性明胶(HxAlGltn)[16]。
接枝共聚改性的基础是明胶链上的多种活性基团,利用自由基、离子与明胶链上的活性基团发生加成或开环聚合反应,对明胶进行接枝制得改性明胶[14]。如利用天然高分子材料阿魏酸同明胶相互作用可使明胶性能得以改善且无细胞毒性。
1.4.3 共混改性
共混改性是与明胶不发生反应的天然或合成高分子化合物和明胶混合组成复合物。Lin 等得到的聚(氨基酸酯)膦腈与明胶共混纳米纤维可提高聚(氨基酸酯)膦腈/明胶纳米纤维在水中的稳定性,改善纯聚[(丙氨酸乙酯)0.67(甘氨酰乙酯) 0.33] 膦腈纳米纤维的亲水性[17]。
1.4.4 复合改性法
复合改性法包括物理改性、化学改性、共混改性联合以及增塑剂、乳化剂、共混或化学改性联合两种。以明胶与壳聚糖共混为例,王丽媛等将明胶与壳聚糖共混并向其中加入乳化剂吐温-80,利用适量吐温-80阻碍水分子的渗透,降低水蒸气透过率,同时增强膜的机械性能[18]。
2 明胶的应用
2.1 明胶在食品中的应用
2.1.1 果糖添加剂
据报道,全世界的明胶有60%以上用于食品糖果工业[13]。溶于水后的明胶微粒所形成的网状结构为糖和水提供充塞的空隙。其随温度下降而凝聚,使柔软的糖果能保持稳定形态。明胶在糖果中的一般加量为5%-10%。在晶花软糖中明胶用量6%时效果最好。在橡皮糖中明胶的加量为6.7%。在牛轧糖中为0.6%-3%或更多些。在糖果粘液的浓糖浆中加量为1.5%-9%,糖味锭剂或枣子糖果的配料要求含明胶2%-7%[13]。
2.1.2 冷冻食品改良剂
基于明胶胶冻的熔点较低,其可作冷冻食品的胶冻剂,常用于制作餐用胶冻、粮食胶冻等。明胶还可用于制作果冻,作为稳定剂可用于冰淇淋、雪糕等的生产,
明胶在冰淇淋中可防止形成粗粒的冰晶,保持组织细腻和降低溶化速度,其在冰淇淋中的一般用量为0.25%-0.6%[13],胶冻强度的明胶需同浓度相匹配。
2.1.3 肉制品改良剂
明胶作为胶冻剂添加到肉制品中,用于香野猪肉、肉冻、罐头火腿、小牛肉、火腿馅饼、罐头肉类等制品的生产,可提高产品的产量和质量[13]。此外,明胶具有对肉制品的乳化剂、罐头产品的增稠剂作用。
2.1.4 饮料澄清剂
明胶可作为澄清剂用于啤酒、果酒、露酒、果汁、黄酒、巴旦木果仁乳饮料等产品的生产。其作用机理是明胶能与丹宁生成絮状沉淀,静置后,呈絮状的胶体微粒可与浑浊物吸附、凝聚、成块而共沉,再经过滤去除。如,在果汁饮料中明胶加量为2%-3%,在澄清杨梅果汁时用的是含明胶1%的水溶液,在啤酒澄清中所用的是含明胶0.5%的水溶液,在澄清葡萄酒中明胶用量为0.1-0.3g/L[13]。
2.1.5 食品涂层材料
在食品表面涂覆明胶具有以下优点[13]:(1)涂覆明胶能有效抑制褐变反应。(2)在粉末状、颗粒状糖类的表面涂覆食用明胶,能防止糖类吸潮,避免结块现象。(3)可使食品表面有光泽,提高食品质量。(4)防止食品腐败氧化。(5)明胶作稳定剂可防止产品干缩变形。(6) 在浸泡果蔬的糖液中添加明胶溶液可起到保鲜作用。
2.2 明胶在医药中的应用
2.2.1 囊材
明胶因其生物可降解性、良好的生物相容性和成膜性而在医药领域中广泛应用,其中明胶作为胶囊剂(硬胶囊、软胶囊、微胶囊)囊材(图3)的应用则最为广泛且历史悠久。
硬胶囊是以空心胶囊的形式供应的,用于装填粉剂或微粒等固体药物,具备“肠溶”特性,可采用交联剂硬化法、原料混合物法等方法生产。软胶囊主要用于包裹液体药物及物料或加有赋形剂而呈可流动状态的固体药物[1],一般采用转模法制备。明胶中掺入多肽生产软胶囊有利于提高药物的生理适应性(入口1-2min即溶化)。微胶囊可制成多种药物剂型,如散剂、胶囊剂等,在医药方面具有控制或延缓药物的释放、可使药物作用于指定部位、提高药物稳定性、延长药物贮藏期、掩蔽药物的苦味和臭味等作用。
但也存在交联导致胶囊溶出的减缓、不便于素食主义者、存在易传播传染性海绵组织脑科疾病隐患、存在药物迁移的现象等不足,需寻找改性明胶或明胶替代品来改善明胶胶囊的缺陷。



图3[2] 明胶胶囊:(左)硬胶囊;(中)软胶囊;(右)显微镜下微胶囊
2.2.2 血浆扩容剂
明胶作为生物来源的多肽,具有良好的生物相容性。其经改性后凝固点降低,可作为血浆替代品应用于临床,主要用于手术创伤、低血容量性休克等的血容量补充。聚明胶肽已被世界卫生组织(WHO)列为基本药物。目前,国内应用较多的血浆扩容剂产品有聚明胶肽注射液和琥珀酰明胶注射液。前者是六亚甲基二异氰酸酯通过脲桥键交联的脲联明胶注射液;后者是以琥珀酸酐为交联剂,交联改性的琥珀酰明胶注射液[14]。
明胶作为血浆替代品的使用量占全球血浆扩容剂(白蛋白、葡聚糖、羟乙基淀粉等)的25%[14],但明胶在临床应用中会产生急性肾损伤的发病率增加、凝血因子Ⅷ、Ⅰ和血管性血友病因子减少、血小板数量下降、诱导纤维蛋白聚合紊乱、引起严重的过敏反应等毒副作用。
2.2.3 组织工程和药物递送
明胶因其具有较高的生物相容性、生物可降解性且体内降解后不产生其他副产物、无免疫原性和血液相容性以及具有与胶原相同的组分和生物性质,广泛应用于组织工程和药物递送系统中[14]。对于骨组织,Rajzer 等[15]综合聚己内酯(PCL)和磷酸钙修饰后的明胶的矿化作用所得的磷酸钙修饰的明胶/PCL支架(Gel/SG5/PCL)能有效弥补明胶在体内降解速度快、机械性能差等问题。
此外,明胶及改性明胶纳米系统可广泛应用于抗癌药物、蛋白和疫苗、基因药物的递送[13],解决传统阳离子载体的细胞毒性及免疫原性等问题。
2.2.4 其他
明胶可作为海绵基材,发挥止血作用,应用于外科手术和拔牙和疾病的辅助诊断,如明胶修饰的金纳米粒[14],还可用于辅助膀胱癌的非侵入性诊断。
2.3 明胶的其他应用
除在食品和医药领域外,明胶还有许多其他用途:
(1)可作为铸涂纸的胶粘剂;在造纸工业中,单用明胶或明胶、淀粉混合物均可应用于全木浆纸或破布、木浆纸作为施胶物料,提高胶合效果[1]。(2) 可逆转换胶体可应用于生产膜、织物、涂层、胶囊方面[13]。(3)明胶具有发泡性,因此它可以应用在防火剂、庄稼保护覆盖物、涂层衬底、抑制灰尘扩散材料及应用在制备吸收噪音的泡沫水泥化合物、热绝缘体和防火材料[13]。(4)在感光工业上,可利用明胶制成了含有卤化银感光微粒的喷墨印刷接受层,该材料允许将感光材料刚刚冲洗后就进行喷墨印刷,并且温度大时具有良好的墨水亲和性[13]。(5)在日化工业中,明胶、胶原的水解物与维生素类物质配合使用,可制成营养、护肤美容、抗皱等化妆品,如胶原水解物与维生素E配合使用制成搞皱美容霜[1]。
3 指标及检测方法
依据《GB 6783—2013 食品添加剂 明胶》标准,对明胶作为食品添加剂有以下规范。
3.1 明胶作为食品添加剂相关要求
3.1.1 原料要求
可使用的原料包括:屠宰场、肉联厂、罐头厂、菜市场等提供的经检疫合格的新鲜牛、猪、羊和鱼等动物的皮、骨、筋、腱和鳞等;制革鞣制工艺前,剪切下的带毛边皮或剖下的内层皮;骨粒加工厂加工的清洁骨粒和自然风干的骨料。
禁止使用的原料包括:制革厂鞣制后的任何废料;无检验检疫合格证明的牛、猪、羊或鱼等动物的皮、骨、筋、腱和鳞等;经有害物处理过或使用苯等有机溶剂进行脱脂的动物的皮、骨、筋、腱和鳞等。
3.1.2 感官要求
表1[19] 感官要求
项目 |
要求 |
检验方法 |
色泽 |
淡黄色至黄色 |
取适量样品置于洁净透明的玻璃器皿中,在自然
光线下,观察其色泽和状态 |
状态 |
固体状(如颗粒、片状、粉末等) |
气味 |
无不适气味 |
配制明胶溶液(2.5 %),嗅其味 |

图4[2] 淡黄色的明胶
3.1.3 理化指标
表2[19] 理化指标
项目 | 指标要求 | 检验方法 |
水分,w/% ≤ | 14.0 | GB 5009.3 直接干燥法a |
凝冻强度(6.67%)/(Bloom g)≥ | 50 | GB 6783-2013附录A中A.4 |
灰分,w/% ≤ | 2.0 | GB 5009.4b |
透射比/% 波长450 /nm ≥ | 30 | GB 6783-2013附录A中 A.5 |
透射比/% 波长620 /nm ≥ | 50 | GB 6783-2013附录A中 A.5 |
水不溶物,w/% ≤ | 0.2 | GB 6783-2013附录A中 A.6 |
二氧化硫/(mg/kg) ≤ | 30 | GB 6783-2013附录A中 A.7 |
过氧化物/(mg/kg) ≤ | 10 | GB 6783-2013附录A中 A.8 |
总砷(As)/(mg/kg) ≤ | 1.0 | GB/T 5009.11 |
铬(Cr)/(mg/kg) ≤ | 2.0 | GB/T 5009.123 原子吸收石墨炉法c或GB 6783-2013附录A中 A.9 |
铅(Pb)/(mg/kg) ≤ | 1.5 | GB 5009.12 石墨炉原子吸收光谱法 |
a 称样量为1.0 g,精确至0.001 g,干燥温度为105 ℃±2 ℃。
b 称样量为1 g±0.1 g,精确至0.001g。
c 为仲裁法。 |
3.1.4 微生物指标
表3[19] 微生物指标
项目 | 指标要求 | 检验方法 |
菌落总数/(CFU/g) ≤ | 1000 | GB 4789.2 |
沙门氏菌 | 不得检出 | GB 4789.4 |
大肠菌群/ (MPN/g) ≤ | 3 | GB 4789.3 MPN 计数法 |
3.2检验
对作为食品添加剂的明胶检验包括鉴别试验、凝冻强度的测定、透射比的测定、水不溶物的测定、二氧化硫的测定、过氧化物的测定、铬(Cr)的测定。以下基于明胶中SO2含量测定方法进行简要介绍。
SO2测定是基于明胶中亚硫酸盐转变成硫酸后,通过标准碱滴定所消耗的碱量计算出SO2含量。包括以下试剂与材料:过氧化氢溶液:3%;溴酚蓝乙醇溶液:1g/L;氢氧化钠标准滴定溶液:c(NaOH) = 0.01 mol/L;盐酸溶液:2 mol/L[19]。
以图5所示装置实验,需进行样品和空白滴定,具体步骤详见GB 6783-2013。实验所得SO2含量按式2计算:
式2
其中,64.060:SO2的摩尔质量的数值,(g/mol)[M(SO 2 )=64.060]; 0.5:
换算系数;消耗氢氧化钠标准滴定溶液的体积(mL);:空白消耗氢氧化钠标准滴定溶液的体积(mL);c:氢氧化钠标准滴定溶液的浓度(mol/L);m:试样的质量(g)。计算结果取整数。取平行测定结果的算术平均值为测定结果。在重复性条件下获得的两次独立测定结果的绝对差值应不超过1 mg/kg[19]。
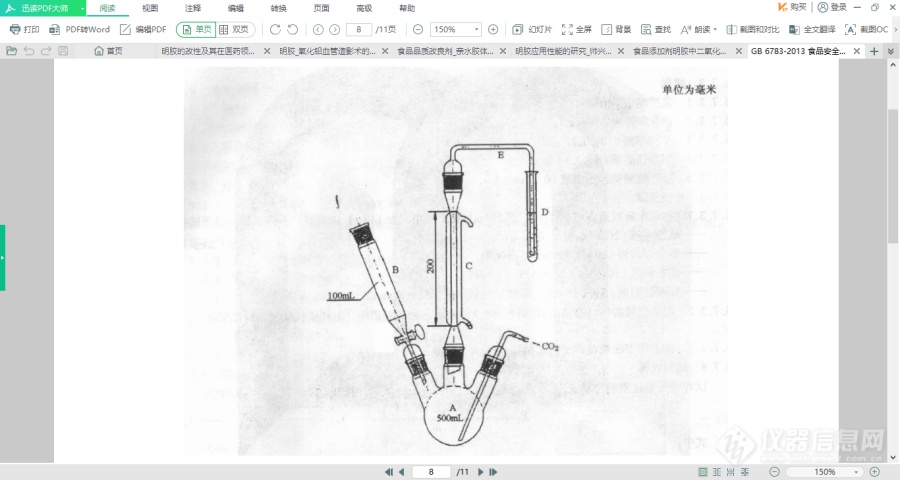
图5[19] 二氧化硫测定装置
4 总结
食品添加剂安全直接关系公众身体健康、关系食品工业健康发展,是食品安全的重要内容之一。国家质量监督检验检疫总局局长支树平曾道:“严厉打击非法添加和滥用食品添加剂专项工作,是党中央国务院的重大决策和号令,是广大人民群众关注的热点和热切期盼,也是质检部门的神圣职责。”明胶是众多食品添加剂之一,相关行业按规范正确使用明胶,是对消费者和自身食品安全的负责。此外,明胶作为用途广泛的生物化工原料,年需求量约1.72万t[1]。其不仅在食品上,现在乃至未来的应用范围仍不断拓宽,具有广阔的市场前景。
参考文献
[1] 缪进康. 明胶及其在科技领域中的利用[J]. 明胶科学与技术, 2009, 29(1):28-51.
[2] 来自百度图片.
[3] Pouradier J, Venet A M. Contribution a l’etude de la structure des geletines II Variation des proprietes physiques et mecaniques avec la mass moleculaire [J]. J.Chim. Phys, 1950, 47: 391-398.
[4] 王前. 明胶制备工艺及溯源方法研究[D]. 北京: 北京化工大学, 2009:12-15.
[5] 傅晓敏, 陈丽娟. 明胶分子量分布测定和表征的研究进展[J]. 明胶科学与技术, 1994, 14(003):113-118
[6] Ebihara T, Hattori S, Matsubara Y, et al. Use of pepsin-treated gelatin as a stabiliser for injectable trace protein substances [P]. EP110477, 2001: 196-200.
[7] Olmo T, Okawa Y, Horiuchi M, et al. 用水喷射法控制明胶的分子量分布和物理性能[J]. 明胶科学与技术, 2002, 22(3):127-134.
[8] 徐文达. 关于明胶的等离子点与等电点[J]. 明胶科学与技术, 1986, 6(1):31.
[9] 赵振厚. 明胶等电点及明胶的混配[J]. 明胶科学与技术, 2003, 23(2):72-73.
[10] 彭必先, 陈丽娟. 从胶原到明胶(第二部分)[J]. 明胶科学与技术, 1994, 14(2):57-65.
[11] 王卫平. 食品品质改良剂: 亲水胶体的性质及应用(之八)——蛋白质亲水胶体[J]. 1997, 23(4):81-84.
[12] 《明胶生产工艺以及设备》编写组. 明胶生产工艺以及设备[M]. 1996:5.
[13] 帅兴华, 王少强, 宋增峰, 等. 明胶应用性能的研究[J]. 皮革化工, 2007, 24(3):20-23.
[14] 张丹丹, 叶海, 平其能, 等. 明胶的改性及其在医药领域的应用[J]. 药学进展, 2017, 41(8):600-607.
[15] Rajzer I, Menaszek E, wiatkowski R K, et al. Electrospun gelatin/poly(ε-caprolactone) fibrous scaffold modified with calcium phosphate for bone tissue engineering[J]. Mater Sci Eng C Mater Biol Appl, 2014, 44: 183-190.
[16] Yoshizawa K, Mizuta R, Taguchi T. Enhanced angiogenesis of growth factor-free porous biodegradable adhesive made with hexanoyl group-modified gelatin[J]. Biomaterials, 2015, 63: 14-23.
[17] Lin Y J, Cai Q, Li L, et al. Co-electrospun composite nanofibers of blends of poly[(amino acid ester)phosphazene] and gelatin[J]. Polym Int, 2010, 59(5): 610-616.
[18] 王丽媛, 侯梦奇, 李晓, 等. 4种改性方式对明胶膜性能的影响[J]. 食品科学, 2015, 36(6): 40-44.
[19] 中华人民共和国国家卫生和计划生育委员会. GB 6783—2013 食品添加剂 明胶. 2013-11-29发布, 2014-06-01实施.









