推荐厂家
暂无
暂无


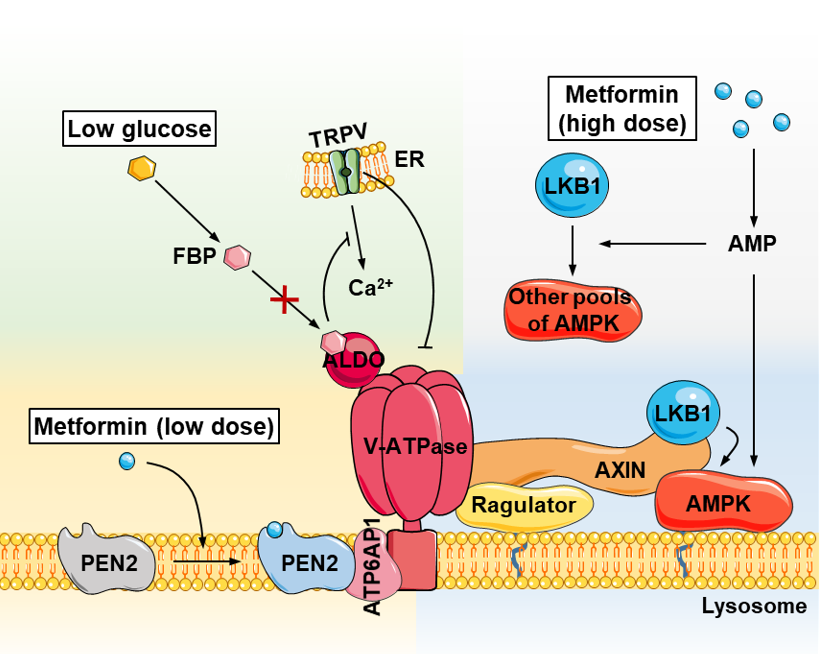


科技日报讯 据物理学家组织网8月13日(北京时间)报道,澳大利亚的研究人员确定一种名为白细胞介素-11的分子,在癌细胞的生长扩散中发挥着重要作用,能够成为抗癌疗法的新靶点。此前研究中,该分子的作用一直被忽视,而今这匹“黑马”极有可能为包括肠癌和胃癌在内的多种癌症带来全新的治疗途径。相关论文在线发表在《癌细胞》杂志网站上。 在肿瘤处于发展过程中时,病灶周围的正常组织会出现发炎状况,并产生许多不同的分子,其中就包括两种相关的蛋白质白细胞介素-11和白细胞介素-6。这些激素样信号分子被统称为细胞因子,被认为是促进癌细胞生长和扩散的重要物质。但前者一直被认为在其中仅起到很小的作用。 然而,澳大利亚沃尔特伊丽莎医学研究所的研究人员特蕾西·帕博斯凯和马提亚斯·恩斯特发现,白细胞介素-11是促进癌细胞生长与扩散最重要的一个细胞因子。通过与澳大利亚墨尔本CSL制药公司的合作,他们发现阻断白细胞介素-11的信号能在胃癌和肠癌模型中使肿瘤停止生长,并使肿瘤收缩。这有望为肠癌和胃癌的治疗带来一种新途径,而这两种癌症也是全球最常见的两种癌症。 帕博斯凯表示:“在考虑促进癌细胞生长发育的细胞因子时,人们往往首先想到白细胞介素-6,而与它非常相似的白细胞介素-11却被人忽视。此次新研究发现,后者实际上才是最主要的致癌因素。” 恩斯特副教授指出,通过阻断细胞因子信号来治疗癌症是一个令人兴奋的新疗法,与现有疗法相比具有许多潜在优势。而CSL制药公司同样看好白细胞介素-11相关药物的前景,其高级副总裁宣称,他们已经开发出一些针对白细胞介素-11受体的候选药物,将有望在胃癌和肠癌的治疗中发挥作用。(记者王小龙) 总编辑圈点 上世纪七十年代,人们曾经乐观地认为,二十年内就能发现癌症的疗法。大家后来才明白,癌细胞的复杂超出了当时的想象。多年研究后,的确也发现不少抑制肿瘤的办法。比如被寄予厚望的新招,就是阻断细胞因子作用,相当于逮捕肿瘤的信号兵。相关药物这几年用于治疗炎症和癌症,无明显副作用,比那些玉石俱焚的猛药更令人放心。目前对肿瘤尚无一针见效的绝招,但“零敲碎打”的效果也很显著了。 《科技日报》(2013-08-14 一版)
日前,南京医科大学朱东亚教授与其科技团队在美国《Nature Medicine》杂志发表了题为《阻断缺血诱导的nNOS与PSD95相互作用治疗脑缺血损伤》的论文,提出了一个治疗脑中风的新药物作用靶点,进而研究出了一种小分子药物。由于这种新药既能够起到有效的治疗作用,又避免了目前其他药物普遍存在的副作用过大的缺陷,《Nature Medicine》杂志社特邀该领域的科学家为此发表评论,称“小分子药物ZL-006的出现让我们看到了脑卒中等神经系统疾病治疗的新曙光”。 脑卒中,俗称脑中风,在我国的发病率高居所有病症的前三位,这种疾病发病率高且后遗症多(包括偏瘫、认知障碍等)。 如何才能找到一种疗效好又无副作用的抗脑卒中药物,是国际医学界多年来悬而未决的重要课题。 在多年研究的基础上,一次独辟蹊径的设想使朱东亚将研究的目光从抑制靶标本身移向了“下游”——细胞内蛋白与蛋白的相互作用。从蛋白间结合的角度进行抗脑卒中药物的研究非常困难,在世界范围也鲜有先例可循。 在仔细研究了两种蛋白的性质和结构的基础上,朱东亚设计了一百多种化合物,并最终筛选出了“ZL—006”——一种一端亲水另一端疏水的小分子化合物。通过动物及细胞实验验证,该化合物确实可以阻断两蛋白的结合,而且在若干种脑卒中模型中都显示了它的疗效,更为重要的是,实验已经证实这种药物不会影响认知、学习和记忆,也不会导致动物具有进攻性等行为异常,它不具有其他药物针对受体的副作用。(科技日报)Stroke is a major public health problem leading to high rates of death and disability in adults1, 2. Excessive stimulation of N-methyl-D-aspartate receptors (NMDARs) and the resulting neuronal nitric oxide synthase (nNOS) activation are crucial for neuronal injury after stroke insult3, 4, 5, 6, 7. However, directly inhibiting NMDARs or nNOS can cause severe side effects because they have key physiological functions in the CNS5, 8, 9, 10, 11, 12. Here we show that cerebral ischemia induces the interaction of nNOS with postsynaptic density protein-95 (PSD-95). Disrupting nNOS–PSD-95 interaction via overexpressing the N-terminal amino acid residues 1–133 of nNOS (nNOS-N1–133) prevented glutamate-induced excitotoxicity and cerebral ischemic damage. Given the mechanism of nNOS–PSD-95 interaction, we developed a series of compounds and discovered a small-molecular inhibitor of the nNOS-PSD-95 interaction, ZL006. This drug blocked the ischemia-induced nNOS–PSD-95 association selectively, had potent neuroprotective activity in vitro and ameliorated focal cerebral ischemic damage in mice and rats subjected to middle cerebral artery occlusion (MCAO) and reperfusion. Moreover, it readily crossed the blood-brain barrier, did not inhibit NMDAR function, catalytic activity of nNOS or spatial memory, and had no effect on aggressive behaviors. Thus, this new drug may serve as a treatment for stroke, perhaps without major side effects.
[align=center]靶向抗癌药物的研究进展[/align][align=center]摘 要[/align][align=center] [/align][align=left]恶性肿瘤是威胁人类健康的常见病和多发病,其病死率极高,死亡率占所有疾病死亡率的首位,引起了人们的普遍关注。传统意义上的抗癌药物在体内无一定的特异性分布,导致对肿瘤细胞起作用的药物剂量无法达到要求,在杀死或抑制肿瘤细胞的同时也损伤相当数量的正常细胞,从而产生严重的器质性病变。随着人体内各种通路及肿瘤实体生理机制的阐明,出现了一种通过将药物或者相关蛋白直接导向肿瘤细胞的新型抗癌药物,即靶向抗癌药物。这类药物的特异性强,疗效显著。本文主要就近年来靶向抗癌药物的研究进展进行了综述,并对靶向抗癌药物发展前景进行了预测和展望。[/align][align=left] [/align][align=left]关键词:靶向;抗癌药物;研究进展[/align][align=center] [/align][align=center] [b]Progressin the research of anticancer drugs targeting [/b][/align][align=center][b]ABSTRACT[/b][/align][align=center][b] [/b][/align]Malignant tumor is aserious threat to human health of the common and frequently occurring disease,its mortality is very high, mortality accounts for all disease mortality in thefirst place, caused the widespread attention of people. Anticancer drug in thetraditional sense of no specific distribution in the body, leading to drug doseeffect not to meet the requirements of the tumor cells, damage to normal cellsin a considerable number of kill or inhibit tumor cell at the same time,resulting in serious pathological changes. With the elucidation of variouspathways and tumor entity and physiological mechanism of the human body, theemergence of a new anticancer drug or by direct guidance related proteins intumor cells, namely targeting anticancer drugs. This drug is of good effect. Thispaper mainly in recent years targeted anticancer drugs research progress were narrated,and the target anticancer drug development prospect is forecasted andprospected.[b]Keywords[/b]: Targeting anticancer drug research progress[b]一 引言[/b][align=left] 在癌症的治疗中,传统化疗药物细胞毒的特异性差,在杀死或抑制肿瘤细胞的同时也损伤相当数量的正常细胞,直接影响心、肺、肝、肾以及神经系统等功能。严重者必须中断化疗,导致化疗失败[sup][/sup]。并且,药物分子不能有效到达预期靶标部位,造成药物在靶部位浓度不足。因此,研究者在癌症治疗中开始寻求具有较好靶向性并具有较高释放效率[sup][/sup]的体系,即靶向抗癌药物。靶向抗癌药是指针对在肿瘤发生发展过程中具有关键作用的特定靶标进行治疗的药物[sup][/sup],近年来这类药物被相继开发出来。例如,肿瘤新生血管生成抑制剂阿瓦斯丁等已经开始在临床应用;拓扑异构酶Ⅰ抑制剂及其同类物最近对其机理的研究也取得了新的进展;另外基于肿瘤信号转导机制的药物如蛋白激酶抑制剂等在肿瘤治疗中的研究也成为新的热点[sup][/sup]。[/align][b]二 肿瘤新生血管生成抑制剂[/b]任肿瘤细胞的生长与转移很大程度上依赖于新血管的生成。肿瘤会诱导其周围血管的快速生成,导致血管内皮细胞组织形态的改变,内皮细胞不断迁移、增殖,从而使新血管逐渐生成[sup][/sup]。开发和研究能够破坏或抑制血管生成、有效地抑制肿瘤生长和转移的药物,是新型抗肿瘤药物研究的活跃领域之一。与抑制肿瘤生长的传统治疗方式相比,靶向新生血管生成的治疗模式可能意味着更高的特异性,更低的毒性,以及有利于克服肿瘤的耐药性,而且还可广泛用于多种肿瘤转移的治疗。抗肿瘤新生血管药物的主要类型有:以血管内皮细胞生长因子为靶点的单克隆抗体,如贝伐单抗(阿瓦斯丁);以血管内皮细胞生长因子受体为靶点的多靶点小分子酪氨酸激酶抑制剂,如索拉非尼、舒尼替尼;作用于血管内皮细胞靶点的血管生成抑制剂,如重组人血管内皮抑制素(恩度)、沙利度胺(反应停)。以近几年来研究热门的蛋白酪氨激酶(PTK)抑制剂为例,对其作用机制和上市情况进行阐述。PTK是一组酶系,能催化ATP上的磷酸基转移到许多重要的蛋白质的酪氨酸残基上,使其残基磷酸化,从而激活各种底物酶,通过一系列反应影响细胞的生长、增殖和分化[sup][/sup]。多数肿瘤细胞PTK活性异常升高,因此PTK是一个非常重要和有价值的抗肿瘤靶点。2005-2010 年间,此类药物累计申报新化合物总量已经达到 27 个,占所有类别抗肿瘤新药的50%[sup][/sup]。这些药物大多数为me-too药,如盐酸埃克替尼,该产品是在2004年获得 FDA批准上市的厄洛替尼基础上进行结构改造得到,是一种表皮生长因子受体( EGFR) 酪氨酸激酶抑制剂,针对同样靶点的上市产品还有吉非替尼[sup][/sup]。[b]三 微管蛋白抑制剂[/b]一直以来,肿瘤细胞的微管都被视为抗肿瘤药物的良好靶点,微管蛋白抑制剂被作为最有效的抗肿瘤临床一线药物。许多化合物都能干扰微管蛋白的功能,主要是与微管作用以抑制其聚合,使细胞分裂停止于有丝分裂的中期或者促进微管聚合,抑制微管解聚进而影响细胞分裂[sup][/sup]。较为经典的如长春碱类和鬼臼霉素类可与微管蛋白结合,阻滞微管蛋白聚合成微管,影响微管蛋白稳定性,干扰纺锤体的形成,阻滞有丝分裂的进行,使细胞分裂停滞在中期[sup][/sup]。近年来,细胞微管相关的抗肿瘤药物在原有基础上得到了进一步的发展,长春花生物碱类长春氟宁、多拉司他汀、罗米地新、艾立布林等药物已经相继进入二到三期临床试验,有的甚被作为某些肿瘤的二三线临床用药[sup][/sup]。这些药物在原有基础上增加了药物作用的特异性,并在一定程度上减少了不良反应。相信在不久的将来,以细胞微管为靶点的抗癌药物能为我们带来更多的惊喜,成为临床上更有效的抗癌药物。[b]四 叶酸介导的抗肿瘤药物[/b][align=left]在叶酸是核酸生物合成的代谢物,叶酸缺乏时白细胞减少,因此叶酸拮抗物可用于治疗急性白血病。某些以二氢叶酸还原酶为靶点的叶酸拮抗剂可以不可逆的抑制二氢叶酸还原酶的活性。这样通过抑制二氢叶酸还原酶,从而抑制DNA和RNA的合成,阻碍肿瘤细胞的生长[sup][/sup]。此类药物如甲氨喋呤,临床用于急性白血病和绒毛膜上皮癌,常与亚叶酸钙合用降低毒性[sup][/sup]。[/align][align=left]此外,叶酸受体在大部分人体肿瘤细胞表面过度表达,而在正常细胞表面则很少表达,甚至不表达。这就使得利用叶酸介导的抗肿瘤药物靶向作用于叶酸呈阳性的肿瘤细胞成为可能,从而减少传统抗癌药物对正常细胞的毒副作用。此类药物如EC0225,Endocyte 公司于2007 年 3 月开始对其进行Ⅰ期临床试验用于治疗顽固性或病灶转移性肿瘤[sup][/sup]。[/align][b]五 DNA拓扑异构酶抑制剂[/b] DNA 的不间断复制是肿瘤细胞不断增生的关键所在。如果有效的抑制DNA 引物酶,阻断引物的合成,DNA制将会受到限制,肿瘤细胞将不再增生,进而抑制了肿瘤的生长[sup][/sup]。DNA引物酶作为理想靶点为抗肿瘤药物的研究提供了线索,当前抑制DNA复制主要以 DNA拓扑异构酶为靶点展开的。作为一种独特酶,DNA拓扑异构酶存在于真核生物和原核生物细胞中,用以调节DNA空间构型动态变化,参与DNA的不断复制、翻译、重组和修复等过程,在形成染色体结构及染色体分离与浓缩方面起到了主导作用[sup][/sup]。[b]六 端粒酶抑制剂[/b]在基因端粒酶是一种RNA 聚合酶,能以本身RNA 为模板,在染色体末端合成六聚脱氧核苷酸TrAGGG 的重复序列,以补偿细胞分裂时的染色体末端缩短,解决“末端复制问题”[sup][/sup]。正常人体细胞的端粒酶活性较低,但大多数的肿瘤细胞的端粒酶活性显著升高。因此,检验端粒酶活性是癌诊断的重要方法,是抗癌药物需要研究的靶点之一。端粒酶在肿瘤细胞被过度表达,它是肿瘤细胞增殖所必需的。抑制端粒酶的活性,肿瘤细胞进入静止状态,最后产生细胞凋亡。端粒酶抑制剂是一类潜在的高选择性的抗肿瘤药物,在恶性肿瘤的基因治疗中有重要作用。已发现的端粒酶抑制剂有AZT、AZGT及其衍生物、异噻唑啉衍生物TMPI、类黄连素、小的非核苷合成复合物BIBR等。[align=center]七 总结与展望[/align][align=left]近年来,抗癌药物的研究已从利用和改进毒性较大的传统抗癌药物发展向靶向药物设计和研发转变。随着科学技术的发展和对肿瘤发病机制认识的深入,临床抗癌药物的靶向性越来越集中。靶向抗癌药物已凭其特异性、针对性和有效性较强,患者耐受性较好而毒副反应相对于细胞毒药物较低等特点,在肿瘤治疗中取得很大成功。与此同时,靶向抗癌药物研发中仍存在很多需要解决的科学与技术问题。例如:单一靶点的小分子类药物治疗范围窄,且易产生耐药性;即使是使用抗肿瘤靶向药物治疗非常成功的适应证,由于肿瘤细胞具有高度变异的性质,患者的肿瘤仍可能在初始治疗成功后复发;有些肿瘤靶点精确性不够,它们也存在于某些正常细胞,所以会导致相应毒性;多数靶向抗癌药物不良反应多等。[/align][align=left]这些问题都有待于解决。并且,要清醒的认识到靶向抗肿瘤药物开发近几年呈现爆炸式增长,可以想象在未来 5-10年市场将相当拥挤,此类药物的开发立项中需要趋于冷静和理性,需要药企和研究者之间的合作,探索更具有创新性思维的临床研究模式。[/align][align=left]无论如何,根据特定导向的靶点的需要来设计制备疗效确切的抗癌药物,将是靶向抗癌药物的发展方向,靶向抗癌药物必将随着其疗效最优化的进步而在各类肿瘤中得到更广泛的应用。在靶点治疗理念的指导下,在合理的研究设计、全面的临床前评价和严谨合理的临床试验的基础上,抗肿瘤药物新靶点研究前景变得更加广阔,也能开发出更多新靶点特异性抗肿瘤新药。[/align][align=left]另一方面,根据患者的基因和蛋白资料实施给药方案,并“量体裁衣”式地对患者合理用药,以提高药物的疗效,降低药物的毒副反应,同时减轻患者的痛苦和经济负担,利用基因导向个体化用药;能否通过对靶位基因的筛查达到早期诊断并提示预后,甚至可以通过干预这些基因的异常表达达到治疗的目的。个人认为,这将是我们努力的方向。[/align][b]参考文献[/b] EavanG1 Prolififeration,elleyeleandaPotosisineaneer.Nature,2004,411(6835):342~348. Cho K J,Wang X,Nie S M. Clin.CancerRes.,2008,14: 1310—1316 Sawyers C. Targeted cancer therapy .Nature, 2004,432(7015): 294-297 梁岩,何珩,孙翠萍.抗肿瘤用药的应用及进展.中国医疗前沿,2009,4(21):17~18 林健,卜一珊.分子抗癌靶向药物的研究进展.天津药学,2005,17(12):61~62 郑晓克.抗肿瘤药物的研究进展.中山大学研究生学刊,2008,4(29):7~12 DuffaudF, Blay JY. Gastrointestinal stromal tumors and ncatmcnl . Oncology, 2003,65 (3):187-197 陈晓媛,张虹,高晨燕.小分子靶向抗肿瘤药物临床研究策略探讨及案例分析.新药申报与审评技术,2013,22(3):269~273 孙西洋,任常山,曹心珂.抗肿瘤药物的靶向给药系统研究进展.中国医药生物技术,2008,3(6):461~464 Ng SS,Figg WD T.antiangiogenesisin vitroinfluence of formulation vehicles and binding proteins.Cancer Res,2004,64(3):821-824 Bellmunt J,ThéodoreC,Demkov T.Phase III trial of plus best supportive care compared with alone after aplatinum-containing regimen in patients with advanced transitional cellcarcinoma of the tract.Clin Oncol,2009,27(27):4454-4461 王祎,刘燕,丁秀云.抗肿瘤药物的研究进展.包头医学,2012,36(3):129~132 曹胜利,郭燕文,王先波.抗叶酸剂类抗肿瘤药物的研究进展.中国新药杂志,2007,16(10):747~753 梁旭华,孙洋,谭春雷.叶酸受体介导的抗肿瘤靶向前药研究进展.中国新药杂志,2012,21(22):2647~2653 卿晨.恶性肿瘤化疗耐药及克服耐药的研究.昆明医科大学学报,2013,34(1):1~3 王丽鸿.分子靶向抗癌药物的研究进展.牡丹江医学院学报,2013,34(2):81~82 李嘉,包春波.抗肿瘤化学药物研究进展.华西药学杂志,2009,4(21):1~5

 400-860-5168转6007
400-860-5168转6007
 留言咨询
留言咨询

 400-860-5168转4529
400-860-5168转4529
 留言咨询
留言咨询

 400-860-5168转1372
400-860-5168转1372
 留言咨询
留言咨询


