推荐厂家
暂无
暂无
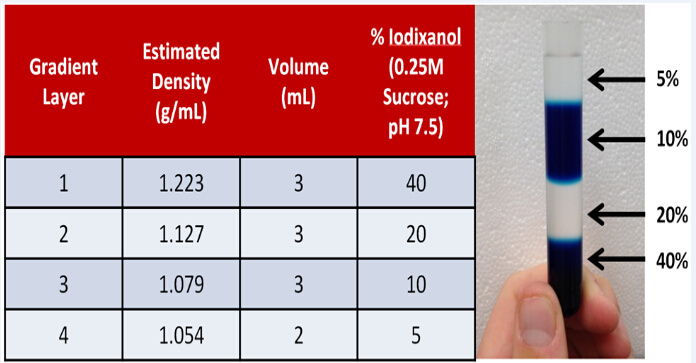




[color=#231815]生物活性蛋白质分离纯化技术研究进展[/color][color=#231815][color=#333333]生物体是天然活性蛋白质的宝库,近年来,越来越多具有生物活性的蛋白质被发现和研究,在生物制药、营养食品等方面具有广阔的应用前景。然而,分离纯化的技术与策略将影响天然蛋白的活性与功能,以及相关的经济效益。基于目前研究现状,对生物活性蛋白质的分离纯化技术进行了综述。 [/color][/color]
从混杂微生物群体中获得只含有某一种或某一株微生物的过程称为微生物分离与纯化。在分子生物学的研究及应用中,不仅需要通过分离纯化技术从混杂的天然微生物群中分离出特定的微生物,而且还必须随时注意保持微生物纯培养物的“纯洁”,防止其他微生物的混入。 1、用固体培养基分离和纯化 单个微生物在适宜的固体培养基表面或内部生长、繁殖到一定程度可以形成肉眼可见的、有一定形态结构的子细胞生长群体,称为菌落。当固体培养基表面众多菌落连成一片时,便成为菌苔。不同微生物在特定培养基上生长形成的菌落或菌苔一般都具有稳定的特征,可以成为对该微生物进行分类、鉴定的重要依据。大多数细菌、酵母菌、以及许多真菌和单细胞藻类能在固体培养基上形成孤立的菌落,采用适宜的平板分离法很容易得到纯培养。所谓平板,即培养平板的简称,它是指固体培养基倒入无菌平皿,冷却凝固后,盛固体培养基的平皿。这方法包括将单个微生物分离和固定在固体培养基表面或里面。固体培养基用琼脂或其它凝胶物质固化的培养基,每个孤立的活微生物体生长、繁殖形成菌落,形成的菌落便于移植。最常用的分离、培养微生物的固体培养基是琼脂固体培养基平板。这种由Kock建立的采用平板分离微生物纯培养的技术简便易行,100多年来一直是各种菌种分离的最常用手段。 1.1 稀释倒平板法 首先把微生物悬液作一系列的稀释(如1:10、1:100、1:1000、1:10000),然后分别取不同稀释液少许,与已熔化并冷却至50℃左右的琼脂培养基混合,摇匀后,倾入灭过菌的培养皿中,待琼脂凝固后,制成可能含菌的琼脂平板,保温培养一定时间即可出现菌落。如果稀释得当,在平板表面或琼脂培养基中就可出现分散的单个菌落,这个菌落可能就是由一个细菌细胞繁殖形成的。随后挑取该单个菌落,或重复以上操作数次,便可得到纯培养。 1.2 涂布平板法 因为将微生物悬液先加到较烫的培养基中再倒平板易造成某些热敏感菌的死亡,且采用稀释倒平板法也会使一些严格好氧菌因被固定在琼脂中间缺乏氧气而影响其生长,因此在微生物学研究中常用的纯种分离方法是涂布平板法。其做法是先将已熔化的培养基倒入无菌平皿,制成无菌平板,冷却凝固后,将一定量的微生物悬液滴加在平板表面,再用无菌玻璃涂棒将菌液均匀分散至整个平板表面,经培养后挑取单个菌落。 1.3 平板划线法 最简单的分离微生物的方法是平板划线法,即用接种环以无菌操作沾取少许待分离的材料,在无菌平板表面进行连续划线(图2),微生物细胞数量将随着划线次数的增加而减少,并逐步分散开来,如果划线适宜的话,微生物能一一分散,经培养后,可在平板表面得到单菌落。有时这种单菌落并非都由单个细胞繁殖而来的,故必须反复分离多次才可得到纯种。其原理是将微生物样品在固体培养基表面多次作“由点到线”稀释而达到分离目的的。划线的方法很多,常见的比较容易出现单个菌落的划线方法有斜线法、曲线法、方格法、放射法、四格法等。
[I][B][color=#DC143C][size=4][font=新宋体]生物制药设备和分离纯化技术,一本从事制药行业的好书![/font][/size][/color][/B][/I][em0807][img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=81109]生物制药设备和分离纯化技术[/url]
 400-876-8980
400-876-8980
 留言咨询
留言咨询

 400-876-8980
400-876-8980
 留言咨询
留言咨询

 400-831-3689
400-831-3689
 留言咨询
留言咨询