

面对面想你
第1楼2009/03/20
1.1 NOx 光催化氧化
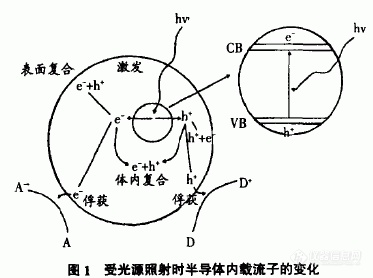
光催化材料的电子和空穴被光激 发后, 空穴本身具有很强的得电子能力, 可夺取 NOx 体系中 的电子, 使其被活化而氧化。电子与水及空气中的氧反应生 成氧化能力更强的?OH 及 O2-?等, 这是将 NOx 最终氧化生 成 NO3-的最主要的氧化剂。氧化 NOx 生成的 NO3-会残留在 催化剂的表面, 当累积到一定浓度时会使催化剂活性降低, 所以需要水的洗净、再生。而通过催化剂流出的水几乎是没 有酸性的, 完全可以被空气中的粉尘中和而无害化[5]。
1.2 NOx 光催化还原
光催化还原反应是使 NOx 在光催 化剂的作用下直接分解生成完全无害的 N2。以 TiO2 为催化 剂的反应条件比较特殊, 一般需要加入还原剂, 如将需要加 入 NH3 才可将 NO 降解为 N2O 和 N2[6], 加入甲醇可将 N2O 降 解为 N2[7]; 有些反应还需要在低温下进行[8]。因此, 在该文中 除该小节外, 涉及到以 TiO2 为光催化剂转化 NOx, 均指光催化氧化( 特殊指明除外) 。 另外, 特定的光催化剂也可将 NOx 还原。用光沉积法在 TiO2 上附载 Ag+, 可将 N2O 降解为 N2 [7]。 Michael A 等以存 在 表 面 氧 空 穴 的 TiO2 为 催 化 剂 将 N2O 还 原 为 N2[8]。 Shicheng Zhang 等用浸渍法在 ZSM!5 沸石表面附载微量 TiO2, 以其作为光催化剂, 在室温下可将 NO 还原[9]。此外, 在 一些非 TiO2 催化剂( 如植入金属离子的沸石[10-13)] 的光催化 作用下, 可在常温下将 NOx 还原为 N2。
与光催化氧化 NOx 相比, 光催化还原反应具有不产生 NO3-、不需要水的洗净及再生等优点。其主要存在问题是在 还原过程中, 如控制不当, 除生成 N2 外, 还会生成诸如 CO[7]、 N2O[9]之类的有害副产物。如果是用 NH3 作还原剂, 仍存在 腐蚀、堵塞设备和运输储存的安全性等问题[6]。
2 光催化反应器
2.1 固定床光催化反应器 目前有不少研究者采用在这 种固定床反应器进行气相污染物( 主要是室内空气) 的光催 化转化研究。他们将 TiO2 附着在光纤网( 反应器见图 2) [14]、 活性炭滤网( 反应器见图 3) [15]、玻璃板[16]等上或加入聚合物 制成薄板[17], 将其置于反应器内, 而灯光则从反应器中央[14] 或上面[15]照射。还有学者直接将光催化剂涂在管式反应器的 内壁, 将光源置于管中央, 也达到了满意的 NOx脱除的效果[18]。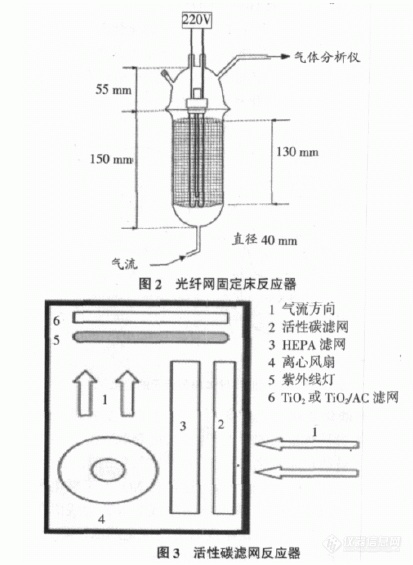
面对面想你
第2楼2009/03/20
还有一些学者将 TiO2 制成薄膜或涂料, 使其附着在建 筑物表面[19], 或者利用公路的路面[20]或墙体[21]作为催化剂载 体来转化大气中 NOx。这些实验虽然在实验室内对 NOx 的 转化达到了不错的效果, 但由于实际环境和实验室有很大 差别, 其结果能否运用于实际, 还是一个未知数。 由于固定床反应器构造相对比较简单, 所以其操作简 单, 成本低, 但其简单的构造也造成了其气固两相的接触和 光照效率不高的缺点。
2.2 流化床光催化反应器
为了提高气固两相的接触和 光照效率, 使用流化床技术以提高对大量气体污染物的处 理效率也正受到人们的关注。目前研究者已经制成了很多高 效的流化床反应器[22-25], 如 Matsuda S, Hatano H 等制成了可 大量处理含 NOx 的气体( 如烟道气) 流化床反应器( 图 4) [22], 他们用双管系统作流化床, 将光源置于内管, 以溶胶- 凝胶 法在硅胶粉表面涂渍 TiO2 制得颗粒状的催化剂, 并将其置 于内外管间的环型区域, 制成了具有较好 NOx 转化效果的 流化床反应器。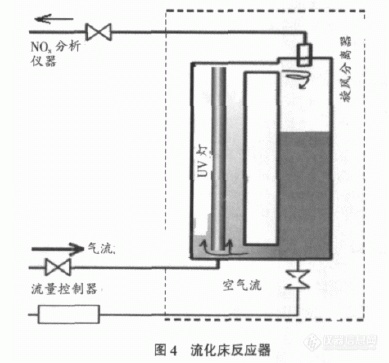
流化床反应器的优点是宜于催化剂的装载和卸载, 可 以连续进行 NOx 的处理; 通过加热可以除去硝酸, 使催化剂 再生; 流化床中催化剂的剧烈运动会提高整个床层的传质 效率; 由于催化剂的运动, 催化剂的受光表面也会增强, 因 而光催化效率也得以增强[24]。另外, 较低的 NOx 初始浓度, 较长的停留时间, 合理的气速和空隙率[25], 合适的催化剂粒 径[24], 均可提高流化床反应器的光催化效率。
由于构造相对复杂, 流化床反应器的操作比较复杂, 此 外, 催化剂从反应混合物中分离出来也比较困难。
3 TiO2 性能的改进
设计合适的反应器能够很好地促进光催化反应, 催化 剂的性能也对光催化转化 NOx 反应起重要的作用。目前, 不 少学者在研究催化剂性能的改进。
3.1 利用可见光 TiO2 作为光催化剂的缺点是光吸收波 长范围狭窄。TiO2 是带隙能为 3.2 eV 的半导体氧化物, 相当 于小于 380 nm 波长的光照射才能激活, 这个波长的光在紫 外光区, 只占太阳光能的 4 %左右, 而太阳光能的 45 %在可 见光区, 因此如何利用可见光成为最近研究的热点。
为了能充分利用可见光, 研究人员对 TiO2 进行了改性 研究。Isao Nakamura 等将 TiO2 置于 H2 含量为 2 托的石英 容器内, 在 673 K 的温度下以频率为 13.56 MHz 的短波照 射10 ̄60min, 发现经此方法处理的 TiO2 可吸收 600nm 可见 光而转化 NO, 并且其在紫外光下的光催化性能没有改变[26]; 此 外, 在 TiO2 中掺杂 N 元素, 也可使其在可见光谱下转化 NOx [27-28]。还有研究者将 Pt 原子负载在 TiO2 表面, 在蓝光( 430 ̄ 530 nm) 、绿光( 470 ̄570 nm) 照射下, 对 NOx 有很高的转化 效率, 甚至在红光( 580 ̄670 nm) 照射下也有一定的转化[29]。
3.2 载体的选择 TiO2 作催化剂转化 NOx 分为吸附和氧化 2 个过程, 而吸附过程尤为重要[22]。合适的载体不但能支 撑粉状 TiO2, 增加催化剂的表面积, 还能通过促进吸附过程 而提高光催化效率。新型的载体包括活性炭( AC) [15]、沸石[30]、 氧化钙[31]、ZrO2[32]、高岭土[33]等, 其中活性炭不但能促进吸附, 还 能很好地消除水蒸气对反应的抑制, 从而提高光催化效率[34]。
4 其他光催化剂
人们一直研究以 TiO2 为光催化材料降解 NOx, 近几年 来, 人们又发现了其他可用于降解 NOx 的新型光催化材料。 以离子交换技术和热真空技术在沸石中植入过渡金属离子 ( Cu+, Ag+, 或 Pb2+) [10-13], 以其作为光催化剂, 在紫外线的照射 下, 可在常温下将 NOx分解为氮气和氧气。用硅酸钒( VS!2) [12] 代替金属离子, 也可达到类似的效果。
AnpoM等从动力学角度分析了这类光催化剂分解NOx 的机理。他们认为, 在紫外线的照射下, 会有电子从光激发 下的金属离子和金属氧化物转移到 NOx 的反 π键上, 从而 引起 NOx 的光分解过程[10-12]。
5 展望
近10年来, 物理、化学工作者们围绕光催化机理及提 高 TiO2 的光催化效率等问题进行了大量的研究工作, 其大 部分主要涉及环境治理领域。TiO2 光催化脱除 NOx 的技术 尽管尚未成熟, 但有着诱人的前景。通过探索不同因素对光 催化效率的影响及催化作用机理, 人们对这一反应体系的 认识将越来越全面。然而, 为了使这一技术真正得到应用, 还有很多问题急需解决。如提高 TiO2 对高浓度 NOx 的脱除 效率, 减少有害中间产物的形成等, 只有解决了这些问题, 才能使该技术真正造福于人类。