手把手教你如何查询药品在美国FDA注册及缴费的信息
作为原料药出口型的制药企业,对美国市场的药品注册情况必须要有所了解,才能熟知市场需求,对产品的选择与销售策略是有很大参考意义的。在介绍查询方法之前,先简单说说原料药与制剂注册的一点基本知识:
对于原料药来说,产品销售到美国市场必须首先提交DMF,FDA的药物评价及研究中心(Center for Drug Evaluation and Research, CDER)收到文件后,FDA首先会对你递交的文件进行初步完整性审核,这个过程中不对文件进行技术性审核,通过之后可获得一个登记号(DMF号),凡是在FDA登记了DMF的,每年必须按时缴纳厂地费(Facility Payments);如果有制剂商购买了你的原料药(购买之前,制剂商会在FDA网站上查找哪些企业已有登记)进行制剂研发成功后,会向FDA提交新药注册申请(NDA)或仿制药注册申请(ANDA),这时候会启动对原料药DMF的技术审核,并要求你缴纳DMF费,此费用只是在第一个客户引用时需缴纳,这是与厂地费不同的地方。
根据上述介绍,如何知道有哪些企业的原料药已登记、已交费,哪些企业的制剂获批了呢?下面以图文的形式做一个详细的介绍。
一、原料药DMF登记信息查询
1、首先找到FDA官网的主页:https://www.fda.gov/,点击进去,相关画面截图如下:
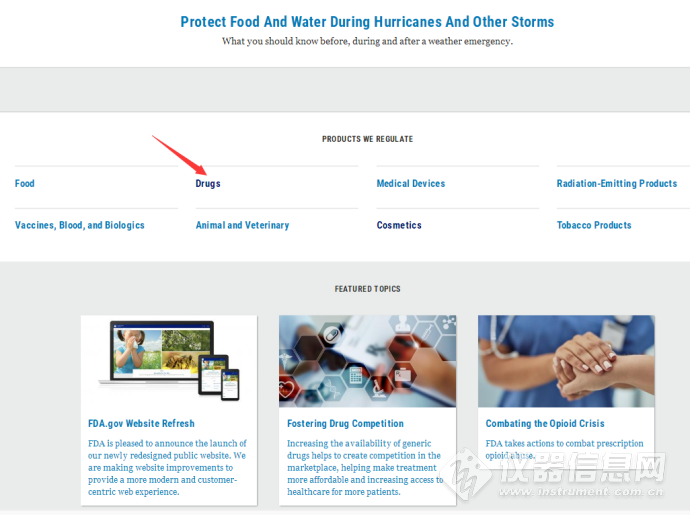
2、点击红色箭头处的“Drugs”,网页中部处画面如下:

3、继续点击Drug Development and Review Process,如下图:

4、点击Forms & Submission Requirements,如下图:
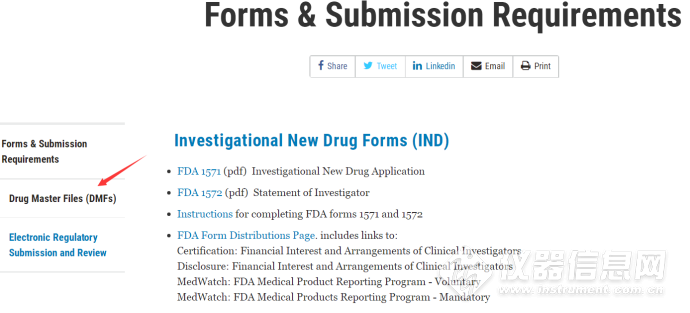
5、点击Drug Master Files(DMF),就可以看到两种格式的DMF清单啦
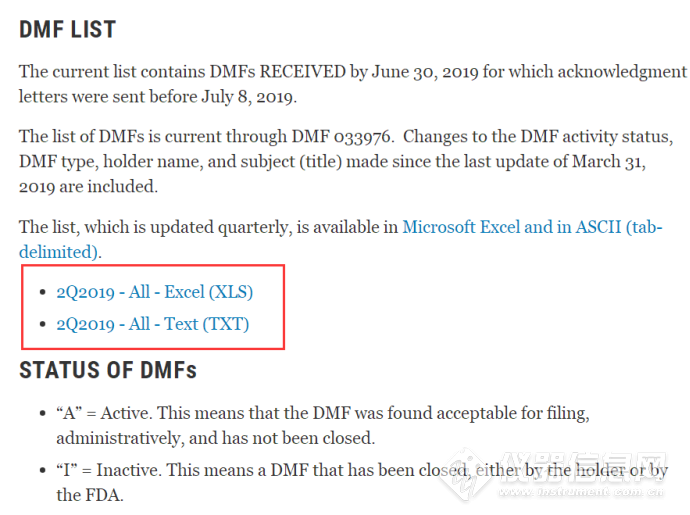
二、原料药缴费信息查询
1、打开FDA官网的主页:https://www.fda.gov/,如下:
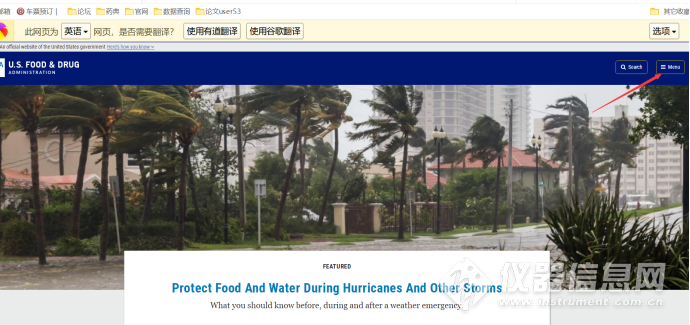
2、点击右上角的Menu,如下:
3、点击Industry,如下:

4、点击User Fees,如下:

5、点击箭头处Generic Drug User Fee Amendments,找到GDUFA PaidFacilities List,可以下载厂地费的付费信息:
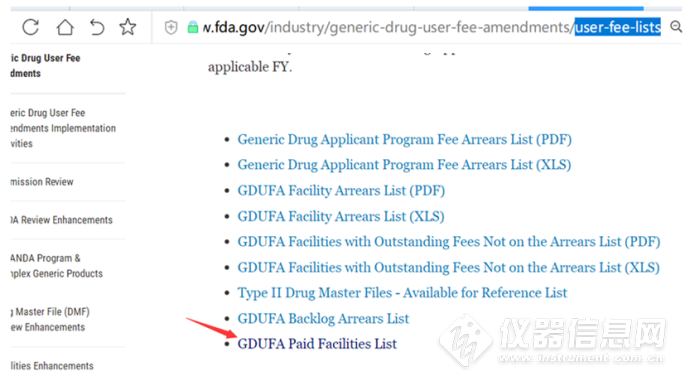
6、仍然在Generic Drug User Fee Amendments页面点击Drug Master File Fees:

找到红色框框处,点击可下载DMF费用的付费信息:

还是同样的页面,可以顺便看看,老外的收费可是相当高哦:
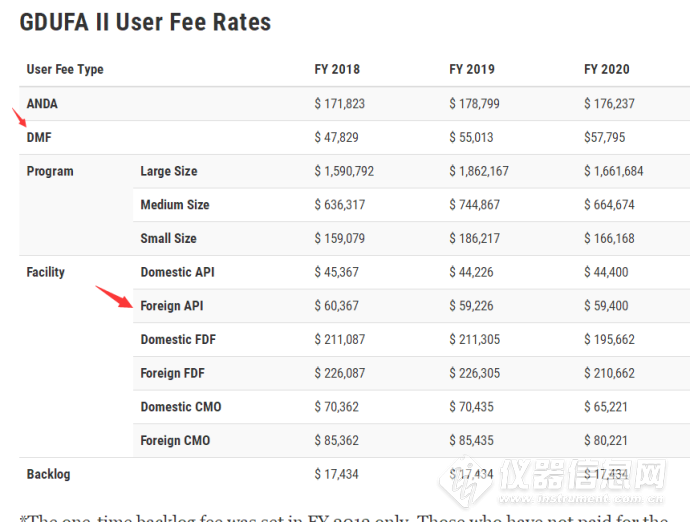
三、制剂批准信息
1、与前面相同,从主页https://www.fda.gov/找到以下页面:

2、点击Drug进入
3、再点击红色箭头处“Drug Approvals and Databases”,出现以下画面:

4、继续点击红色箭头处“Drug @FDA Search”,出现以下画面:

5、然后根据个人查询需求,只要知道产品的英文名,即可查到相关信息,比如我想查询美国FDA批准阿司匹林的情况,点击“A”进去,根据字母顺序找到ASPIRIN,可以看到ANDA号、剂型、注册公司:




















