基于TILLING技术的基因突变分析
小麦是我国主要的粮食作物,其栽培面积和总产量仅次于水稻,随着生活水平的日益提高,人们对小麦品质的要求也越来越高,因此,品质改良已成为小麦育种工作的重要目标之一[1]。
小麦是异源6倍体植物,基因组庞大,突变机制较为复杂,反向遗传学技术,例如T-DNA插入、转座子标签,已经越来越多的应用于研究中。然而,这些方法大多数,应用于基因组较小的模式植物,小麦的多倍性及转化体获得的难度,制约了这些方法的更好使用,而TILLING技术不受物种倍性影响,推动了基因功能研究和品质改良的发展。
1 材料与方法
1.1 植物材料
春小麦(Triticum aestivum L.)品种龙辐麦17经航天诱变选育而成。共获得1122个EMS诱变的龙辐麦17 M2代单粒传植株,苗期单株编号,采集叶片,迅速冷冻干燥,用于DNA提取。
1.2 基因组DNA提取及DNA池构建
将干燥后的叶片按编号置于装有珠子的1.5ml离心管中,利用组织研磨器Vibration Mill Type MM301(Retsch GmbH Co, Germany)将叶片磨成粉末状;加600μl DNA Extraction buffer [0.1 mol/ L Tris;0.1 mol/ L KCl;0.5M EDTA pH 8.0;1 mol/ L PVP 40;1.5 mol/ L Na2S2O6],充分混匀;保温振动1 h;加200μl 5 mol/L KAc,混匀并离心;取约300 μl上清液加至165 μl预冷的异丙醇中,沉淀DNA;用70 %乙醇洗DNA,干燥后,溶于TER[Tris 10mmol/L,EDTA 1 mmol/L,RNA酶0.05mg/ml],-20 ℃保存备用。
利用1.0%的琼脂糖凝胶电泳检测DNA样品,并将其稀释至40 ng/μl,随机两两等量混匀,构建两倍的DNA池,用于后续TILLING筛选。
1.3 特异性引物设计及筛选
根据NCBI提供的目标基因序列信息,在线设计引物,并用1%琼脂糖凝胶电泳检测PCR产物,选择PCR产物条带单一,大小在700-1500左右的4对引物(表1),其中除Pinb引自Wang等[2](2008)。
表1 用于TILLING检测的基因及其荧光标记引物序列
Table1 Genes and their IRDye labled primer sequences used in TILLING
基因 Gene | 引物序列 Primer sequence (5′–3′) | 长度 Length (bp) |
正向 Forward | 反向 Reverse |
Pinb | CCAACGAAACTAATGAGAAATAAAAAGGTG | AAGTTGTTGGATGGACGAATAAGGTT | 1334 |
Waxy | ACCCGCATGGTGTTTGATAATTTCAGTG | AGAATGCCACCTAGCCATGAAATGAGT | 790 |
1.4 TILLING检测
参照潘娜[3](2011)建立的小麦TILLING技术检测平台,对目的基因进行检测。采用Touchdown PCR程序,10μl PCR体系含10 ×Buffer 0.5μl;Mg2+ 0.6μl;dNTP 0.8μl;引物各0.4μl;Ex Taq HS DNA聚合酶0.05μl,在Bio-Rad c1000仪上扩增。扩增后加20μl 0.1M CELⅠ酶,45℃酶切15 min,利用Sephadex G50(GE Healthcare 公司)纯化板纯化酶切产物,并90℃浓缩35-45 min。利用6%变性聚丙烯酰胺凝胶,在LI-COR 4300仪器中电泳检测酶切产物并采用Gelbuddy软件对电泳图像分析处理,标记突变位点。
1.5 基因点突变分析
检测到突变后对PCR产物进行测序验证,利用Invitrogen软件、NCBI等对序列进行比对、翻译等分析,确定突变位置与类型。
点突变密度(%)=突变碱基数/检测总碱基数×100%。
2 结果与分析
本实验对小麦籽粒硬度基因pinb进行了1122个单株的TILLING检测。基因的突变密度分别为1/374.18 kb。
Pinb基因共获得7个突变株系的4个不同的突变位点(图1),有6个突变单株的碱基突变位点均位于外显子区域,突变株编号及突变位点分别是LF996第512bp位的C-T碱基转换,LF892、LF997、LF919第726bp位的G-A碱基转换,及LF791、LF1114第750bp位的G-A碱基转换,LF996 pinb基因第37为氨基酸S变为氨基酸F,LF892、LF997、LF919 pinb基因第110为氨基酸G变为氨基酸S,LF791、LF1114第116位氨基酸W被终止,内含子区域突变是LF890突变株第350bp碱基G转换为碱基A。见表1
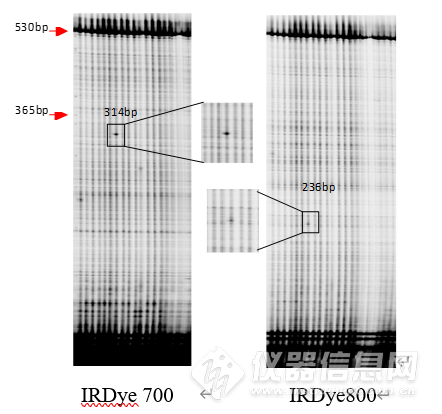
图1 Waxy基因电泳图
Fig1 Electrophorogram of Waxy gene
表1 基因点突变信息
Table1 Point mutations of quality gene
基因名称 Gene name | 登录号 Accession No. | 基因大小 Gene size (bp) | PCR扩增长度 PCR size (bp) | 等位变异 Mutant allele | 氨基酸突变 amino acid mutation | 突变株编号 Number of mutation | 总突变频率 Total mutation density (kb) |
pinb | AJ302100.1 | 870 | 1334 | C512T | S37F | 996 | 1/374.18 |
| | | | G726A | G110S | 892、919、997 |
| | | | G750A | W116- | 791、1114 |
| | | | G350A | 未改变 | 890 |
3 讨论
籽粒硬度是小麦重要的品质性状,对食品加工及磨粉质量都有重要影响。Pinb是调控籽粒硬度的主效基因之一,与pina基因共同作用决定小麦胚乳质地[4-5]。
本实验Pinb基因的突变密度是1/374.18 kb,低于Feiz等[6]在普通软质小麦突变体库得到的pinb基因1/12 kb的突变密度,但高于潘娜[3]利用空间诱变新麦18突变体库群体得到的该基因1/3073 kb的突变密度。Morris等[5, 7]获得的硬红春小麦pinb基因突变体,分别发生在pinb基因第39位和第44位的色氨基酸T及第56位半胱氨酸C,均突变为终止密码子。Wang等[13]获得Pinb基因,382bp处C – T碱基转换和257bp处G – A碱基转换。在潘娜[3]创制的TILLING群体中,pinb基因组736 bp的A碱基缺失,引起移码突变,而本实验突变株LF791、LF1114,LF996,LF892、LF997、LF919的基因突变依次为750bp位的G-A碱基转换,512bp位的C-T碱基转换,726bp位的G-A碱基转换,均导致错义突变。
王亮等[8]和Chen等[9]的研究中几乎所有Puroindoline变异类型的籽粒硬度值都显著高于野生型,而本实验,对突变株进行表型分析,籽粒硬度测定显示LF996、 LF892、LF1114突变株的籽粒硬度均极显著低于野生型。此外,突变体自交系研究发现,突变对小麦出粉率、面包体积、面粉灰分等品质性状均有影响,不同Puroindoline变异类型之间在磨粉、面包等加工品质上也存在较差别[9-10]。基于以上的研究发现,可利用本实验获得的突变株,进行后代品质研究,为品质改良奠定基础。
4 结 论
本研究所获得的基因点突变及表型突变株为植物基因功能研究及小麦品质改良提供了新材料。
References
[1] Liu L(刘丽), Yang J-H(杨金华), Hu Y-X(胡银星), Cheng G(程耿). Research Progress in Effects of Glutenin Subunits on Wheat Processing Quality. Journal of Agricultural Science and Technology (中国农业科技导报), 2012, 14(1): 33-42 (in Chinese with English abstract)
[2] Wang J, Sun J Z, Liu D C, Yang W L, Wang D W, Tong Y P, Zhang A M. Analysis of Pina and Pinb alleles in the microcore collections of chinese wheat germplasm by Ecotilling and identification of a novel Pinb allele. Journal of Cereal Science 2008, 48(3): 836-842
[3]潘娜. 空间环境诱发小麦突变体的TILLING分析, 中国农业科学院, 2011.
[4]CaPPaerlliR,Bo币elloqGirouxMJ,AmoorsoMGPuorindolineA一geneexPerssion15involved
inassociationofPuroindolinetostacrh.TheoerctialandAPPliedGenetics,2003,107:1463一1468
[5]Chen F. Molecular Characterization of Puroindoline Alleles in Chinese and CIMMYT Common Wheats and Their Eeffct on Porcessing Quaiity
[6]Feiz L, Martin J M, Giroux M J. Creation and functional analysis of new Puroindoline alleles in Triticum aestivum.Theoretical and Applied Genetics,2009, 118:247-257
[7] Morris C F,Lillemo M,Simeone M C,Giorux M J,Bbab S L,Kimberiee K K.Pervalence of Puorindoline garin hdarness genotypes among historieally significant North American spring and winter wheats. Crop Scienee,2001,41:218-228
[8] Chen F,He z H,Xia x C,el a1.Molecular and biochemical charac—terization of P“roindoline a and b alleles in Chinese landraces andhistorical eultivars[J].Theoretical and Applied Genetics. 2006,112:400—409.
[9] 王亮,穆培源,桑伟,等.新疆小麦品种籽粒硬度及Puroindoline基因等位变异的分子检测[J].麦类作物学报。2010,30(1):17-22.
[10] 赵新,王步军.不同硬度小麦品质差异的分析[J].麦类作物学报,2009,29(2):246—251。


