推荐厂家
暂无
暂无




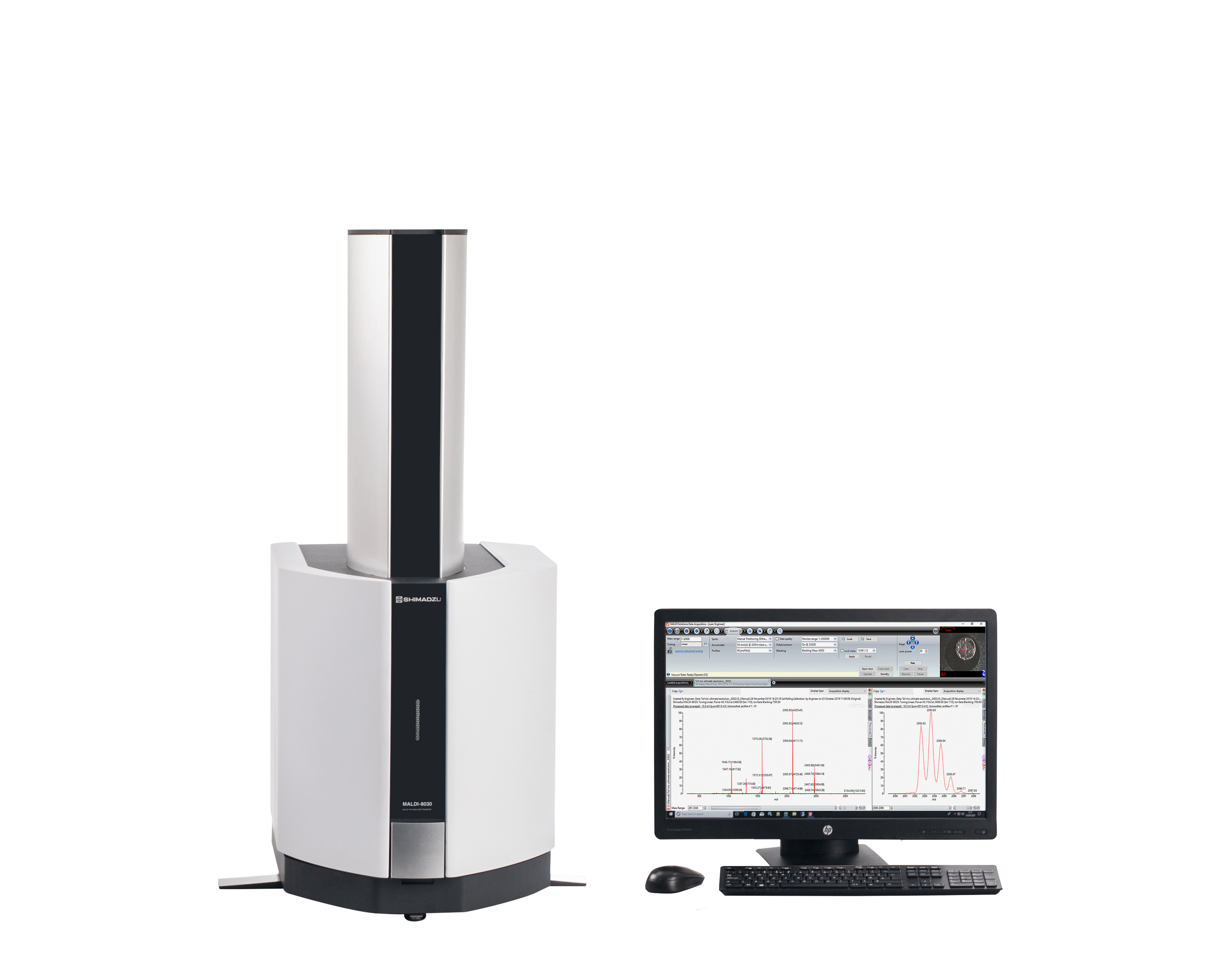

方法确认要求实验室对非标准方法、实验室制定的方法、超出其预定范围使用的标准方法、扩充和修改过的标准方法的确认制定程序。实验室做方法确认应该综合考虑成本、风险和技术可行性基础上,并根据预期的用途来进行方法确认。实验室进行方法确认的内容应完整,一般包括:a)方法的选择性;b)方法适用范围;c)检出限和/或定量限;d)线性范围;e)精密度(重复性和/或再现性);f)稳健度;g)正确度;h)准确度;i)灵敏度;j)结果的测量不确定度。确认方法特性参数的选择1.方法确认首先要明确检测对象特定的需求,包括样品的特性、数量等,并应满足客户的特殊需要,同时应根据方法的预期用途,选择需要确认的方法特性参数。典型的需要确认的方法特性参数见下表。典型方法确认参数的选择 确证方法 筛选方法待评估性能参数定量方法定性方法定量方法定性方法检出限*√√√√定量限√√--灵敏度√√--选择性√√√√线性范围√-√-测量区间√-√-基质效应√√√-精密度(重复性和再现性)√-√-正确度√---稳健度√√√√测量不确定度(MU)√---注:*:被测物的浓度接近于“零”时需要;√:表示正常情况下需要的性能参数;-:表示正常情况下不需要。2.通常情况下,实验室内方法确认,需要确认的技术参数包括方法的选择性、检出限、定量限、线性范围、正确度、重复性、稳健度等。3.通常情况下,对于定性方法,实验室间方法确认至少应确认方法的检出限和选择性;对于定量方法,实验室间方法确认至少应确认方法的适用对象、线性范围、定量限和精密度。
定义??1 方法确认??方法确认,英文标准中称为“validation”,可译为“确认”。其定义为“通过提供客观证据,对特定的预期用途或应用要求,得到满足的认定。”??方法确认是对非标准方法,实验室制定的方法,超出预定范围使用的标准方法或其它修改的标准方法确认能否合理、合法使用的过程。??2 方法验证??方法验证,英文标准中称为“verification”,可译为“证实”或“验证”。在实验室工作中,其定义为“提供客观证据,证明某项目满足规定要求”。??方法验证是指在标准方法或者非标方法在引入实验室使用前,对实验室从人、机、料、法、环、测等方面评定其是否有能力在满足方法要求的情况下开展检测校准活动的过程。??二者从定义上很相似,在实际操作中,验证或确认参数也都需要从检出限、定量限、灵敏度、选择性、线性范围、测量范围等参数进行评估。??这样看来,方法验证和方法确认从技术层面上殊途同归,但实际上,二者却有着本质上的区别。其中最关键的区别,在于方法确认与方法验证的对象是不同的。??对象不同??1 方法确认??方法确认主要针对非标方法,其对象在“17025”标准中有所规定。从广义的理解来看,除了国际、区域、国家、行业、地方标准所规定方法以外的检测方法都属于非标准方法,除了第一类的方法属于标准方法,其他三类都属于非标准方法。??当实验室采用的检测方法为非标准方法时,就要对非标准方法进行确认,针对非标准方法的不同类型,进行区分来加以讨论。??2 方法验证??方法验证,是针对标准方法进行的。“17025”中规定,在引入检测或校准之前,实验室应证实能够正确地运用这些标准方法。??标准方法是指由公认机构经过评价确认后向社会公开发布的技术规范文件。实验室在使用标准方法之前,应经过方法验证,或称之为方法证实,即实验室在使用标准方法进行检测前需要证实实验室使用标准方法的技术能力是否达到了标准的规定要求。??目的不同??1 方法确认??确认该非标准方法能否合理、合法使用。??2 方法验证??验证实验室是否有能力按方法要求开展检测/校准活动。??内容不同??1 方法确认??一个非标方法的确认,在文件中要包括以下内容:??(1)方法适当的标识 ??(2)方法所适用的范围 ??(3)检测或校准样品是什么类型,以及对样品的描述 ??(4)被测参数的范围 ??(5)方法对仪器、设备的要求,包括仪器设备关键技术性能的要求 ??(6)需要用到的的标准物质 ??(7)方法对环境条件的要求,对环境稳定周期的要求 ??(8)操作步骤,包括:??—样品的标志、处置、运输、存储和准备 ??—检测、校准工作开始前需要进行的检查 ??—检查设备工作是否正常,需要时,使用前之前对设备进行校准和调整 ??—结果的记录方法 ??—安全注意事项 ??(9)结果接受(或拒绝)的准则、要求 ??(10)需记录的分析数据 ??(11)不确定度评定。??非标方法的技术确认,需要从五个方面确认:??(1)使用参考标准或标准物质进行比较 ??(2)与其他方法所得的结果进行比较 ??(3)实验室间比对 ??(4)对影响结果的因素作系统性评审 ??(5)根据对方法的理论原理和实践经验的科学理解,对所得结果不确定度进行的评定。??技术确认要尽可能全面,并需有确认记录。??2 方法验证??(1)对执行新方法所需的人力资源的评价,即检测/校准人员是否具备所需的技能及能力,必要时应进行人员培训,经考核后上岗。??(2)对现有设备适用性的评价,是否要补充新的的标准器或标准物质。??(3)对物品制备,包括前处理、存放等各环节是否满足新方法要求的评价。??(4)对操作规范、不确定度,原始记录、报告格式及其内容是否适应新方法要求的评价。??(5)对设施和环境条件的评价,必要时进行验证。??(6)对新方法正确运用的评价,当有旧方法变更时,应对新旧方法进行比较,尤其是差异分析与比对的评价。??(7)按新方法要求进行两次以上完整模拟检测/校准,出具两份完整结果报告。??注意:1. 方法确认应有文件规定和相应记录,当修改已经确认过的方法时,应确定 这些修改的影响,如果影响到原有的确认,应重新进行确认。??2. 方法验证应有文件规定和相应记录,当方法变化后,应重新进行验证。??两者最大的区别??通俗的讲,标准方法的验证(证实)和非标准方法的确认最大的区别是,对于前者实验室可以依“葫芦画瓢”,方法的特性指标、应用范围等有关权威组织都帮你完成了,而对于后者,你只能通过“自身”努力来证实你所用的方法,不论自创还是“模仿”,能够真正满足客户的要求。??两者的联系??相对于方法验证来说,方法确认类似于方法验证的简化版,且方式更灵活。但是实验室最终该如何做好方法验证或确认,还需要各实验室对相关法规标准及参考文献进行深入的研究,制定适合自身的作业指导书并严格执行。??将方法验证、确认和转移简单总结如下:??任何分析检测的目的都是为了获得稳定、可靠和准确的数据,方法验证在其中起着极为重要的作用。方法验证的结果可以用于判断分析结果的质量、可靠性和一致性,这是所有质量管理体系不可分割的一部分。一般在下列情况下,要求对分析方法进行验证、确认(或称证实)或重新验证:??1)首次用于常规检测前 ??2)转到另一个实验室时 ??3)对于验证过的方法,其条件或方法参数发生变化时(例如,仪器性能参数发生改变或样品基质不同时),并且这种变化超出了方法的原适用范围。
最近,实验室的检测标准有更新了,是农药残留检测的方法,GB23200.8-2016,里面我们有22项是通过的CMA认证的。那么问题就来了,在方法确认的时候,我们是否需要22项都要做确认呢?我理解的确认是:加标回收试验,看方法精密度和回收率是否达到标准要求。各位老师,前辈,一起来侃侃吧!在方法确认的时候,我们是否需要把通过认证的全部项目进行确认呢?
 400-889-7796
400-889-7796
 留言咨询
留言咨询

 400-612-9980
400-612-9980
 留言咨询
留言咨询

 400-629-8889
400-629-8889
 留言咨询
留言咨询


