医院污水是医疗机构在治疗病人活动过程中产生的废水和生活污水。医院污水中往往含有病原性微生物、有毒有害的化学污染物、有机物和放射性污染等,具有空间传染、急性传染和潜伏性传染等特征,不经有效处理将成为疫情扩散的一条重要途径,对生态环境及人类健康造成极大的危害[1-4]。
目前,我国医院普遍采用一级处理加消毒工艺,消毒剂通过与水泵联动或虹吸水混合后,进入接触池,在接触池内污水和消毒剂经过一定时间的接触,达到水质净化和消毒要求后排放。医院污水处理典型工艺流程见图1:
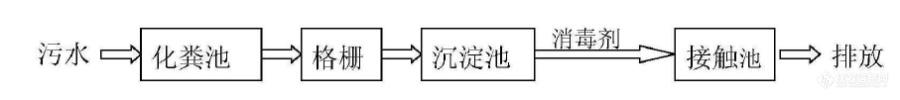
图1 医院污水处理典型工艺流程
在处理工艺中,采用消毒法杀灭污水中的病原菌、病毒和其他有害微生物。常用的消毒剂主要有液氯、次氯酸钠、漂白粉、二氧化氯及氯胺等,其中以次氯酸钠的应用最为广泛(占54.5%),其次是二氧化氯(占27.3%),而液氯近年来有被取代的趋势[5-8]。
由于医院在污水中使用大量的含氯消毒剂,随着分析检测技术的提高和研究的深入,目前能从含氯类污水中检测到的致癌物多达数百种。同时还检测到一些能引发人肝和神经中毒,代谢紊乱的化合物,以及可能导致怀孕妇女早产及胎儿的体重过轻、引发肝或肾伤害疾病的化合物。因此,我国《医疗机构水污染物排放标准》(GB18466-2005)中对余氯有着明确的限量值,总余氯量要小于0.5mg/L,严格控制不合格污水排出已迫在眉睫。为此,研制适应医院用污水中总余氯测定的标准物工作,就成为严格控制、确保监测质量工作能够执行的关键所在。
参照《环境标准样品研复制技术规范》(HJ/T 173-2005)的要求,我们在研究过程中制定了研究路线图,见图2。
并在作样品的均匀性、稳定性检验过程中按GB/T 6678-2003 化工产品采样总则进行样品的随机抽样操作。
1 仪器与试剂
1.1 仪器
AE240型十万分之一电子天平(瑞士梅特勒公司)
TP114型万分之一电子天平(美国丹佛仪器公司)
滴定管(50mL和5mL)、轻质具塞瓶(100mL和10mL)碘量瓶、容量瓶、锥形瓶、烧杯等玻璃仪器(北京玻璃仪器厂)
1.2 试剂
硫代硫酸钠(分析纯,国家标准物质研究中心)
重铬酸钾(标准物质,北京化学试剂研究所)
高锰酸钾(标准物质,北京化学试剂质监站科技开发部)
氯胺T(分析纯,天津市光复精细化工研究所)
硫酸,冰醋酸,碘化钾,可溶性淀粉,氨水,丙三醇,无水乙醇,碳酸钠,试剂均为分析纯(天津化学试剂厂)。
2 实验方法
2.1 候选物的纯度及均匀性检验
通过前期调研发现[ ],氯胺T成为总余氯标准物质样品研究的候选物。由于溶液标准物质的标准值通常是基于样品称量质量和纯度值计算得到的,因此,制备前首先要对候选物进行纯度及均匀性进行检验。
2.1.1 纯度检验
称取氯胺T样品0.5 g,置于500 mL具塞锥形瓶中,加水溶解,至锥形瓶里溶液的体积约为50 mL时,加入10%碘化钾溶液25 mL及冰醋酸5 mL。盖上瓶塞使之混和均匀,然后放置暗处约10 min,使作用完全。用水沖洗瓶口及瓶塞,并用0.1 mol/L硫代硫酸钠溶液滴定,滴至游离碘的深棕色接近消失而略具淡黄色时,加入2 mL 5%淀粉指示剂,继续用硫代硫酸钠滴定,滴至蓝色消失时即为滴定终点。(M氯胺T = 281.69g/mol)
表1 氯胺T纯度检验
滴定管编号 2 液温 20.3 ℃
内 容 | 1 | 2 | 3 | 4 | 5 |
m样(g) | 0.5018 | 0.4957 | 0.4825 | 0.4613 | 0.4807 |
校正后测定氯含量消耗滴定剂的体积 | V1(测定消耗Na2S2O3)(mL) | 35.21 | 34.84 | 33.84 | 32.37 | 33.73 |
V2(滴定管的校正值)(mL) | -0.11 | -0.11 | -0.11 | -0.10 | -0.11 |
V3(溶液温度补正值)(mL) | 0.00 | 0.00 | 0.00 | 0.00 | 0.00 |
V(校正后体积)(mL) | 35.21 | 34.73 | 33.73 | 32.27 | 33.62 |
c(Na2S2O3)(mol/L) | 0.1000 |
样品含量(%) | 98.83 | 98.68 | 98.46 | 98.54 | 98.51 |
样品含量平均值(%) | 舍 | 98.55 |
极差(%) | | 0.22 |
标准偏差(%) | | 0.094 |
2.1.2 均匀性检验结果
样品均匀性的测定采用两口瓶进行,将氯胺T样品放入两口瓶内(不要放的太满),充分震荡,分层后,分别取上、下层样品,按1.3.1.1所述的方法检验不同粒径的氯胺T样品中的氯含量,从而判断样品的均匀性。
表2 氯胺T样品的均匀性检验结果
滴定管编号 2 液温 20.3 ℃
内 容 | 上层样品中氯的含量测定 | 下层样品中氯的含量测定 |
1 | 2 | 3 | 4 | 1 | 2 | 3 | 4 |
m样(g) | 0.4787 | 0.5011 | 0.4918 | 0.5038 | 0.4851 | 0.4476 | 0.5109 | 0.5114 |
V1(Na2S2O3)(mL) | 33.60 | 35.14 | 34.47 | 35.34 | 34.04 | 31.42 | 35.84 | 35.89 |
V2(滴定管校正值) | -0.11 | -0.11 | -0.11 | -0.11 | -0.11 | -0.09 | -0.11 | -0.11 |
V3(温度补正值) | 0.00 | 0.00 | 0.00 | 0.00 | 0.00 | 0.00 | 0.00 | 0.00 |
V(校正后体积)(mL) | 33.49 | 35.03 | 34.36 | 35.23 | 33.93 | 31.33 | 35.73 | 35.78 |
c(Na2S2O3)(mol/L) | 0.1000 |
样品含量(%) | 98.54 | 98.46 | 98.40 | 98.48 | 98.51 | 98.59 | 98.53 | 98.53 |
平均值(%) | 98.47 | 98.54 |
极差和相对极差(%) | 0.14(0.142)(多保留一位) | 0.08(0.081)(多保留一位) |
标准偏差(%) | 0.058(0.059)(多保留一位) | 0.035(0.035)(多保留一位) |
样品平均值(%) | 98.55 |
接近程度(%) | 99.92 | 99.99 |
氯的化学性质非常活泼,如何令其长期稳定在具有氧化性的高价状态且量值不变是保证其量值的稳定及计量可溯源性的基础。配制标准物质样品溶液首先需要选择合适的溶剂,本项目对氯胺T浓度分别为1.0、0.5和0.2g/L时,在各种溶液基质(水、氨水、丙三醇、乙醇溶液)及不同贮存条件(常温、冷藏、密封冷藏)下的稳定性进行考察,从而选择出最有利于氯胺T稳定的液态介质、浓度及贮存条件。
2.2 标准物质候选物溶液的制备和溶液稳定条件筛选
氯溶液的稳定性是本项研究的重点,在研制条件初选中,选择用聚丙烯白塑料瓶做容器,并选择室温贮存和冰箱低温贮存(4℃)两种方式进行筛选,具体条件见表3。
表3 溶液稳定条件筛选
储存条件 | 条件1 | 条件2 | 条件3 |
容 器 | 聚丙烯白塑料瓶 | 带内盖的聚丙烯白塑料瓶 | 聚丙烯白塑料瓶 |
贮存温度 | 室温 | 低温(4℃) | 低温(4℃) |
检验间隔 | 1天 | 1天 | 1天 |
检验时间 | 7天 | 7天 | 7天 |
对氯胺T溶液三种浓度,四种不同溶液基质和不同贮存条件的稳定性考察结果是:
2.2.1 1.00g/L氯胺T溶液的稳定性
由实验结果可知,氯―水溶液常温下的稳定性最差,7天内变化了0.200g/L,减小总浓度的20%;氯―乙醇溶液低温下保存时溶液的稳定性最好,7天内变化了0.0263g/L,减小总浓度的2.63%。
2.2.2 0.50g/L氯胺T溶液的稳定性
由实验结果可知:氯―氨水溶液常温下的稳定性最差,7天内变化了0.0971g/L,减小总浓度的22.54%;氯―丙三醇低温下保存时溶液的稳定性最好,7天内变化了0.0167g/L,减小总浓度的3.40%。
2.2.3 0.20g/L氯胺T溶液的稳定性
由实验结果可知:氯―水溶液常温下的稳定性最差,7天内变化了0.0383g/L,减小总浓度的18.31%;氯―乙醇低温下保存时溶液的稳定性最好,7天内变化了0.0032g/L,减小总浓度的1.55%。
由上面实验总结表明,0.50g/L氯―乙醇溶液(冷藏)、0.20g/L氯―乙醇(冷藏)和0.20g/L氯―丙三醇溶液(冷藏)的稳定性较好,可作为余氯标准物质样品的备选溶液使用。
在常规总余氯测定分析中,总余氯测定多采用分光光度法,在《水质游离氯和总氯的测定:N,N―二乙基―1,4―苯二胺分光光度法》(GB11898-1989)中标注:“本标准适用于0.0004~0.07mmol/L(0.03~5mg/L)游离氯或总氯(以Cl2计)的测定。样品浓度较高时,需进行稀释”。因此,0.2g/L的浓度能确保日常水质分析中总余氯测定的需要。同时,相对于丙三醇和乙醇的溶液基质来说,水―乙醇体系对该检验方法的干扰较小。为此,确定以0.20g/L氯―乙醇(冷藏)溶液作为最佳研究方案。
2.3 标准物质样品的均匀性及稳定性检验
标准物质的均匀性是指标准物质的特征量值在空间分布上的均匀程度,为了确定同一批环境标准样品最小包装单元间特性量值的变动性,采用了等重复测量次数的方差分析实验设计,进行瓶间均匀性的研究方法。即将随机抽取每个单元样品,进行等次数重复测量,从而估计因瓶间不均匀可能引起的特性量值不确定度。另外,为了确定环境标准样品单个包装单元内特性量值的变动性,还采用了等重复测量次数的方差分析实验设计,进行瓶内均匀性研究。
而标准物质的稳定性则是标准物质样品的特征量值随时间变化的程度。根据《标准样品工作导则》(GB/T 15000-2008)中关于稳定性检验的要求,当不同时间间隔内测定结果的偏差不超过测试方法的精密度,则认为该批样品在试验时间内是稳定的。本部分实验对制备的总余氯标准样品进行了均匀性及稳定性分析,从而检验其是否能达到标准物质的相关技术规范要求。
为进行标准物质样品的均匀性及稳定性研究性实验,我们一次性密封了300瓶样品,每瓶内装20 mL溶液。并对每瓶溶液进行编号,从1~300号。
2.3.1 样品瓶间均匀性检验
根据HJ/T173-2005《环境标准样品研复制技术规范》标准中5.2.2.1的相关规定,在300瓶样品溶液中抽21瓶做“瓶间均匀性检验”,为能使测定结果具有代表性,将300瓶样品分成三组,每组100瓶,依据部分随机数表(见表4),在三组中各抽样7瓶组成21瓶检验样品。抽取结果见表5
表4 部分随机数表
68 | 85 | 97 | 74 | 47 | 53 | 90 | 05 | 90 | 84 | 87 | 48 | 25 | 01 | 11 | 05 | 45 | 11 | 43 | 15 | 60 | 40 | 31 | 84 |
59 |
59 | 54 | 13 | 09 | 13 | 80 | 42 | 29 | 63 | 03 | 24 | 64 | 12 | 43 | 28 | 00 | 01 | 65 | 62 | 07 | 79 | 83 | 05 | 59 |
61 |
39 | 18 | 32 | 69 | 33 | 46 | 58 | 09 | 34 | 03 | 59 | 28 | 97 | 31 | 02 | 65 | 47 | 47 | 70 | 39 | 74 | 17 | 30 | 22 |
65 |
67 | 43 | 31 | 09 | 12 | 60 | 19 | 57 | 63 | 78 | 11 | 80 | 10 | 97 | 15 | 70 | 4 | 89 | 81 | 78 | 54 | 84 | 87 | 83 |
42 |
61 | 75 | 37 | 16 | 56 | 90 | 75 | 39 | 03 | 57 | 49 | 92 | 72 | 95 | 27 | 52 | 87 | 47 | 12 | 52 | 54 | 62 | 43 | 23 |
13 |
表5 瓶间均匀性检验的抽样结果表
第一组 | 68 | 85 | 97 | 47 | 53 | 5 | 90 |
第二组 | 184 | 187 | 148 | 125 | 101 | 105 | 145 |
第三组 | 211 | 243 | 215 | 260 | 240 | 231 | 284 |
2.3.1.1 瓶间均匀性检验的操作步骤
取10.00mL样品溶液放入200mL的碘量瓶中,加入0.5g碘化钾和1mL1.0mol/L的硫酸溶液,液封后,放入暗处静置5min,用c(Na2S2O3) = 0.1mol/L的标准滴定溶液滴定至淡黄色,加2mL 5%的淀粉指示剂,继续用c(Na2S2O3) = 0.1mol/L的标准滴定溶液滴定至溶液蓝色消失,同时做空白实验。
2.3.1.2 计算公式:
2.3.1.3 瓶间均匀性检验数据和结果统计
表6 瓶间均匀性检验数据统计
V空 = 0.00mL c(Na2S2O3) = 0.1000mol/L t液温= 20℃
实验相关数据 | 68 | 85 | 97 | 47 | 53 | 5 | 90 |
V(Na2S2O3) (mL) | 1.154 | 1.153 | 1.154 | 1.154 | 1.154 | 1.153 | 1.153 |
试样中氯含量(g/L) | 0.2045 | 0.2044 | 0.2045 | 0.2045 | 0.2045 | 0.2044 | 0.2044 |
平均氯含量 (g/L) | 0.2045 |
相对标准偏差 | 0.03% |
实验相关数据 | 184 | 187 | 148 | 125 | 101 | 105 | 129 |
V(Na2S2O3) ( mL) | 1.155 | 1.155 | 1.153 | 1.153 | 1.155 | 1.155 | 1.153 |
试样中氯含量(g/L) | 0.2047 | 0.2047 | 0.2044 | 0.2044 | 0.2047 | 0.2047 | 0.2044 |
平均氯含量(g/L) | 0.2046 |
相对标准偏差 | 0.08% |
实验相关数据 | 211 | 243 | 215 | 260 | 240 | 231 | 284 |
V(Na2S2O3) ( mL) | 1.154 | 1.155 | 1.153 | 1.154 | 1.154 | 1.153 | 1.155 |
试样中氯含量(g/L) | 0.2045 | 0.2047 | 0.2044 | 0.2045 | 0.2045 | 0.2044 | 0.2047 |
平均氯含量(g/L) | 0.2045 |
相对标准偏差 | 0.06% |
结论:从21瓶样品的“瓶间均匀性检验”结果中可以看出,总平均值为
R=s/ρ=0.00018/0.2045=0.09%
2.3.2 瓶内均匀性检验
如上所述,从300瓶样品溶液中抽抽12瓶做“瓶内均匀性检验”。抽取结果见表7
表7 瓶内均匀性检验的抽样结果表
第一组 | 59 | 54 | 13 | 9 |
第二组 | 113 | 180 | 142 | 129 |
第三组 | 263 | 203 | 224 | 264 |
2.3.2.1 瓶内均匀性检验的操作步骤
取10.00mL溶液放入200mL的碘量瓶中,加入0.5g碘化钾和1mL1.0mol/L的硫酸溶液,液封后,放入暗处静置5min,用c(Na2S2O3) = 0.1mol/L的标准滴定溶液滴定至淡黄色退去,加2mL5%的淀粉,继续用c(Na2S2O3) = 0.1mol/L的标准滴定溶液滴定至溶液蓝色消失,同时做空白实验。
2.3.2.2 计算公式
2.3.2.3 瓶内均匀性检验数据和结果统计
表8 瓶内均匀性检验数据统计
V空 = 0.00mL c(Na2S2O3) = 0.1000mol/L t液温= 20.2℃
实验相关数据 | 59 | 54 | 13 | 9 |
取液操作说明 |
从溶液上层取10.00mL,逐渐将移液管尖下移。 |
V(Na2S2O3)(mL) | 1.153 | 1.153 | 1.154 | 1.152 |
试样中氯含量(g/L) | 0.2044 | 0.2044 | 0.2045 | 0.2042 |
平均氯含量(g/L) | 0.2044 |
相对标准偏差 | 0.06% |
实验相关数据 | 113 | 180 | 142 | 129 |
取液操作说明 |
将移液管尖插到溶液下层,取10.00mL中层溶液。 |
V(Na2S2O3)(mL) | 1.152 | 1.154 | 1.152 | 1.154 |
试样中氯含量(g/L) | 0.2042 | 0.2045 | 0.2042 | 0.2045 |
平均氯含量(g/L) | 0.2043 |
相对标准偏差 | 0.09% |
实验相关数据 | 263 | 203 | 224 | 264 |
取液操作说明 |
将移液管尖插到溶液瓶底,取10.00mL下层溶液。 |
V(Na2S2O3)(mL) | 1.153 | 1.155 | 1.153 | 1.154 |
试样中氯含量(g/L) | 0.2044 | 0.2047 | 0.2044 | 0.2045 |
平均氯含量(g/L) | 0.2045 |
相对标准偏差 | 0.09% |
结论:从12瓶样品的“瓶内均匀性检验”结果中可以看出,总平均值为
R=s/ρ=0.00015/0.2044=0.07%
2.3.3 “瓶间均匀性检验”和“瓶内均匀性检验”的总结
本项实验共抽33瓶样品,其总平均值为
R总=s/ρ=0.00014/0.2045=0.07%
从以上结果可以看出,瓶间均匀性检验和瓶内均匀性检验的相对标准偏差均达到要求,可以认为样品均匀一致。
2.4 样品溶液稳定性检验
稳定性实验需要对样品进行为期6个月的随机抽样检验,我们对样品每隔2天进行等重复性随机抽样检验,抽样方式同上。检验结果统计见图3

图3样品溶液稳定性检验统计结果
在六个月中,每隔三天检测一个点,每点随机抽三个样品,六个月共检测62次,在300瓶样品中共抽检186个样品,检测总结果是:
内 容 | 结 果 | 内 容 | 结 果 |
测定结果的总和 | 12.6268 | 总平均值 | 0.2037(g/L) |
总极差 | 0.0013 | 相对总极差 | 0.64% |
标准偏差 | 0.00041 | 相对标准偏差 | 0.20% |
=0.00041
3 该方法的不确定度计算
3.1 总余氯滴定分析过程
用硫代硫酸钠标准滴定溶液测定氯含量,其滴定分析过程见图4。
图4 滴定分析过程分解图
硫代硫酸钠溶液的标准和样品中总氧化性氯含量测定的计算公式为:
式中:Vc 表示测定样品时消耗的硫代硫酸钠标准滴定溶液的体积;
Vb 表示标定硫代硫酸钠溶液时消耗硫代硫酸钠溶液的体积;
3.2 滴定分析过程中的因果关系
滴定分析中的因果关系见图5。
图5 氧化还原滴定测定余氯的因果关系图
根据实验的具体数据对引起方法不确定的各因素进行分项计算,并作方法的不确定度计算。
表9 方法不确定度分项计算结果表
符号 | 说明 | X | 标准不确定度 U(x) | 相对标准不确定度U(x)/x |
rep | 重复性 | 1 | 0.001 | 0.001 |
mK2Cr2O7 | K2Cr2O7的质量 | 0.16795 | 0.00012g | 0.00071 |
PK2Cr2O7 | K2Cr2O7的纯度 | 100%±0.05% | 0.00029 | 0.00029 |
Vb | 标定Na2S2O3消耗的体积 | 34.38 | 0.019mL | 0.00055 |
MK2Cr2O7 | K2Cr2O7的摩尔质量 | 294.1846g/mol | 0.0012g/mol | 0.0000041 |
Vc | 测定样消耗Na2S2O3体积 | 1.154 | 0.0023mL | 0.0020 |
V样 | 吸取样品的体积 | 10.00 | 0.0063mL | 0.00063 |
M样 | 样品的摩尔质量 | 281.68959g/mol | 0.00338g/mol | 0.000012 |
ρ | 样品的含量 | 0.2045 | 0.0005 | 0.0025 |
U(x)/x = [0.0012+0.000712+0.000292+0.000552+0.00000412+0.00202+0.000632+0.0000122]1/2
= 0.0025
U(x) = 0.0025×0.2045 = 0.0005
即测定结果0.2045g/L的不确定度为0.0005。
4 小结
4.1标准物质样品均匀性良好
本项目研制的总余氯标准物质样品瓶间均匀性检验结果总平均值为0.2045g/L,相对标准偏差(RSD)为0.09%;瓶内均匀性结果总平均值为0.2044g/L,RSD为0.07%。
本部分实验共抽样33瓶,其结果总平均值为0.2045g/L,RSD为0.07%。实验结果表明,该标准物质样品瓶内均匀性检验及瓶间均匀性检验的相对标准偏差均达到要求,可认为该样品均匀一致。
4.2 瓶密封装样品稳定性良好
该标准物质在6个月稳定性检验期内,累计测定62次,测定结果总平均值为0.2037g/L,总极差为0.0013g/L,相对总极差为0.64%,RSD为0.20%,因此认为该标准物质在检验期内稳定。


